
【题目】碳酸氢钠是重要的化工产品。用标准盐酸溶液滴定可测定碳酸氢钠样品中碳酸氢钠含量。已知碳酸氢钠受热易分解,且在250℃~270℃分解完全。
完成下列填空:
(1)测定碳酸氢钠含量的实验步骤:用电子天平称取碳酸氢钠样品(准确到_____g),加入锥形瓶中,加入使之完全溶解;加入甲基橙指示剂,用标准盐酸溶液滴定。当滴定至溶液由_____色变为_____色,半分钟不变色为滴定终点,记录读数。该实验不能用酚酞作指示剂的原因是_____。
(2)若碳酸氢钠样品质量为0.840g,用0.5000mol/L的标准盐酸溶液滴定至终点,消耗标准盐酸溶液19.50mL。样品中NaHCO3的质量分数为_____(保留3位小数)。
(3)如果滴定尖嘴部分在滴定过程中出现气泡,且滴定终点读数时气泡未消失,会导致测定结果____(选填“偏高”、“偏低”或“不受影响”)。
(4)碳酸氢钠样品含有少量水分(<0.5%)和氯化钠。以下是测定碳酸氢钠样品中水分的实验方案(样品中NaHCO3含量已知)。
①在恒重的坩埚中称取碳酸氢钠样品,样品和坩埚的质量为m1g。
②将样品和坩埚置于电热炉内,在250℃~270℃加热分解至完全,经恒重,样品和坩埚的质量为m2g。
③……。
该实验方案中,质量差(m1-m2)是_____的质量。若所称取样品中NaHCO3的质量为m3g,则样品中水分的质量m=_____(用含m、m1、m2的代数式表示)。
【答案】0.001 黄 橙 滴定终点溶液呈弱酸性,酚酞的变色范围为8-10,无法准确判断滴定终点 0.975 偏低 碳酸氢钠分解生成的CO2、H2O和样品中的含有的水分 m1-m2-![]()
【解析】
(1)电子天平能准确到小数点后三位;碳酸氢钠的溶液中滴加甲基橙指示剂,溶液呈黄色;而弱酸性的溶液中滴加甲基橙指示剂,溶液呈橙色;酚酞试液在pH≥8的溶液中才呈红色;
(2)根据NaHCO3~HCl,则n(NaHCO3)=n(HCl)计算;
(3)根据c(待测)= 分析不当操作对V(标准)的影响,以此判断浓度的误差;
分析不当操作对V(标准)的影响,以此判断浓度的误差;
(4)由2NaHCO3![]() Na2CO3+H2O+CO2↑可知加热前后固体质量减轻,主要是生成CO2气体和水蒸气;先计算出m3gNaHCO3分解生成的水和CO2的质量,再计算样品中含有的水分质量。
Na2CO3+H2O+CO2↑可知加热前后固体质量减轻,主要是生成CO2气体和水蒸气;先计算出m3gNaHCO3分解生成的水和CO2的质量,再计算样品中含有的水分质量。
(1)用电子天平称取碳酸氢钠样品能准确到0.001g;碳酸氢钠溶液中加入甲基橙指示剂,溶液呈黄色,用标准盐酸溶液滴定,当滴定至溶液由黄色变为橙色,半分钟不变色为滴定终点;因滴定终点溶液呈弱酸性,而酚酞试液的变色范围为8-10,用酚酞作指示剂将无法准确判断滴定终点;
(2)滴定至终点消耗0.5000mol/L的标准盐酸溶液19.50mL,则参加反应的HCl为0.5000mol/L×0.01950L=0.00975mol,根据NaHCO3~HCl,则n(NaHCO3)=n(HCl),0.840g样品中m(NaHCO3)=0.00975mol×84g/mol=0.819g,故样品中NaHCO3的质量分数为![]() =0.975;
=0.975;
(3)滴定管尖嘴部分在滴定前没有气泡,滴定过程中出现气泡,且滴定终点读数时气泡未消失,导致消耗标准液偏小,则测定结果偏低;
(4)已知2NaHCO3![]() Na2CO3+H2O+CO2↑,则该实验方案中,质量差(m1-m2)是碳酸氢钠分解生成的CO2、H2O和样品中的含有的水分;称取样品中NaHCO3的质量为m3g,则完全反应生成的碳酸钠质量为m4g,
Na2CO3+H2O+CO2↑,则该实验方案中,质量差(m1-m2)是碳酸氢钠分解生成的CO2、H2O和样品中的含有的水分;称取样品中NaHCO3的质量为m3g,则完全反应生成的碳酸钠质量为m4g,

m4=![]() g,生成的水和CO2的质量为m3g -
g,生成的水和CO2的质量为m3g - ![]() g=
g=![]() m3g,故所则样品中水分的质量m= m1-m2-
m3g,故所则样品中水分的质量m= m1-m2-![]() m3g。
m3g。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】有甲、乙两种物质:

(1)乙中含有的官能团的名称为:氯原子和______________。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
![]()
其中反应I的反应类型是___________,反应II的条件是_______________,反应III的化学方程式为__________________________________(不需注明反应条件)。
(3)下列物质不能与乙反应的是_________(选填序号)。
a.金属钠 b.溴水 c.碳酸钠溶液 d.氢氧化钠溶液
(4)请设计实验证明乙中含有氯元素。
操作 | 现象 | 结论 |
______________ | ___________ | 乙中含有氯元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
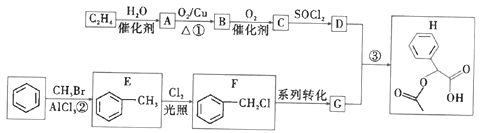
【题目】乙烯和苯是有机合成的基础原料,图中是有机物H( )的合成路线(部分产物和条件已省略):
)的合成路线(部分产物和条件已省略):
已知:![]() 。
。
请回答下列问题:
(1)B的官能团名称为__________________,反应①②的反应类型分别为_________、_____________。E的名称为_______________。
(2)写出反应③的化学方程式:________________。
(3)P与乙烯的最简式相同,其相对分子质量为56,P的所有可能的结构(含P)数目为__________种(不考虑立体异构),写出P的属于环烃的同分异构体的结构简式:____________________。
(4)![]() 是苯的同系物,M的核磁共振氢谱有2组峰,且峰面积比为2∶3,M的二氯代物有________种。
是苯的同系物,M的核磁共振氢谱有2组峰,且峰面积比为2∶3,M的二氯代物有________种。
(5)已知: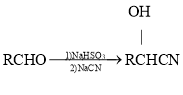 。参照上述流程,设计以F为原料制备G的合成路线:
。参照上述流程,设计以F为原料制备G的合成路线:
 ________________________(无机试剂任选)。
________________________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。请回答下列问题:
(1)基态Fe原子的价电子轨道表示式(电子排布图)为____,O2-核外电子有___种运动状态。
(2)锂的紫红色焰色是一种_______光谱,LiFePO4中阴离子VSEPR模型名称为______,中心原子的杂化轨道类型为____。
(3)一般情况下,同种物质固态时密度比液态大,但普通冰的密度比水小,原因是____________;H2O2难溶于CS2,简要说明理由:____________________。
(4)Li2O是离子晶体,其晶体能可通过如图甲的Born - Haber循环计算得到。可知,Li2O晶格能为____kJ/mol。

(5)磷化钛熔点高、硬度大,其晶胞如图乙所示。
①磷化钛晶体中Ti原子周围最邻近的Ti数目为____;设晶体中Ti原子与最邻近的P原子之间的距离为r,则Ti原子与跟它次邻近的P原子之间的距离为_______。
②设磷化钛晶体中Ti、P原子半径分别为a pm、b pm,它们在晶体中紧密接触,则该晶胞中原子的空间利用率为_____ (用a、b表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如下:

1mol该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为a(不考虑醇羟基和硝基与氢氧化钠的反应,下同),溶液蒸干得到的固体产物再与足量的干燥碱石灰共热,又消耗氢氧化钠的物质的量为b,则a,b分别是( )
已知:![]()
A.5mol,10mol B.6mol,2mol C.8mol,4mol D.8mol,2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对乙烯和聚乙烯的描述中,不正确的是( )
A.乙烯是纯净物,聚乙烯是混合物
B.常温下,乙烯为气态,聚乙烯为固态
C.乙烯的化学性质与聚乙烯相同
D.取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向10 mL 0.1 mol/LNaOH溶液中,逐滴加入10 mL浓度为c mol/L的HF稀溶液。已知 25℃时:①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH=-67.7 kJ/mol ②H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol。请根据信息判断,下列说法中不正确的是
A.整个滴加过程中,水的电离程度不一定存在先增大后减小的变化趋势
B.将氢氟酸溶液温度由25℃升高到35℃时,HF的电离程度减小(不考虑挥发)
C.当c>0.1时,溶液中才有可能存在c(Na+)=c(F-)
D.若滴定过程中存在:c(Na+)>c(OH-)>c(F-)>c(H+),则c一定小于0.1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室产生的废液中的阳离子只可能含有Na+、NH4+、Ba2+、Cu2+、Al3+、Fe2+、Fe3+中的某几种,实验室设计了下述方案对废液进行处理,以回收金属,保护环境。
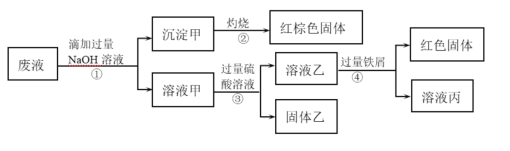
已知:步骤①中,滴加NaOH溶液过程中产生的沉淀会部分溶解。下列说法中正确的是
A.根据步骤①的现象,说明废液中一定含有Al3+
B.由步骤②中红棕色固体可知,废液中一定存在Fe3+
C.沉淀甲中可能含有Al(OH)3
D.该废液中一定含有NH4+、Ba2+、Cu2+、Fe2+和Fe3+至少存在一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】呋喃酚是生产呋喃丹、好安威等农药的主要中间体,是高附加值的精细化工产品。一种以邻氯苯酚(A)为主要原料合成呋喃酚(F)的流程如下:

回答下列问题:
(1)A物质核磁共振氢谱共有______个峰,④的反应类型是_______,C和D中含有的相同官能团的名称是________。
(2)下列试剂中,能和D反应的有__________(填标号)。
A.溴水 B.酸性K2Cr2O7溶液 C.FeCl2溶液 D.纯碱溶液
(3)写出反应①的化学方程式是__________(有机物用结构简式表示,下同)。
(4)有机物B可由异丁烷经三步反应合成:
![]()
条件a为________, Y 生成 B 的化学方程式为 _______。
(5)呋喃酚的同分异构体很多,写出符合下列条件的所有同分异构体的结构简式____ 。
①苯环上的一氯代物只有一种 ②能发生银镜反应的芳香酯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com