
| A. | C4H10 O (醇类) | B. | C3H6Cl(不饱和卤代烃) | ||
| C. | C4H8O2(酯类) | D. | C9H12(芳香烃) |
分析 A.-C4H9的同分异构体是4种,根据基元法确定C4H10O的醇类同分异构体数目;
B.该化合物是含有碳碳双键的卤代烃,即相当于是丙烯中的1个氢原子被氯原子取代后的生成物,所以共计有3种,又因为1-氯-1丙烯存在顺反异构,所以总共是4种;
C.根据酯基位置异构和碳链异构分析C4H8O2的酯类同分异构体;
D.C9H12符合苯的同系物通式,含一个苯环,剩余3个碳可组成3个甲基、1个甲基和1个乙基、1个丙基,取代苯环上氢原子得同分异构体.
解答 解:A.-C4H9的同分异构体是4种,因此C4H10O的醇类同分异构体数目是4种,故A正确;
B.根据化学式C3H5Cl可知,该化合物是含有碳碳双键的卤代烃,即相当于是丙烯中的1个氢原子被氯原子取代后的生成物,所以共计有3种:CH2═CHCH2Cl、CHCl═CHCH3、CH2═CClCH3,又因为CHCl═CHCH3存在顺反异构,所以总共是4种,故B正确;
C.根据酯基位置异构和碳链异构可得:HCOOCH2CH2CH3、HCOOCH(CH3)2、CH3COOCH2CH3、CH3CH2COOCH3,符合条件的共4种,故C正确;
D.分子式为C9H12的单环芳烃共有8种同分异构体,其中二种丙苯:正丙苯和异丙苯,三种甲乙苯:邻间对三种,三种三甲苯:邻三甲苯、偏三甲苯和均三甲苯,故D错误;
故选D.
点评 本题考查同分异构体的书写,题目难度不大,掌握同分异构体判断的方法和规则是解题关键,要认真学习有机物的结构特点和同分异构体的判断方法.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 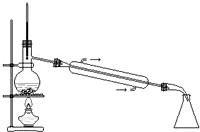 实验室中制取少量蒸馏水 | B. | 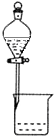 分离碘和酒精 | ||
| C. | 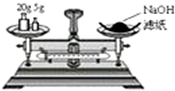 称量氢氧化钠固体 | D. | 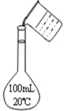 配制100 mL 0.10 mol•L-1盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 海水成分 | Na+ | Ca2+ | Mg2+ | HCO3- | Zn2+ |
| 含量/mol•L-1 | 0.4 | 0.002 | 0.045 | 0.002 | 10-7 |
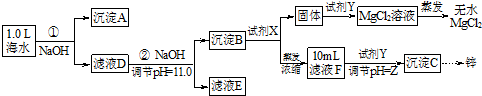
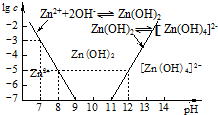
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
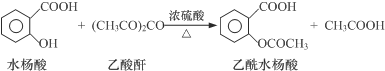
| 试剂 | 沸点(℃) | 溶解度 | 化学性质 |
| 水杨酸 | 211 | 微溶于冷水,易溶于热水 | |
| 乙酸酐 | 139 | 在水中逐渐分解 | |
| 乙酰水杨酸 | 微溶于水 | 与碳酸钠反应生成水溶性盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ①②⑤ | C. | ② | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LHF中含有H-F键的数目为0.5NA | |
| B. | 常温下,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| C. | 常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| D. | 电解饱和食盐水,阳极产生22.4L气体时,电路中通过的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 青蒿素易溶于水和酒精 | |
| B. | 青蒿素中含多个环状结构,其中有一个六元碳环 | |
| C. | 青蒿素中含过氧键,过氧键属于极性共价键 | |
| D. | 青蒿素和纤维素都属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L CH3COONa溶液显碱性 | |
| B. | 0.1mol/L醋酸溶液的pH=3 | |
| C. | 物质的量浓度相同的盐酸和醋酸同时与锌反应,开始时锌粒跟盐酸反应比跟醋酸反应的速率快 | |
| D. | 中和100mL1mol/L 的CH3COOH溶液需要100mL1mol/L的NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com