
| A. | 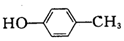 对甲苯酚 属于芳香化合物 对甲苯酚 属于芳香化合物 | B. | 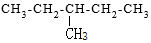 3-甲基戊烷 属于烷烃 3-甲基戊烷 属于烷烃 | ||
| C. | 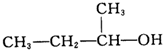 2-甲基-1-丙醇-元醇 2-甲基-1-丙醇-元醇 | D. | 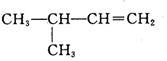 3-甲基-1-丁烯 属于脂肪烃 3-甲基-1-丁烯 属于脂肪烃 |
分析 A.含酚-OH;
B.为饱和烃;
C.含-OH,且含-OH的最长碳链含4个C原子;
D.含碳碳双键,且含双键的最长碳链有4个C,3号C上有甲基.
解答 解:A.含酚-OH,-OH与甲基位于苯环的对位,则名称为对甲苯酚,含苯环属于芳香化合物,故A正确;
B.为饱和烃,名称为3-甲基戊烷,属于烷烃,故B正确;
C.含-OH,且含-OH的最长碳链含4个C原子,则名称为2-丁醇,故C错误;
D.含碳碳双键,且含双键的最长碳链有4个C,3号C上有甲基,则名称为3-甲基-1-丁烯,由链状结构可知属于脂肪烃,故D正确;
故选C.
点评 本题考查有机物的官能团及名称,为高频考点,把握有机物的结构、官能团、分类为解答的关键,侧重分析与应用能力的考查,注重基础知识的夯实,题目难度不大.


科目:高中化学 来源: 题型:解答题
 液氨气化后分解产生的氢气可作为燃料供给氢氧燃料电池.
液氨气化后分解产生的氢气可作为燃料供给氢氧燃料电池.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该装置将化学能转化为电能 | |
| B. | Zn棒与Cu棒作用一样,都只做电极材料 | |
| C. | Cu棒上发生还原反应 | |
| D. | 该装置发生反应的离子方程式是:Zn+Cu2+=Zn2++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  图中,Zn-MnO2干电池放电时,MnO2被氧化 | |
| B. |  图中,电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等 | |
| C. |  图中,在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl7-形式存在,则阳极反应式为:Al-3e-+7AlCl4-=4Al2Cl7- | |
| D. |  图中,K分别与M、N连接,均可保护Fe电极,连接M时为“牺牲阳极的阴极保护法” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属元素之间只能形成共价化合物 | |
| B. | 第IA族元素的金属性一定比IIA族元素的金属性强 | |
| C. | 短周期中,同周期元素的离子半径从左到右逐渐减小 | |
| D. | 非金属元素的气态氢化物还原性越强,对应元素的最高价含氧酸酸性越弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
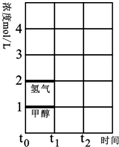 工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H.如表所列数据是该反应在不同温度下的化学平衡常数(K).
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H.如表所列数据是该反应在不同温度下的化学平衡常数(K).| 温度 | 250℃ | 300℃ | 350℃ |
| K/L2•mol-2 | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )的方法中,原子经济性最好的是(反应均在一定条件下进行)( )
)的方法中,原子经济性最好的是(反应均在一定条件下进行)( )| A. |  | B. |  | ||
| C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③⑤ | C. | ①②③④ | D. | ②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com