
某课外小组同学用下图所示装置进行实验(夹持装置已省略)。

(1)用该装置制备NO2并研究其性质。
①收集一试管NO2,取下试管B倒立在水中,观察到的现象是________________。
②该反应的化学方程式是________________________________。
③C中NaOH溶液吸收NO2,生成两种盐,且被氧 化与被还原的NO2的物质的量之比是1:1,请写出该反应的离子方程式________________________________。
(2)该装置也可用于制备Cl2并研究其性质。
①若A中固体为漂白粉,滴入浓盐酸,则A中发生反应的化学方程式是___________。
②在B中放一小块湿润的淀粉碘化钾试纸,可观察到试纸变蓝,请结合离子方程式解释原因________________________________________。
③硫代硫酸钠(Na2S2O3)可替代NaOH溶液吸收氯气,已知25.0mL 0.1 mol·L-1的Na2S2O3溶液恰好把标准状况下224 mL Cl2完全转化为Cl-时,S2O32-转化成_____(填选项)。
a. S2- b. S c. SO32- d. SO42-
(12分,每空2分)(1)①液面上升,红棕色气体变为无色
②3NO2+H2O=2HNO3+NO ③2NO2+2OH-=NO2-+NO3-+H2O
(2)①Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
②Cl2+2I-=2Cl-+I2 I-被氧化为I2,遇淀粉变蓝 ③d
【解析】
试题分析:(1)①NO2溶于水生成硝酸和NO,所以收集一试管NO2,取下试管B倒立在水中,观察到的现象是液面上升,红棕色气体变为无色。
②该反应的化学方程式是3NO2+H2O=2HNO3+NO。
③由于被氧化与被还原的NO2的物质的量之比是1:1,所以生成的硝酸钠和亚硝酸钠的物质的量之比是1:1的,则该反应的离子方程式是2NO2+2OH-=NO2-+NO3-+H2O。
(2)①漂白粉的有效成分是次氯酸钙,次氯酸钙具有强氧化性,能把浓盐酸氧化生成氯气,反应的化学方程式是Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O。
②氯气具有强氧化性,I-被氧化为I2,遇淀粉变蓝,反应的离子方程式是Cl2+2I-=2Cl-+I2。
③Na2S2O3中S元素的化合价是+2价,设氧化产物中S元素的化合价是n,则根据电子的得失守恒可知,0.025×0.1×(n-2)×2=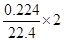 ,解得n=6,即氧化产物是硫酸钠,答案选d。
,解得n=6,即氧化产物是硫酸钠,答案选d。
考点:考查NO2的性质、氯气的制备、氧化还原反应的有关判断和计算、方程式的书写
点评:该题是中等难度的试题,也是高考中的常见题型。试题紧扣教材,贴近高考,有利于调动学生的学习兴趣,激发学生的学习积极性。也有利于培养学生的逻辑推理能力和发散思维能力,提升学生的学科素养。


科目:高中化学 来源: 题型:
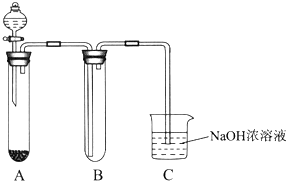 某课外小组同学用下图所示装置进行实验(夹持装置已省略).
某课外小组同学用下图所示装置进行实验(夹持装置已省略).查看答案和解析>>
科目:高中化学 来源:天津市耀华中学2012届高三第一次模拟考试化学试题 题型:058
某课外小组同学用下图所示装置在实验室制各氯气并探究其相关性质(夹持设备已略).

(1)制备氯气选用的药品为:漂白粉固体和浓盐酸,相关的化学反应方程式为________.
(2)装置B的作用之一是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象________.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中①、②、③依次放
入________(选填字母).

(4)设计装置D、E的目的是比较氯、溴、碘的菲金属性.当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为________色,说明氯的非金属性大于溴;之后打开活塞,将装置D中少量溶液加入装置E中,振荡;观察到的现象是________,则说明溴的非金属性大于碘.
(5)有同学提出该实验方案仍有不足,请说明其中两点不足及原因是:
①________;
②________.
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市西城区(北区)高一上学期期末考试化学试卷(带解析) 题型:填空题
某课外小组同学用下图所示装置进行实验(夹持装置已省略)。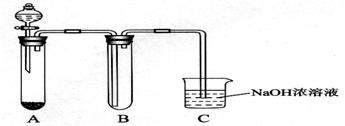
(1)用该装置制备NO2并研究其性质。
①收集一试管NO2,取下试管B倒立在水中,观察到的现象是________________。
②该反应的化学方程式是________________________________。
③C中NaOH溶液吸收NO2,生成两种盐,且被氧 化与被还原的NO2的物质的量之比是1:1,请写出该反应的离子方程式________________________________。
(2)该装置也可用于制备Cl2并研究其性质。
①若A中固体为漂白粉,滴入浓盐酸,则A中发生反应的化学方程式是___________。
②在B中放一小块湿润的淀粉碘化钾试纸,可观察到试纸变蓝,请结合离子方程式解释原因________________________________________。
③硫代硫酸钠(Na2S2O3)可替代NaOH溶液吸收氯气,已知25.0mL 0.1 mol·L-1的Na2S2O3溶液恰好把标准状况下224 mL Cl2完全转化为Cl-时,S2O32-转化成_____(填选项)。
a. S2- b. S c. SO32- d. SO42-
查看答案和解析>>
科目:高中化学 来源:2013-2014学年安徽省濉溪县高三第四次月考化学试卷(解析版) 题型:填空题
中学化学中常见的几种物质存在下图所示的转化关系。其中, A是一种黑色粉末状固体,C是一种黄绿色气体,实验室中常用E溶液吸收多余的C。(图中部分产物和反应条件已略去)。

试回答下列问题:
(1)写出A与B的浓溶液反应的化学方程式 。
(2)将B的浓溶液与H的浓溶液混合,立即产生大量气体C,该反应的离子方程式为 。
(3)某课外小组同学用E溶液吸收C,利用下图所示装置向吸收液中持续通入SO2气体。实验过程中观察到如下现象:

①开始时,溶液上方出现白雾,试纸a变红。甲同学认为是HCl使a变红,乙同学不同意甲的观点,乙同学认为使a变红的是
(写出一种即可)。
②片刻后,溶液上方出现黄绿色气体,试纸b变蓝。用离子方程式解释b变蓝的原因: 。
③最终试纸b褪色。同学们认为可能的原因有两种:一是I2有还原性,黄绿色气体等物质将其氧化成IO3-,从而使蓝色消失;二是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com