
����Ŀ����������ѧ̼��������ʱ���鵽���������ϣ�
��CO2+Na2CO3+H2O=2NaHCO3 �� CO2ͨ�뱥��̼������Һ�������ɫ������CO2�����ڱ���̼��������Һ��
��̼���ơ�̼�������ڲ�ͬ�¶��µ��ܽ�������
0 �� | 10 �� | 20 �� | 30 �� | |
Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 |
������ʵ��1����֤CO2ͨ�뱥��̼������Һ�������ɫ����
������̼������Һ��ȡ100 g 20 ���ˮ������35 g̼���ƹ��壬������ã�ȡ�ϲ���Һ��
������װ��һ����ʵ�飬����5���������Ƶõ�̼������Һ��ͨ��CO2��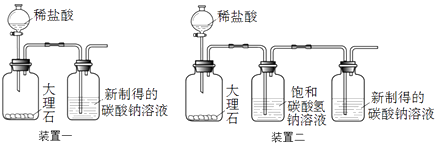
���������⡿ʵ���У�ʼ��û�п�����������ԭ����ʲô�أ���������������ʵ��̽����
������ʵ��2��
ʵ����� | ʵ������ |
��ȡ100 g 20 ���ˮ������35 g̼���ƹ��壬������ã�ȡ�ϲ���Һ | û�г��ְ�ɫ���� |
��1����0 ��~30 �棬Na2CO3��NaHCO3���ܽ�����¶ȱ仯Ӱ��ϴ������
��2������ʯ��ϡ���ᷴӦ�����ӷ���ʽΪ��
��3��װ�ö��б���̼��������Һ����������
��4��������ʵ��3��
ʵ����� | ʵ������ |
��ȡ100 g�ȿ�ˮ������35 g̼���ƹ��壬��ȫ�ܽ⣬�ٽ�����20 �棬ȡ�ϲ���Һ | װ��һ��װ�ö��е�̼������Һ�о����ְ�ɫ���� |
�����������ʵ����û�п������������ԭ������
��5��CO2ͨ�뱥��̼������Һ�������ɫ������ԭ������
���𰸡�
��1��Na2CO3
��2��CaCO3 +2H��=Ca2��+H2O+CO2��
��3���ų�HCl�ĸ���
��4�����Ƶ�̼������Һû�дﵽ����
��5��̼�������ܽ��С��̼����,ˮ����,���ɵ�̼�����Ƶ��������ڷ�Ӧ��̼����
����������1����0 ��~30 �棬Na2CO3��NaHCO3���ܽ�����¶ȱ仯Ӱ��ϴ���� Na2CO3��
��2������ʯ��ϡ���ᷴӦ�����ӷ���ʽΪ��CaCO3 +2H��=Ca2��+H2O+CO2����
��3��װ�ö��б���̼��������Һ�������������Ȼ������壬�Ӷ��ų��Ȼ��������ʵ��ĸ��ţ�
��4�������������ʵ����û�п������������ԭ�������Ƶ�̼������Һû�дﵽ���ͣ�
��5��CO2ͨ�뱥��̼������Һ�������ɫ������ԭ���ǣ�̼�������ܽ��С��̼���ƣ����ŷ�Ӧ�Ľ��У�ˮ��������С�����ɵ�̼�����Ƶ��������ڷ�Ӧ��̼���ơ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴Ӧ��2A��g��+B��g��2C��g����H��0�����и�ͼ����ȷ���ǣ� ��
A.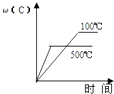
B.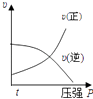
C.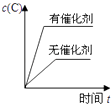
D.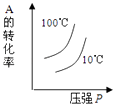
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷�ӦZn+Cu2+= Zn2++ Cu��Ƴ�ԭ��ء���õ�صĸ����������͵������Һѡ���������
A. Zn��Cu��ZnSO4B. Cu��Zn�� ZnCl2
C. Cu��Zn��CuCl2D. Zn��Cu��CuSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ������һ�����ォ��ˮ�е��л�������ǵ��ۣ��Ļ�ѧ��ֱ��ת��Ϊ���ܣ������ô˵��������϶�ͭ������˵������ȷ���ǣ� �� 
A.���������ӽ���Ĥ���������ƶ�
B.ͭ�缫Ӧ��X������
C.M�缫��Ӧʽ����C6H10O5��n+7nH2O��24ne���T6nCO2��+24nH+
D.��N�缫����0.2 mol����ʱ�������缫����16g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʻ�Ϊͬ���칹�����
A. ����������
B. ��������ϩ
C. ��ϩ���ϩ
D. ���������춡��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ԭ��������������Ⱦ�����й㷺��Ӧ�ã���ҵ�ϳ�������ͼ��ʾ���װ�ã��������Ļ�������[Fe��CN��6]3���ɽ���̬�������е�����ת��Ϊ�����õ�������ת��Ϊ[Fe��CN��6]4�� �� ͨ���⣬Ȼ��ͨ��H2S���Դ���������˵������ȷ���ǣ� �� 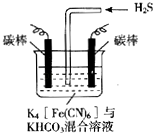
A.���ʱ������ӦʽΪ[Fe��CN��6]4����e��=[Fe��CN��6]3��
B.����������������Һ��pH���
C.������������Ҫ���ϲ���K4[Fe��CN��6]��KHCO3
D.ͨ��H2Sʱ������Ӧ�����ӷ���ʽΪ��2[Fe��CN��6]3��+2CO32��+H2S=2[Fe��CN��6]4��+2HCO3��+S��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��TiO2�ڹ�ҵ�������ճ�����������Ҫ��;��
��1����ҵ����������ʯ��FeTiO3 �� ��FeO��Al2O3��SiO2�����ʣ�����������Ӧ�Ƶã� 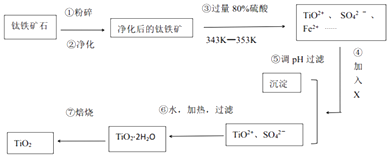
���У�����۷����ķ�ӦΪ��2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O��
��i�������ѿ�ʯʱ������Ũ����������Һ��������д���ù������������������Ӧ�����ӷ�Ӧ����ʽ�� ��
��ii��������X������
��iii���ܢ�������Ŀ���� ��
��iv��д���Ļ�ѧ��Ӧ����ʽ ��
��2��TiO2��ͨ���������ַ����Ʊ������ѣ�����һ���Ƚ�TiO2��Cl2��C��Ӧ�õ�TiCl4 �� ����þ��ԭ�õ�Ti��
��i��д������TiCl4�Ļ�ѧ��Ӧ����ʽ
�������ǵ��TiO2�����Ti��ͬʱ����O2����
����������TiO2��������ʯīΪ����������CaOΪ���Һ����̼�������۳أ�
��ii��������Ӧ�ĵ缫��ӦʽΪ ��
��iii�����������趨������۳��м���̼���ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С����ij2L�ܱ������м���һ�����Ĺ���A������B��������ӦA��s��+2B��g��D��g��+E��g����H=QkJmol��1 �� ��T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ����ʵ������±���
ʱ�䣨min�� | 0 | 10 | 20 | 30 | 40 | 50 |
B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
��1��T1��ʱ���÷�Ӧ��ƽ�ⳣ��K=��
��2��30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬���ݱ��е������жϸı������������������ĸ��ţ���
a��ͨ��һ������B
b������һ�����Ĺ���A
c���ʵ���С���������
d�����߷�Ӧ��ϵ�¶�
e��ͬʱ����0.2molB��0.1molD,0.1molE
��3�����ڸ÷�Ӧ���ø����ʱ�ʾ�ķ�Ӧ������ʱ��Ĺ�ϵʾ������Ϊ��ͼ�е�������ţ� 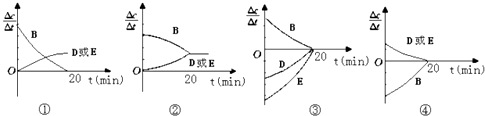
��4��ά��������������¶�T1���䣬����������м���1.60molB,0.20molD,0.20molE��nmolA���ﵽƽ����������20����ʱ�����ʵ�Ũ����ȫ��ͬʱ����Ͷ�����A�����ʵ���nȡֵ��Χmol��
��5��ά��������������¶�T1���䣬�����ʵ���ʼ���ʵ���Ϊ��n��A��=1.0mol��n��B��=3.0mol��n��D��=amol��n��E��=0mol���ﵽƽ���n��E��=0.50mol����a= ��
��6�������ܱ��������ȣ�ʵ����B��ת����B%��ʱ��仯��ʾ��ͼ��ͼ��ʾ��ͼ��֪��Q0������ڡ���С�ڡ�����c��v��v�棨����ڡ�����С�ڡ����ڡ����� 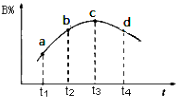
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com