
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
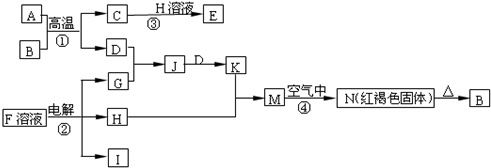
| A�������������̣�ÿ����1molKMnO4����ת��6mol���� | ||||
B���ڶ������ʱ�������缫��ӦʽΪ2MnO
| ||||
C���ڶ����������ӷ���ʽΪ��2H2O
| ||||
| D���ڶ������ʱ������ΧpH��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����;���ֱ�ﵽƽ��ʱ������ϵ����ͬ�����Ũ����� |
| B����;���ֱ�ﵽƽ��ʱ������ϵ����ͬ��������������� |
| C����;���ֱ�ﵽƽ��ʱ������ϵ����ͬ����ķ�Ӧ������� |
| D����;���ֱ�ﵽƽ��ʱ����������ܶ��Ǣ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
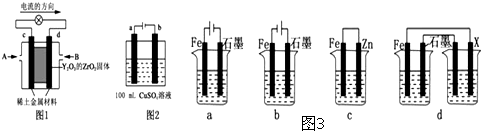
| A��ˮ����������̫���ܵ�صij��ò��� |
| B�������������������Բ������п�ʴ���Ƴ� |
| C�������¿�����������������ʢװŨ�����Ũ���� |
| D����������������ˮ����ɱ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ı���������Ӧ���ת��������ƽ�ⳣ��Ҳһ������ | ||||||
| B����Ӧ2NO2��g���TN2O4��g����H��0�������¶ȸ÷�Ӧƽ�ⳣ������ | ||||||
| C�����ڸ������淴Ӧ���¶�һ��ʱ���������淴Ӧ��ƽ�ⳣ����� | ||||||
D��CO2+H2
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.265mol/L |
| B��0.525mol/L |
| C��0.21mol/L |
| D��0.42mol/L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com