
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
 能源是现代社会发展的支柱之一,化学能是重要的能源.
能源是现代社会发展的支柱之一,化学能是重要的能源.
查看答案和解析>>
科目:高中化学 来源: 题型:
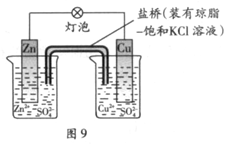
下图是铜锌原电池装置。其电池的总反应是:Zn(s) + CuSO4(aq)== ZnSO4(aq) + Cu(s)。若该电池中两电极的总质量为300g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为298g。


请回答以下问题:
⑴R的名称是___________,其作用是__________________。R中的阳离子移向___________ (填A或B)中的溶液。
⑵电极Y的材料是________,B中的电解质溶液是________________。
⑶X为原电池的___ 极,其电极反应式是______________。
(4)产生铜的质量为 ;转移的电子的物质的量为 。
(5) 高铁酸盐在能源环保领域有广泛用途。我国学者提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如右图所示。
① Fe电极作 极 (填“阴”或“阳”);
② Ni电极的电极反应式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(16分)下图是铜锌原电池装置。其电池的总反应是:Zn(s) + CuSO4(aq)==ZnSO4(aq) + Cu(s)。七彩教育网若该电池中两电极的总质量为300g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为298g。
请回答以下问题:
⑴R的名称是___________,其作用是__________________。R中的阳离子移向___________ (填A或B)中的溶液。
⑵电极Y的材料是________,B中的电解质溶液是________________。
⑶X为原电池的___ 极,其电极反应式是______________。
(4)产生铜的质量为 ;转移的电子的物质的量为 。
(5) 高铁酸盐在能源环保领域有广泛用途。我国学者提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如右图所示。
① Fe电极作 极 (填“阴”或“阳”);
② Ni电极的电极反应式为: 。
查看答案和解析>>
科目:高中化学 来源:2010年福建省高二上学期期中考试化学卷 题型:填空题
(16分)下图是铜锌原电池装置。其电池的总反应是:Zn(s) + CuSO4(aq)== ZnSO4(aq) + Cu(s)。七彩教育网若该电池中两电极的总质量为300g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为298g。


请回答以下问题:
⑴R的名称是___________,其作用是__________________。R中的阳离子移向___________ (填A或B)中的溶液。
⑵电极Y的材料是________,B中的电解质溶液是________________。
⑶X为原电池的___ 极,其电极反应式是______________。
(4)产生铜的质量为 ;转移的电子的物质的量为 。
(5) 高铁酸盐在能源环保领域有广泛用途。我国学者提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如右图所示。
① Fe电极作 极 (填“阴”或“阳”);
② Ni电极的电极反应式为: 。
查看答案和解析>>
科目:高中化学 来源:2009-2010学年北京市西城区高一(下)期末化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com