


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
铜及其化合物一般都具有特征颜色,例如Cu、Cu2O呈红色,CuO呈黑色、CuSO4·5H2O呈蓝色等。研究性学习小组甲为检测实验室用H2还原CuO所得的红色固体中是否含有 Cu2O进行了认真探究。
Ⅰ.查阅资料:Cu2O属于碱性氧化物;高温灼烧CuO生成Cu2O;Cu2O在酸性条件下能发生下列反应:
Cu2O+2H+===Cu+Cu2++H2O
Ⅱ.设计实验方案:
方案1:取该红色试样溶于足量的稀硝酸中,观察溶液颜色的变化。
方案2:取该红色试样溶于足量的稀硫酸中,观察溶液是否呈蓝色。
方案3:称得干燥坩埚的质量为a g,取红色试样置于坩埚中称得总质量为b g,在空气中高温灼烧至质量恒定,称得最后总质量为c g。
(1)请你评价方案1和方案2。如果你认为该方案合理,请简述其化学原理;如果你认为该方案不合理,请简述原因。
方案1:____________________________________________________________。
方案2:__________________________________________________________。
(2)方案3中,若确认红色粉末中含有Cu2O,则a、b、c应符合的数学的关系为________,该实验方案最少得进行________次称量。
Ⅲ.研究性学习小组乙,设计了新的探究方案,拟通过干燥管中CuSO4是否变蓝判断红色固体中是否含有Cu2O,装置如图所示:

(3)简述该探究方案中,检验气体发生装置气密性的方法(说明操作方法、现象和结论)
________________________________________________________________________。
(4)为确保探究的科学、合理、安全,你认为实验中还应采取的措施有________(填序号)。
A.在氢气发生器与硬质玻璃管之间加一干燥装置
B.加热前先排尽装置中的空气
C.在盛有硫酸铜的干燥管后再连接一个装有碱石灰的干燥管
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4?5H2O呈蓝色等。研究性学习小组甲为检测实验室用H2还原CuO所得红色固体中是否含有Cu2O进行了认真的探究。
Ⅰ.查阅资料:①Cu2O属于碱性氧化物; ②高温灼烧CuO生成Cu2O;③Cu2O在酸性条件下能发生下列反应:Cu2O+2H+=Cu+Cu2++H2O。
Ⅱ.设计实验方案:
方案1:取该红色试样溶于足量的稀硝酸中,观察溶液颜色变化
方案2:取该红色试样溶于足量的稀硫酸中,观察溶液是否呈蓝色
方案3:称得干燥坩埚的质量为a g ,取红色试样置于坩埚中称得总质量为b g,在空气中高温灼烧至质量恒定,称得最后总质量为c g。
⑴请你评价方案1和方案2。如果你认为方案合理,请简述其化学原理;如果你认为该方案不合理,请简述原因。
方案1 :
方案2 :
⑵方案3中,若确认红色粉末中含有Cu2O,则a、b、c应符合的数学的关系为 ,该实验方案最少得进行 次称量。
Ⅲ.研究性学习小组乙,设计了新的探究方案,拟通过干燥管中CuSO4是否变蓝判断红色固体中是否含有Cu2O,装置如图所示。
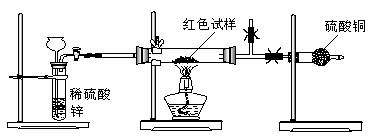
⑶简述该探究方案中,检验气体发生装置气密性的方法(说明操作方法、现象和结论)
。
⑷为确保探究的科学、合理、安全,你认为实验中还应采取的措施有: (填序号)
A.在氢气发生器与硬质玻璃管之间加一个干燥装置
B.加热前先排尽装置中的空气
C.在盛有硫酸铜的干燥管后再连接一个装有碱石灰的干燥管
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4?5H2O呈蓝色等。研究性学习小组甲为检测实验室用H2还原CuO所得红色固体中是否含有Cu2O进行了认真的探究。
A.查阅资料:①Cu2O属于碱性氧化物; ②高温灼烧CuO生成Cu2O;③Cu2O在酸性条件下能发生下列反应:Cu2O+2H+=Cu+Cu2++H2O。
B.设计实验方案:
方案1:取该红色试样溶于足量的稀硝酸中,观察溶液颜色变化
方案2:取该红色试样溶于足量的稀硫酸中,观察溶液是否呈蓝色
方案3:称得干燥坩埚的质量为a g ,取红色试样置于坩埚中称得总质量为b g,在空气中高温灼烧至质量恒定,称得最后总质量为c g。
⑴请你评价方案1和方案2。如果你认为方案合理,请简述其化学原理;如果你认为该方案不合理,请简述原因。
方案1 : 。
方案2 : 。
⑵方案3中,若确认红色粉末中含有Cu2O,则a、b、c应符合的数学关系式为 ,该实验方案最少需进行 次称量。
C.研究性学习小组乙,设计了新的探究方案,拟通过干燥管中CuSO4是否变蓝判断红色固体中是否含有Cu2O,装置如图所示。
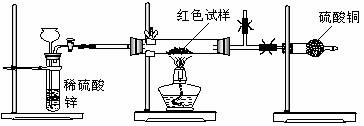
⑶简述该探究方案中,检验气体发生装置气密性的方法(说明操作方法、现象和结论)
。
⑷为确保探究的科学、合理、安全,你认为实验中还应采取的措施有: (填序号)
A.在氢气发生器与硬质玻璃管之间加一个干燥装置
B.加热前先排尽装置中的空气
C.在盛有硫酸铜的干燥管后再连接一个装有碱石灰的干燥管
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com