
某温度时,测得0.01mol/L NaOH溶液的PH为11,则该温度下,水的离子积Kw=_____________。在此温度下,将PH= a 的NaOH溶液Va L与PH= b 的硫酸Vb L混合。
①若所得溶液为中性,且a=12,b=2,则Va :Vb = __________________________
②若所得混合液的PH=10,且a=12,b=2,则Va :Vb = ______________________
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。
请回答下列问题:
(1)煤的气化的主要化学反应方程式为:___________________________。
(2)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:________________________________________。
(3)利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)  CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1
② 2CH3OH(g)  CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
③ CO(g) + H2O(g)  CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
总反应:3H2(g) + 3CO(g)  CH3OCH3(g) + CO2 (g)的ΔH= ___________;
CH3OCH3(g) + CO2 (g)的ΔH= ___________;
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是__________(填字母代号)。
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(4)已知反应②2CH3OH(g)  CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
① 比较此时正、逆反应速率的大小:v正 ______ v逆 (填“>”、“<”或“=”)。
② 若加入CH3OH后,经10 min反应达到平衡,此时
c(CH3OH) = ;该时间内反应速率v(CH3OH) = 。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E都是短周期元素,原子序数逐渐增大,原子半径按B、A、E、D、C依次增大。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)D元素在周期表中的位置是__________
(2)甲物质的电子式是________ __
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中反应的离子方程式是
(4)用电子式表示A的气态氢化物的形成过程
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:CO(g)  C(s) +
C(s) + 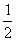 O2(g)的△H为正值,△S为负值。设△H和△S不随温度而变化,下列说法中正确的是( )
O2(g)的△H为正值,△S为负值。设△H和△S不随温度而变化,下列说法中正确的是( )
A.低温下是自发变化
B.高温下是自发变化
C.低温下是非自发变化,高温下是自发变化
D.任何温度下都是非自发变化
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列关于电解质溶液的判断正确的是( )
A.在PH=12的溶液中,K+、Cl-、HCO3-、Na+可以常量共存
B.在PH=0的溶液中,Na+、NO3-、SO32-、K+可以常量共存
C.0.1mol/L一元碱BOH溶液的PH=10,可推知BOH溶液中存在BOH = B+ + OH-
D.在0.1mol/L一元酸HA溶液的PH=3,可推知NaA溶液中存在:A- + H2O HA + OH-
HA + OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,可逆反应2NO2  2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:
2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成n mol O2的同时生成2n mol NO2;
②单位时间内生成n mol O2 的同时生成2n mol NO;
③混合气体的密度不再改变的状态;④混合气体的颜色不再改变的状态;
⑤密闭容器中压强不再改变的状态;
⑥混合气体的平均相对分子质量不再改变的状态。
A.②③⑤⑥ B.①④⑤⑥ C.①③④⑥ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
下表物质与其所含化学键类型、所属化合物类型完全正确的一组是( )
| 选项 | A | B | C | D |
| 物质 | MgCl2 | CO2 | HCl | NaOH |
| 所含化学 键类型 | 离子键、 共价键 | 共价键 | 离子键 | 离子键、 共价键 |
| 所属化合 物类型 | 离子 化合物 | 共价 化合物 | 离子 化合物 | 共价 化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
美国“海狼”潜艇上的核反应堆内使用了液态铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
A.原子半径:Na>Al
B.若把铝钠合金投入一定量的水中只得到无色溶液,则n(Al)≤n(Na)
C.m g不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则铝的质量分数越小
D.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
称取两份铝粉,第一份加入足量的盐酸,第二份加入足量的烧碱溶液,若生成的氢气质量相同,则两份铝粉的质量比为
A.1:1 B.3:2
C.2:3 D.1:6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com