
下列各组物质中,按熔点由低到高排列的是( )
A.O2、I2、Hg B.CO2、Al2O3、KCl
C.Na、K、Rb D.H2S、H2Se、H2Te
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
某温度下,某反应达平衡时平衡常数K=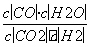 。恒容时,温度升高,H2的浓度减小。下列说法正确的是( )
。恒容时,温度升高,H2的浓度减小。下列说法正确的是( )
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2的浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2OCO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如图所示。
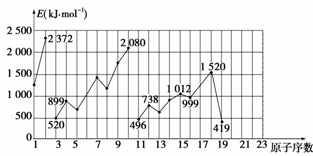
试根据元素在同期表中的位置,分析图中曲线的变化特点,并回答下列问题。
(1)同主族内不同元素的E值变化的特点是_________________________________。各主
族中E值的这种变化特点体现了元素性质的____________变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系式中正确的是________(填写编号,多选倒扣)。
①E(砷)>E(硒) ②E(砷)<E(硒)
③E(溴)>E(硒) ④E(溴)<E(硒)
(3)估计1 mol气态Ca原子失去最外层一个电子所需能量E值的范围:
_____<E<____________。
(4)10号元素E值较大的原因是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)写出与H2O分子电子数相等的微粒________(写一个即可)。
(2)水分子在特定条件下容易得到一个H+形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是________。
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(3)将白色的无水CuSO4固体溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配合离子。请写出生成此配合离子的离子方程式:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于范德华力的叙述不正确的是( )
A.是一种较弱的化学键
B.范德华力较弱,破坏它所需能量较少
C.范德华力对物质的熔、沸点有影响
D.稀有气体原子之间存在范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
下列观点错误的是( )
A.宏观物质都是由微观粒子构成的。微观粒子的种类和数量不同、彼此的结合方式多样,决定了物质的多样性
B.分子是保持物质化学性质的最小粒子,如果分子的组成或结构变了,其化学性质就变了
C.构成宏观物质的微观粒子之间存在多种形式的相互作用,如离子键、共价键等等
D.储存在物质中的化学能在化学反应前后是不变的
查看答案和解析>>
科目:高中化学 来源: 题型:
答案 AB
解析 水分子中各原子已达到稳定结构,H3O+是H+和H2O中的O形成配位键;[B(OH)4]-是3个OH-与B原子形成3个共价键,还有1个OH-的O与B形成配位键;其他项均不能形成配位键。
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z是三种主族元素,如果Xn+阳离子与Yn-阴离子具有相同的电子层结构,Zn-阴离子半径大于Yn-阴离子半径,则三种元素的原子序数由大到小的顺序是( )
A.Z>X>Y B.X>Y>Z
C.Z>Y>X D.X>Z>Y
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com