
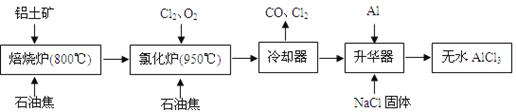
ĪŽĖ®AlCl3æÉÓĆ×÷ÓŠ»śŗĻ³ÉµÄ“߻ƼĮ”¢Ź³Ę·ÅņĖɼĮµČ”£¹¤ŅµÉĻÓÉĀĮĶĮæó£ØÖ÷ŅŖ³É·ÖŹĒA12O3ŗĶFe2O3£©ŗĶŹÆÓĶ½¹£ØÖ÷ŅŖ³É·ÖŹĒC£©°“ĻĀĶ¼ĖłŹ¾Į÷³Ģ½ųŠŠŅ»ĻµĮŠ·“Ó¦Ą“ÖʱøĪŽĖ®AlCl3”£
£Ø1£©ĀČ»ÆĀĮŌŚ¼ÓČČĢõ¼žĻĀŅ×Éż»Ŗ£¬ĘųĢ¬ĀČ»ÆĀĮµÄ»ÆѧŹ½ĪŖAl2Cl6£¬ĆæÖÖŌŖĖŲµÄŌ×Ó×īĶā²ć¾ł“ļµ½8µē×ÓĪČ¶Ø½į¹¹£¬ŌņAlCl3ŹĒ ¾§Ģ壬Ęä½į¹¹Ź½ĪŖ ”£
£Ø2£©ĀČ»ÆĀÆÖŠAl2O3”¢Cl2ŗĶC·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ ”£
£Ø3£©ĄäČ“Ę÷ÅųöµÄĪ²ĘųÖŠŗ¬ÓŠ“óĮæCOŗĶÉŁĮæCl2£¬ŠčÓĆNa2SO3ČÜŅŗ³żČ„Cl2£¬“Ė·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ ”£
£Ø4£©Éż»ŖĘ÷ÖŠÖ÷ŅŖŗ¬ÓŠAlCl3ŗĶFeCl3£¬Šč¼ÓČėÉŁĮæAl£¬Ęä×÷ÓĆŹĒ£ŗ ”£
£Ø5£©AlCl3²śĘ·ÖŠFeŌŖĖŲŗ¬ĮæÖ±½ÓÓ°ĻģĘäĘ·ÖŹ£¬ĪŖ²ā¶Ø²śĘ·ÖŠFeŌŖĖŲµÄŗ¬Į棬ĻÖ³ĘČ”16.25gĪŽĖ®AlCl3²śĘ·£¬ČÜÓŚ¹żĮæµÄNaOHČÜŅŗ£¬¹żĀĖ³ö³ĮµķĪļ£¬³ĮµķĪļ¾Ļ“µÓ”¢×ĘÉÕ”¢ĄäČ“”¢³ĘÖŲ²ŠĮō¹ĢĢåÖŹĮæĪŖ0.32g”£Ōņ²śĘ·ÖŠFeŌŖĖŲµÄŗ¬ĮæĪŖ£ŗ ”£
”¾ÖŖŹ¶µć”æĀĮĢś¼°Ęä»ÆŗĻĪļµÄŠŌÖŹ”¢»Æѧ¼ĘĖć C2 C3
”¾“š°ø½āĪö”æ£Ø1£©·Ö×Ó
£Ø2£©A12O3+3C12+3C 2A1C13+3CO
£Ø3£©SO32-+C12+H2O SO42-+2C1-+2H+
£Ø4£©³żČ„FeCl3”£
£Ø5£©1.4%
½āĪö£ŗ£Ø1£©øł¾ŻĀČ»ÆĀĮŌŚ¼ÓČČĢõ¼žĻĀŅ×Éż»Ŗ£¬ĖµĆ÷AlCl3·ŠµćŗܵĶ£¬Ó¦ĪŖ·Ö×Ó¾§Ģ壻
£Ø2£©øł¾Ż¹¤ŅÕĮ÷³ĢæÉÖŖĀČ»ÆĀƵIJśĪļ£¬¾ĄäČ“”¢Éż»ŖæÉÖʱøĪŽĖ®AlCl3£¬ĖµĆ÷ĀČ»ÆĀƵIJśĪļÖŠŗ¬ÓŠA1C13£¬ĄäÄżĘ÷Ī²Ęųŗ¬ÓŠCO£¬ĖłŅŌAl2O3”¢Cl2ŗĶC·“Ó¦£¬Éś³ÉA1Cl3ŗĶCO£¬·“Ó¦·½³ĢŹ½ĪŖA12O3+3Cl2+3C 2A1Cl3+3CO
£Ø3£©Cl2ÓŠĒæŃõ»ÆŠŌ£¬½«SO32-Ńõ»ÆĪŖSO42-£¬×ŌÉķ±»»¹ŌĪŖC1-£®·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖSO32-+C12+H2O═SO42-+2C1-+2H+£»
£Ø4£©Éż»ŖĘ÷ÖŠÖ÷ŅŖŗ¬ÓŠAlCl3ŗĶFeCl3£¬Éż»ŖÖʱøĪŽĖ®AlCl3£¬Ó¦³żFeCl3Č„£®ĖłŅŌ¼ÓČėÉŁĮæAlÄæµÄŹĒ³żČ„FeCl3£¬
£Ø5£©²śĘ·ÖŠŗ¬ĀČ»ÆĀĮŗĶĀČ»ÆĢś£¬ČÜÓŚ¹żĮæµÄNaOHČÜŅŗ£¬¹żĀĖ³ö³ĮµķĪļ£¬³ĮµķĪļ¾Ļ“µÓ”¢×ĘÉÕ”¢ĄäČ“”¢³ĘÖŲ²ŠĮō¹ĢĢåÖŹĮæĪŖ0.32g£¬¼“Fe2O3ÖŹĮæĪŖ0.32g”£Ōņ²śĘ·ÖŠFeŌŖĖŲµÄŗ¬ĮæĪŖ£ŗ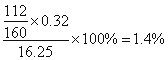
”¾Ė¼Ā·µć²¦”æ±¾Ģāæ¼²éĪļÖŹµÄŠŌÖŹ”¢»Æѧ¼ĘĖć£¬ŠčŅŖŌĖÓĆ·ÖĪö”¢±Č½Ļ”¢¹éÄɵȷ½·Ø¶ŌĖł»ńČ”µÄŠÅĻ¢½ųŠŠ³õ²½¼Ó¹¤ŗĶÓ¦ÓĆ£¬Ź¹ĪŹĢāµĆµ½½ā¾ö”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijӊ»śĪļµÄ½į¹¹¼ņŹ½ĪŖ °“¹ŁÄÜĶÅ·ÖĄą£¬Ėü²»ŹōÓŚ(””””)
°“¹ŁÄÜĶÅ·ÖĄą£¬Ėü²»ŹōÓŚ(””””)
A£®Ļ©ĢžĄą B£®·ÓĄą
C£®ĆŃĄą D£®“¼Ąą
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÄæĒ°”°µĶĢ¼¼õÅÅ”±±øŹÜ¹Ų×¢£¬CO2µÄ²śÉś¼°ÓŠŠ§æŖ·¢ĄūÓĆ³ÉĪŖæĘѧ¼ŅŃŠ¾æµÄÖŲŅŖæĪĢā”£
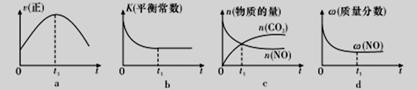
(1)Ęū³µĪ²Ęų¾»»ÆµÄÖ÷ŅŖŌĄķĪŖ2NO(g)+2CO(g)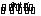 2CO2(g)+N2(g)”£ŌŚĆܱÕČŻĘ÷ÖŠ·¢ÉśøĆ·“Ó¦Ź±£¬c(CO2)ĖęĪĀ¶Č(T)”¢“߻ƼĮ±ķĆ껿(S)ŗĶŹ±¼ä(I)µÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾”£
2CO2(g)+N2(g)”£ŌŚĆܱÕČŻĘ÷ÖŠ·¢ÉśøĆ·“Ó¦Ź±£¬c(CO2)ĖęĪĀ¶Č(T)”¢“߻ƼĮ±ķĆ껿(S)ŗĶŹ±¼ä(I)µÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾”£
¾Ż“ĖÅŠ¶Ļ:
¢ŁøĆ·“Ó¦µÄ”÷H_____________0(Ģī”°>”±»ņ”°<”±)”£
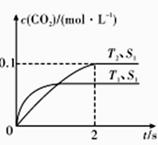
¢ŚŌŚT2ĪĀ¶ČĻĀ£¬0-2sÄŚµÄĘ½¾ł·“Ó¦ĖŁĀŹv(N2) =____________mol/(L·s)”£
¢Ūµ±¹ĢĢå“߻ƼĮµÄÖŹĮæŅ»¶ØŹ±£¬Ōö“óĘä±ķĆ껿æÉŌö“ó»Æѧ·“Ó¦ĖŁĀŹ”£Čō“߻ƼĮµÄ±ķĆ껿S1>S2,ŌŚ“šĢāæØĻąÓ¦Ķ¼ÖŠ»³öc(CO2)ŌŚT1”¢S2Ģõ¼žĻĀ“ļµ½Ę½ŗā¹ż³ĢÖŠµÄ±ä»ÆĒśĻß”£
¢ÜČōøĆ·“Ó¦ŌŚ¾ųČČ”¢ŗćČŻµÄĆܱÕĢåĻµÖŠ½ųŠŠ£¬ĻĀĮŠŹ¾ŅāĶ¼ÕżČ·ĒŅÄÜĖµĆ÷·“Ó¦ŌŚ½ųŠŠµ½t1Ź±æĢ“ļµ½Ę½ŗāדĢ¬µÄŹĒ_______________(Ģī“śŗÅ)”£
(2)Ö±½ÓÅÅ·ÅĆŗČ¼ÉÕ²śÉśµÄŃĢĘų»įŅżĘšŃĻÖŲµÄ»·¾³ĪŹĢā”£
¢ŁĆŗČ¼ÉÕ²śÉśµÄŃĢĘųŗ¬µŖµÄŃõ»ÆĪļ£¬ÓĆCH4“߻ƻ¹ŌNOxæÉŅŌĻū³żµŖŃõ»ÆĪļµÄĪŪČ¾”£
ĄżČē:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ”÷H=-867kJ/mol
2NO2(g)=N2O4(g) ”÷H=-867kJ/mol
Š“³öCH4(g)“߻ƻ¹ŌN2O4(g)Éś³ÉN2(g)”¢CO2(g)ŗĶH2O(g)µÄČČ»Æѧ·½³ĢŹ½:_____________________”£
¢Ś½«Č¼Ćŗ²śÉśµÄ¶žŃõ»ÆĢ¼»ŲŹÕĄūÓĆ£¬æÉ“ļµ½µĶĢ¼ÅŷŵÄÄæµÄ”£ČēĶ¼ŹĒĶعżČĖ¹¤¹āŗĻ×÷ÓĆ£¬ŅŌCO2(g)ŗĶH2O(g)ĪŖŌĮĻÖʱøHCOOHŗĶO2µÄŌĄķŹ¾ŅāĶ¼”£“߻ƼĮb±ķĆę·¢ÉśµÄµē¼«·“Ó¦ĪŖ_________________”£
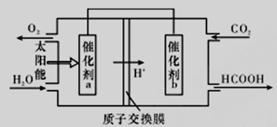
¢Ū³£ĪĀĻĀ0. 1 mol/LµÄHCOONaČÜŅŗpHĪŖ10£¬ŌņHCOOHµÄµēĄė³£ŹżKa =_______________mol·L-1(ĢīŠ“×īÖÕ¼ĘĖć½į¹ū)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¹¤ŅµŗĻ³É°±ÓėÖʱøĻõĖįŅ»°ćæÉĮ¬ŠųÉś²ś£¬Į÷³ĢČēĶ¼ĖłŹ¾£ŗ
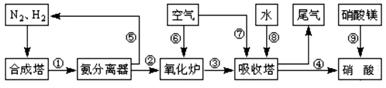
£Ø1£©¹¤ŅµÉś²śŹ±£¬ÖĘČ”ĒāĘųµÄŅ»øö·“Ó¦ĪŖ£ŗCO+H2O(g) CO2+H2
CO2+H2
T”ꏱ£¬Ķł1LĆܱÕČŻĘ÷ÖŠ³äČė0.2mol COŗĶ0.3molĖ®ÕōĘų”£·“Ó¦½ØĮ¢Ę½ŗāŗó£¬ĢåĻµÖŠc(H2)=0.12mol·L£1”£øĆĪĀ¶ČĻĀ“Ė·“Ó¦µÄĘ½ŗā³£ŹżK=_____£ØĢī¼ĘĖć½į¹ū£©”£
£Ø2£©ŗĻ³ÉĖžÖŠ·¢Éś·“Ó¦N2(g)+3H2(g) 2NH3(g)£»”÷H<0”£ĻĀ±ķĪŖ²»Ķ¬ĪĀ¶ČĻĀøĆ·“Ó¦µÄĘ½ŗā³£Źż”£ÓÉ“ĖæÉĶĘÖŖ£¬±ķÖŠT1____573K£ØĢī”°>”±”¢”°<”±»ņ”°=”±£©”£
2NH3(g)£»”÷H<0”£ĻĀ±ķĪŖ²»Ķ¬ĪĀ¶ČĻĀøĆ·“Ó¦µÄĘ½ŗā³£Źż”£ÓÉ“ĖæÉĶĘÖŖ£¬±ķÖŠT1____573K£ØĢī”°>”±”¢”°<”±»ņ”°=”±£©”£
| T/”ę | T1 | 300 | T2 |
| K | 1.00”Į107 | 2.45”Į105 | 1.88”Į103 |
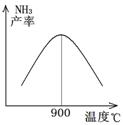
£Ø3£©N2ŗĶH2ŅŌĢś×÷“߻ƼĮ“Ó145”ę¾ĶæŖŹ¼·“Ó¦£¬²»Ķ¬ĪĀ¶ČĻĀNH3µÄ²śĀŹČēĶ¼ĖłŹ¾”£ĪĀ¶ČøßÓŚ900”ꏱ£¬NH3²śĀŹĻĀ½µµÄŌŅņŹĒ
£Ø4£©ĻõĖį³§µÄĪ²ĘųÖ±½ÓÅŷŽ«ĪŪČ¾æÕĘų£¬ÄæĒ°æĘѧ¼ŅĢ½Ė÷ĄūÓĆČ¼ĮĻĘųĢåÖŠµÄ¼×ĶéµČ½«µŖŃõ»ÆĪļ»¹ŌĪŖµŖĘųŗĶĖ®£¬Ęä·“Ó¦»śĄķĪŖ£ŗ
CH4(g)+4NO2=(g)£½4NO(g)+CO2(g)+2H2O(g)£» ”÷H=£574kJ·mol£1
CH4(g)+4NO(g)£½2N2(g)+CO2(g)+2H2O(g)£» ”÷H=£1160kJ·mol£1
Ōņ¼×ĶéÖ±½Ó½«NO2»¹ŌĪŖN2µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ
£Ø5£©°±ĘųŌŚ“æŃõÖŠČ¼ÉÕ£¬Éś³ÉŅ»ÖÖµ„ÖŹŗĶĖ®”£æĘѧ¼ŅĄūÓĆ“ĖŌĄķ£¬Éč¼Ę³É°±Ęų-ŃõĘųČ¼ĮĻµē³Ų£¬ŌņĶØČė°±ĘųµÄµē¼«¼īŠŌĢõ¼žĻĀ·¢Éś·“Ó¦µÄµē¼«·“Ó¦Ź½ĪŖ
ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
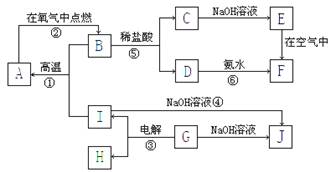
£®A”«I·Ö±š±ķŹ¾ÖŠŃ§»Æѧ֊³£¼ūµÄŅ»ÖÖĪļÖŹ£¬ĖüĆĒÖ®¼äĻą»„¹ŲĻµČēĻĀĶ¼ĖłŹ¾£Ø²æ·Ö·“Ó¦Īļ”¢Éś³ÉĪļƻӊĮŠ³ö£©£¬ĒŅŅŃÖŖGĪŖÖ÷×åŌŖĖŲµÄ¹ĢĢ¬Ńõ»ÆĪļ£¬A”¢B”¢C”¢D”¢E”¢FĮłÖÖĪļÖŹÖŠ¾łŗ¬Ķ¬Ņ»ÖÖŌŖĖŲ”£
ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ
£Ø1£©A”¢B”¢C”¢D”¢E”¢FĮłÖÖĪļÖŹÖŠĖłŗ¬Ķ¬Ņ»ÖÖŌŖĖŲŌŚÖÜĘŚ±ķÖŠĪ»ÖƵŚ ÖÜĘŚ”¢
µŚ ×å £»JµÄ»ÆѧĆū³ĘĪŖ ”£
£Ø2£©Š“³ö·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½ £»·“Ó¦¢ŽµÄĄė×Ó·½³ĢŹ½ ”£
£Ø3£©“ÓÄÜĮæ±ä»ÆµÄ½Ē¶Čæ“£¬¢Ł¢Ś¢Ū·“Ó¦ÖŠŹōÓŚ”÷H£¼0µÄ·“Ó¦ŹĒ ”£
 £Ø4£©Š“³ö·“Ó¦E F¹ż³ĢµÄĻÖĻó ,¼°·“Ó¦·½³ĢŹ½£ŗ ”£
£Ø4£©Š“³ö·“Ó¦E F¹ż³ĢµÄĻÖĻó ,¼°·“Ó¦·½³ĢŹ½£ŗ ”£
£Ø5£©ŌŚCČÜŅŗÖŠ¼ÓČėKSCNČÜŅŗ£¬ČÜŅŗ £ØĢī”°±ä”±»ņ”°²»±ä”±£©É«£¬Öš½„ĶØČėĀČĘųÖ±ÖĮ¹żĮ棬æÉÄܹŪ²ģµ½ĻÖĻóŹĒ ”£“ÓÕāŅ»æÉÄÜĻÖĻóÄÜµĆ³ö ½įĀŪ_____________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻņĆ÷·ÆČÜŅŗĄļµĪ¼ÓBa(OH)2ČÜŅŗ£¬µ±SO42-Ąė×ÓĒ”ŗĆ³ĮµķĶźČ«Ź±£¬ĀĮŌŖĖŲµÄ“ęŌŚŠĪŹ½ŹĒ
A£®Ņ»²æ·ÖĪŖAl(OH)3³Įµķ£¬Ņ»²æ·ÖŅŌAl3+“ęŌŚÓŚČÜŅŗÖŠ
B£®Ņ»²æ·ÖĪŖAl(OH)3³Įµķ£¬Ņ»²æ·ÖŅŌAlO2£ŠĪŹ½“ęŌŚÓŚČÜŅŗÖŠ
C£®Č«²æĪŖAl(OH)3³Įµķ
D£®¼øŗõČ«²æŅŌAlO2£ŠĪŹ½“ęŌŚÓŚČÜŅŗÖŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
A”¢B”¢C”¢D¾łĪŖ֊ѧ»Æѧ³£¼ūµÄ“æ¾»Īļ£¬AŹĒµ„ÖŹ”£ĖüĆĒÖ®¼äÓŠČēĻĀµÄ·“Ó¦¹ŲĻµ£ŗ
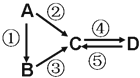
(1)ČōBŹĒĘųĢ¬Ēā»ÆĪļ£¬C”¢DŹĒŃõ»ÆĪļĒŅ»įŌģ³É¹ā»ÆѧŃĢĪķĪŪČ¾”£BÓėCŌŚŅ»¶ØĢõ¼žĻĀ·“Ӧɜ³ÉµÄAŹĒ“óĘųµÄÖ÷ŅŖ³É·Ö£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ______________________________”£
(2)ČōDĪļÖŹ¾ßÓŠĮ½ŠŌ£¬¢Ś”¢¢Ū·“Ó¦¾łŅŖÓĆĒæ¼īČÜŅŗ£¬¢Ü·“Ó¦ŹĒĶØČė¹żĮæµÄŅ»ÖÖŅżĘšĪĀŹŅŠ§Ó¦µÄÖ÷ŅŖĘųĢ唣Ŋ¶Ļµ„ÖŹAµÄŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆ£ŗ__________________”£
(3)ČōAŹĒĢ«ŃōÄܵē³ŲÓĆµÄ¹ā·ü²ÄĮĻ”£C”¢DĪŖÄĘŃĪ£¬Į½ÖÖĪļÖŹÖŠÄĘ”¢ŃõĶāµÄŌŖĖŲĪŖĶ¬Ņ»Ö÷×壬ĒŅČÜŅŗ¾łĻŌ¼īŠŌ”£Š“³ö¢Ś·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ__________________________________”£
(4)ČōAŹĒÓ¦ÓĆ×ī¹ć·ŗµÄ½šŹō”£¢Ü·“Ó¦ÓƵ½A£¬¢Ś”¢¢Ż·“Ó¦¾łÓƵ½Ķ¬Ņ»ÖÖ·Ē½šŹōµ„ÖŹ”£CµÄČÜŅŗÓĆÓŚŹ“æĢÓ”Ė¢ĶµēĀ·°å£¬Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ__________________________”£
(5)ČōAĪŖµ»ĘÉ«¹ĢĢ壬C”¢DŹĒŃõ»ÆĪļ£¬ĒŅCŹĒŌģ³ÉĖįÓźµÄÖ÷ŅŖĪļÖŹ£® BÓėCæÉ·“Ӧɜ³ÉA”£ĒėŠ“³öBµÄµē×ÓŹ½______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ·“Ó¦ĖłµĆČÜŅŗÖŠŅ»¶ØÖ»ŗ¬Ņ»ÖÖČÜÖŹµÄŹĒ £Ø £©
A£®ĻņMgSO4”¢H2SO4µÄ»ģŗĻŅŗÖŠ¼ÓČė¹żĮæµÄBa(OH)2ČÜŅŗ B£®ĻņĻ”ĻõĖįÖŠ¼ÓČėĢś·Ū
C£®ĻņĻ”ŃĪĖįÖŠµĪČėÉŁĮæµÄNaAlO2ČÜŅŗ D£®ĻņNaOHČÜŅŗÖŠĶØČėCO2ĘųĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
µŖŌŖĖŲµÄ»ÆŗĻĪļÓ¦ÓĆŹ®·Ö¹ć·ŗ”£Ēė»Ų“š£ŗ
£Ø1£©»š¼żČ¼ĮĻŅŗĢ¬Ę«¶ž¼×ėĀ£ØC2H8N2£©ŹĒÓĆŅŗĢ¬N2O4×÷Ńõ»Æ¼Į£¬¶žÕß·“Ó¦·Å³ö“óĮæµÄČČ£¬Éś³ÉĪŽ¶¾”¢ĪŽĪŪČ¾µÄĘųĢåŗĶĖ®”£ŅŃÖŖŹŅĪĀĻĀ£¬1 gČ¼ĮĻĶźČ«Č¼ÉÕŹĶ·Å³öµÄÄÜĮæĪŖ42.5kJ£¬ŌņøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ ”£

£Ø2£©298 KŹ±£¬ŌŚ2L¹Ģ¶ØĢå»żµÄĆܱÕČŻĘ÷ÖŠ£¬·¢ÉśæÉÄę·“Ó¦£ŗ2NO2(g) N2O4(g) ¦¤H£½-a kJ/mol (a>0) ”£N2O4µÄĪļÖŹµÄĮæÅضČĖꏱ¼ä±ä»ÆČēĶ¼”£“ļĘ½ŗāŹ±£¬N2O4µÄÅضČĪŖNO2µÄ2±¶£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
N2O4(g) ¦¤H£½-a kJ/mol (a>0) ”£N2O4µÄĪļÖŹµÄĮæÅضČĖꏱ¼ä±ä»ÆČēĶ¼”£“ļĘ½ŗāŹ±£¬N2O4µÄÅضČĪŖNO2µÄ2±¶£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
¢Ł298kŹ±£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ L”¤mol£1£Ø¾«Č·µ½0.01£©”£
¢ŚĻĀĮŠĒéæö²»ŹĒ“¦ÓŚĘ½ŗāדĢ¬µÄŹĒ £ŗ
A.»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä£» B.»ģŗĻĘųĢåµÄŃÕÉ«²»ŌŁ±ä»Æ£» C.ĘųŃ¹ŗć¶ØŹ±
¢ŪČō·“Ó¦ŌŚ398K½ųŠŠ£¬Ä³Ź±æĢ²āµĆn(NO2)=0.6 moln(N2O4)=1.2mol£¬Ōņ“ĖŹ±V£ØÕż£© V£ØÄę£©£ØĢī ”°>”±”¢”°<”±»ņ”°=”±£©”£
£Ø3£©NH4HSO4ŌŚ·ÖĪöŹŌ¼Į”¢Ņ½Ņ©”¢µē×Ó¹¤ŅµÖŠÓĆĶ¾¹ć·ŗ”£ĻÖĻņ100 mL 0.1 mol”¤L£1NH4HSO4ČÜŅŗÖŠµĪ¼Ó0.1 mol”¤L£1NaOHČÜŅŗ£¬µĆµ½µÄČÜŅŗpHÓėNaOHČÜŅŗĢå»żµÄ¹ŲĻµĒśĻßČēĶ¼ĖłŹ¾”£ŹŌ·ÖĪöĶ¼ÖŠa”¢b”¢c”¢d”¢eĪåøöµć”£
¢ŁbµćŹ±£¬ČÜŅŗÖŠ·¢ÉśĖ®½ā·“Ó¦µÄĄė×ÓŹĒ______£»
¢ŚŌŚcµć£¬ČÜŅŗÖŠø÷Ąė×ÓÅضČÓɓ󵽊”µÄÅÅĮŠĖ³Šņ ”£
¢Ūd”¢eµć¶ŌÓ¦ČÜŅŗÖŠ£¬Ė®µēĄė³Ģ¶Č“󊔹ŲĻµŹĒd e£ØĢī”°>”±”¢”°<”±»ņ”°=”±£©”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com