
【题目】一定条件下,对于可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始浓度分别为c 1、c 2、c 3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1mol·L -1、0.3mol·L -1、0.08mol·L -1,则下列判断不正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c 1、c 2、c 3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1mol·L -1、0.3mol·L -1、0.08mol·L -1,则下列判断不正确的是( )
A.c 1:c 2=1:3
B.平衡时,Y和Z的生成速率之比为2:3
C.X、Y的转化率相等
D.c 1的取值范围为0mol·L -1<c 1<0.14mol·L -1
【答案】B
【解析】
试题分析:A.设X转化的浓度为x,则
X(g)+3Y(g)![]() 2Z(g)
2Z(g)
初始浓度(mol/L) c1 c2 c3
转化浓度(mol/L) x 3x 2x
平衡浓度(mol/L) 0.1 0.3 0.08
则:c1:c2=(x+0.1moL/L):(3x+0.3mol/L)=1:3,A正确;B.平衡时,正逆反应速率相等,则Y和Z的生成速率之比为3:2,B错误;C.反应前后X、Y气体的浓度比等于反应系数之比,所以达到平衡状态时,转化率相同,C正确;D.反应为可逆反应,物质不可能完全转化,如反应向正反应分析进行,则0<c1,如反应向逆反应分析进行,则c1<0.14molL-1,有0 mol·L-1<c1<0.14molL-1,D正确;答案选B。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】
(1)下列有关容量瓶的使用方法的操作中,错误的是
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.定容时,将蒸馏水小心倒入容量瓶中到刻度线齐平处
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中定容
E.盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶反复上下颠倒、摇匀。
(2)实验室中需2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是_____________。
A.1000ml;212g B.950ml;543.4g
C.任意规格;572g D.500ml;106g
(3)现用98%、密度为1.8mol/L的浓硫酸配制500mL的稀硫酸。请回答下列问题:
①配制稀硫酸时,需要的玻璃仪器有玻璃棒、烧杯、量筒,还缺少的玻璃仪器有_________(填写仪器名称)。
②经计算,配制500mL0.2mol/L的稀硫酸需要上述浓硫酸的体积为___________。
③稀浓硫酸时,实验操作步骤:________________。
(4)误差分析:①用量筒量取浓硫酸时,仰视读数导致最终结果_____________;(填“偏大”“偏小”或“不变”)
②定容时仰视读数,导致最终结果_______________;(填“偏大”“偏小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
___________+___________→___________+___________+___________+H2O
反应物中发生氧化反应的物质是__________,被还原的元素是___________。
反应中1mol氧化剂__________(填“得到”或“失去”)_________mol电子。
II、图中所示工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品中的NaCl的质量分数。
![]()
①如何检验氯化钡溶液已过量______________;
检验沉淀是否洗涤干净所用到的试剂是__________;样品中NaCl的质量分数的数学表达式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.强电解质都易溶于水,所以BaSO4是弱电解质
B.一定条件下醋酸溶液的导电能力可能比稀硫酸强
C.SO2的水溶液能导电,所以SO2是电解质
D.金刚石不导电,因此金刚石是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若要使0.5mol甲烷和Cl2发生取代反应,反应后CH4与Cl2均无剩余,并生成的四种取代产物的物质的量依次增加0.05mol,则需要Cl2的物质的量为( )
A.1.75mol B.2mol C.1.25mol D.1.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) ![]() Pb(s)+Sn 2+(aq),体系中c(Pb2+)和c(Sn 2+)变化关系如图所示。
Pb(s)+Sn 2+(aq),体系中c(Pb2+)和c(Sn 2+)变化关系如图所示。
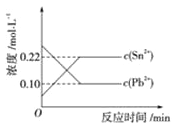
下列判断正确的是( )
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO3)2 固体后,c(Pb2+)变小
C.25 ℃时,该反应的平衡常数K=2.2
D.升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 下列表示乙炔(化学式为C2H2)燃烧热的热化学方程式的是( )
A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g) △H=akJ/mol
B.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l) △H=bkJ/mol
C.C2H2(g)+3/2O2(g)=2CO(g)+H2O(g) △H=ckJ/mol
D.C2H2(g)+3/2O2(g)=2CO(g)+H2O(g) △H=ckJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开学前某同学去实验室打扫卫生发现,放假前做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,几位同学提出了自己的假设并展开了探究活动。

【猜想与假设】小松同学猜想:该溶液没有变质;小雷同学猜想:该溶液已变质
【表达与交流】小雷同学猜想的理由是(1)_____________________。
【实验验证】小松同学为了验正自己的猜想,取一定量试剂瓶中的液体于试管中,加入了少量的无色酚酞溶液,观察到溶液变成红色,于是认为自己的猪想正确。请对小松同学的结论做出评价(2)_______________。
小雷同学验证自己的猜想,取少量试剂瓶中的液体于试管中,加入了足量的稀盐酸,观察到溶液中有气泡产生,证实了溶液己经变质的猜想,写出有气泡产生的反应的化学方程式(3)_________________。
【验证与结论】小林同学和小文同学对已经变质的氢氧化钠溶液做了进一步探究,两位同学为了节约药品,将小松同学实验后的红色溶液平均分成两份于两只试管中,小林同学向其中一只试管中逐滴加入氢氧化钙溶液,观察到有白色沉淀生成,继续滴加至刚好不再产生沉淀时,发现溶液仍为红色,小林同学得出了该瓶溶液为部分变质的结论。请对小林同学的结论做出评价(4)______________________。
【反思与结论】小文同学向另一支试管中加入过量的一种溶液,观察到白色沉淀且溶液由红色变成了无色,准确证实了该瓶溶液已全部变质。请写出一种符合小文同学所加溶液的溶质的化学式(5)________。通过上述实验得出结论:在检验溶液中组成的实验操作中应注意的问题是(6)_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜与稀硝酸反应的化学方程式为:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O现将9.60g的铜单质加入到过量的8.40%的稀硝酸中,充分反应后,试求:
(1)标准状况下生成NO多少L?
(2)这些铜单质能与多少g上述稀硝酸恰好完全反应?
(3)反应中有多少molHNO3被还原?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com