
ĻĀĶ¼ĪŖ×°ÓŠ»īČū£ØÖŹĮæŗöĀŌ²»¼Ę£©µÄĆܱÕČŻĘ÷£¬ÄŚŹ¢22£®4mLŅ»Ńõ»ÆµŖ£¬ČōĶØČė11£®2mLŃõĘų(ĘųĢåĢå»ż¾łŌŚ±ź×¼×“æöĻĀ²ā¶Ø)£¬±£³ÖĪĀ¶ČŃ¹Ēæ²»±ä£¬ŌņČŻĘ÷ÄŚµÄĆܶČĪŖ£ØĢįŹ¾£ŗ²»æ¼ĀĒNO×Ŗ»ÆĪŖNO2µÄæÉÄęŠŌ£©
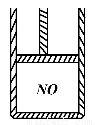
A£® µČÓŚ1£®369 g”¤L-1
B£® µČÓŚ2£®054 g”¤L-1
C£® ŌŚ1£®369g”¤L-1ŗĶ2£®054g”¤L-1Ö®¼ä
D£® ŌŚ2£®054g”¤L-1ŗĶ4£®108g”¤L-1Ö®¼ä
D
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗNOÓėŃõĘųĒ”ŗĆ·ūŗĻĪļÖŹµÄĮæÖ®±ČŹĒ2:1µÄ¹ŲĻµ£¬ĖłŅŌ¶žÕßĒ”ŗĆĶźČ«·“Ӧɜ³ÉNO2£¬ČōČ«²æŹĒ¶žŃõ»ÆµŖ£¬ŌņŗćŃ¹ĻĀĘųĢåµÄĆÜ¶Č¼“ĪŖ¶žŃõ»ÆµŖŌŚ±ź×¼×“æöĻĀµÄĆܶČ46g/22£®4L=2£®054g/L£¬µ«¶žŃõ»ÆµŖ“ęŌŚ
ČēĻĀĘ½ŗā2NO2 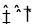 N2O4 £¬Čō¶žŃõ»ÆµŖČ«²æ×Ŗ»ÆĪŖN2O4£¬ŗćŃ¹ĻĀĘųĢåµÄĆܶȏĒN2O4µÄĆܶČĪŖ92g/22£®4L=4£®108g/L£¬¶ųŹµ¼ŹµÄĘųĢåµÄĆܶČÓ¦½éÓŚ¶žÕßÖ®¼ä£¬ĖłŅŌ“š°øŃ”D”£
N2O4 £¬Čō¶žŃõ»ÆµŖČ«²æ×Ŗ»ÆĪŖN2O4£¬ŗćŃ¹ĻĀĘųĢåµÄĆܶȏĒN2O4µÄĆܶČĪŖ92g/22£®4L=4£®108g/L£¬¶ųŹµ¼ŹµÄĘųĢåµÄĆܶČÓ¦½éÓŚ¶žÕßÖ®¼ä£¬ĖłŅŌ“š°øŃ”D”£
æ¼µć£ŗæ¼²é»ģŗĻĘųĢåĆܶȵÄÅŠ¶Ļ£¬¼«¶Ė¼ŁÉč·ØµÄÓ¦ÓĆ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ĖÄ“ØŹ”ŅĖ²żŹŠ“ŗ¼¾ĘŚÖŠæ¼ŹŌø߶ž»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø14·Ö£©£Ø1£©³£ĪĀŹ±£¬½«ÅضČĪŖm mol”¤ L-1µÄCH3COOHČÜŅŗŗĶn mol”¤L-1NaOHČÜŅŗµČĢå»ż»ģŗĻ£¬»ģŗĻŗóČÜŅŗµÄpH£½7£¬mÓėnµÄ“󊔹ŲĻµŹĒm n£ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£¬ĻĀĶ¬£©£»Čō½«PH=2µÄCH3COOHČÜŅŗŗĶPH=12µÄNaOHČÜŅŗµČĢå»ż»ģŗĻ£¬»ģŗĻČÜŅŗµÄPH 7
£Ø2£©Ļū·ĄÓƵÄÅŻÄĆš»šĘ÷ČװµÄŅ©Ę·ŹĒĮņĖįĀĮČÜŅŗŗĶĢ¼ĖįĒāÄĘČÜŅŗ£¬ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾¶žÕß»ģŗĻŹ±·¢ÉśµÄ·“Ó¦
£Ø3£©³£ĪĀĻĀijĒæĖįČÜŅŗpH=a£¬Ēæ¼īČÜŅŗpH=b£¬ŅŃÖŖa£«b£½12£¬Ėį¼īČÜŅŗ»ģŗĻpH=7£¬ŌņĖįČÜŅŗĢå»żV1ŗĶ¼īČÜŅŗĢå»żV2µÄ¹ŲĻµĪŖ
£Ø4£©³£ĪĀŹ±KSP[Cu(OH)2]= 2.2”Į10£20,½«Cu(OH)2ČÜÓŚ2.2mol/LCuCl2ČÜŅŗÖŠŠĪ³ÉĘ½ŗā£¬ČܽāĘ½ŗā·½³ĢŹ½ĪŖ £¬ČÜŅŗµÄPHĪŖ
£Ø5£©ĪļÖŹµÄĮæÅضČĻąĶ¬µÄĻĀĮŠČÜŅŗ¢Ł(NH4)2CO3 ¢Ś(NH4)2SO4 ¢ŪNH4HCO3 ¢ÜNH4HSO4 ¢ŻNH4Cl
¢ŽNH3”¤H2O”£c(NH4+)ÓÉŠ”µ½“óµÄÅÅĮŠĖ³ŠņŹĒ £ØĢīŠņŗÅ£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¼ŖĮÖŹ”³¤“ŗŹŠø߶žĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚ25?CŹ±£¬½«Į½øł²¬µē¼«²åČėŅ»¶ØĮæµÄĮņĖįÄʱ„ŗĶČÜŅŗÖŠ½ųŠŠµē½ā£¬µ±µēĀ·ÖŠÓŠa molµē×Ó×ŖŅĘŹ±£¬ČÜŅŗÖŠĪö³ömg Na2SO4 ”¤10 H2 O¾§Ģ唣ČōĪĀ¶Č²»±ä£¬ŌŚŹ£ÓąČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹżĪŖ
A£®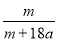 ”Į100% B£®
”Į100% B£®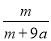 ”Į100%
”Į100%
C£® 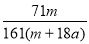 ”Į100% D£®71m/161(m+9a) ”Į100%
”Į100% D£®71m/161(m+9a) ”Į100%
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¼ŖĮÖŹ”³¤“ŗŹŠø߶žĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚ³£ĪĀĻĀĖÄøöČŻ»żĻąĶ¬µÄ³éæÕµÄĆܱÕČŻĘ÷ÄŚ£¬·Ö±š×¢ČėĻĀĮŠø÷×éĘųĢå(ĻČ×¢ČėŅ»ÖÖ£¬ŌŁ×¢ČėĮķŅ»ÖÖ)£¬Č«²æĘųĢå×¢ČėĶź±Ļŗó£¬ČŻĘ÷ÖŠµÄŃ¹Ēæ“ӓ󵽊”µÄĖ³ŠņŹĒ
¢Ł2molĒāĘųŗĶ1molŃõĘų ¢Ś2molĮņ»ÆĒāŗĶ1mol¶žŃõ»ÆĮņ
¢Ū2molŅ»Ńõ»ÆµŖŗĶ1molŃõĘų ¢Ü2mol°±ŗĶlmolĀČ»ÆĒā
A£®¢Ł=¢Ś=¢Ū>¢Ü B£®¢Ł>¢Ś=¢Ū>¢Ü C£®¢Ū>¢Ü>¢Ł>¢Ś D£®¢Ł>¢Ū>¢Ü>¢Ś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¼ŖĮÖŹ”³¤“ŗŹŠøßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø¹²10·Ö£©ĻÖÓŠŃōĄė×Ó½»»»Ä¤”¢ŅõĄė×Ó½»»»Ä¤”¢ŹÆÄ«µē¼«£¬ĒėÓĆĀČ¼ī¹¤ŅµÖŠµÄĤ¼¼ŹõŌĄķ£¬»Ų“šĻĀĮŠĪŹĢā”£
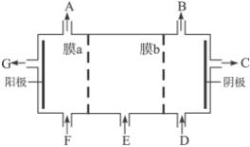
£Ø1£©Š“³öĀČ¼ī¹¤ŅµÖŠµē½ā±„ŗĶŹ³ŃĪĖ®µÄĄė×Ó·½³ĢŹ½ £»
£Ø2£©ĒėĄūÓĆ½»»»Ä¤¼¼Źõ£¬øł¾ŻÉĻĶ¼æņ¼Ü£¬Éč¼ĘŅ»øöµē½āĮņĖįÄĘČÜŅŗÖĘĒāŃõ»ÆÄĘČÜŅŗŗĶĮņĖįČÜŅŗµÄ×°ÖĆ£¬±ź³ö½ų³öĪļÖŹµÄ»ÆѧŹ½£ŗ
A_________£»C_________£» E_________£»Ä¤bĪŖ Ąė×Ó½»»»Ä¤£ØĢī”°Ńō”±»ņ”°Ņõ”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¼ŖĮÖŹ”³¤“ŗŹŠøßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ×°ÖƵÄĻßĀ·½ÓĶØŗó,¾¹żŅ»¶ĪŹ±¼ä,ČÜŅŗµÄpHÖµĆ÷ĻŌĻĀ½µµÄŹĒ
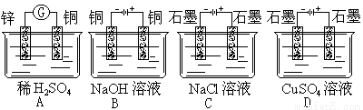
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¼ŖĮÖŹ”³¤“ŗŹŠøßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻņĻõĖįÄĘČÜŅŗÖŠ¼ÓČėĶ·Ū²»·¢Éś·“Ó¦£¬ČōŌŁ¼ÓČė£Ø»ņĶØČė£©Ä³ÖÖĪļÖŹ£¬ŌņĶ·ŪæÉŅŌÖš½„Čܽā£¬²»·ūŗĻ“ĖĢõ¼žµÄĪļÖŹŹĒ
A£®Fe(NO3)3 B£® HCl C£® NaHSO4 D£® NaHCO3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¼ŖĮÖŹ”°×³ĒŹŠø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»Æѧ£ØB¾ķ£©ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ņ»¶ØĢõ¼žĻĀ£¬æÉÄę·“Ó¦£ŗX(g) + 3Y(g) 2Z(g),ČōX”¢Y”¢ZµÄĘšŹ¼ÅØ¶Č·Ö±šĪŖc1”¢c2”¢c3£Ø¾ł²»ĪŖĮć£©,·“Ó¦“ļµ½Ę½ŗāŹ±, X”¢Y”¢ZµÄÅØ¶Č·Ö±šĪŖ0.1mol?L-1”¢0.3 mol?L-1”¢0.08 mol?L-1£¬ ŌņĻĀĮŠÅŠ¶Ļ²»ÕżČ·µÄŹĒ £Ø £©
2Z(g),ČōX”¢Y”¢ZµÄĘšŹ¼ÅØ¶Č·Ö±šĪŖc1”¢c2”¢c3£Ø¾ł²»ĪŖĮć£©,·“Ó¦“ļµ½Ę½ŗāŹ±, X”¢Y”¢ZµÄÅØ¶Č·Ö±šĪŖ0.1mol?L-1”¢0.3 mol?L-1”¢0.08 mol?L-1£¬ ŌņĻĀĮŠÅŠ¶Ļ²»ÕżČ·µÄŹĒ £Ø £©
A£®c1”Ćc2== 1”Ć3 B£®Ę½ŗāŹ±£¬YŗĶZÉś³ÉĖŁĀŹÖ®±ČĪŖ3”Ć2
C£®X”¢YµÄ×Ŗ»ÆĀŹ²»ĻąµČ D£®c1µÄȔֵ·¶Ī§ĪŖ0< c1< 0.14 mol?L-1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¼ŖĮÖŹ”°×³ĒŹŠø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£ØA¾ķ£©£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®²ŻĖįĒā¼ŲČÜŅŗ³ŹĖįŠŌ£¬ŌŚ0.1mol”¤L£1KHC2O4ČÜŅŗÖŠ£ŗc£ØC2O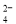 £©>c£ØH2C2O4£©
£©>c£ØH2C2O4£©
B£®ŌŚŠ”ĖÕ“ņĖ®ČÜŅŗÖŠ£ŗc£ØNa+£©+c£ØH+£©=c£ØHCO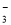 £©+c£ØCO
£©+c£ØCO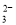 £©+c£ØOH££©
£©+c£ØOH££©
C£®ĻąĶ¬ĪĀ¶ČĻĀ£¬1 mol/L°±Ė®ČÜŅŗÓė0.5mol/L°±Ė®ČÜŅŗÖŠ£¬c£ØOH££©Ö®±ČŹĒ2:1
D£®µ±°±Ė®ÓėŃĪĖįĒ”ŗĆĶźČ«·“Ó¦Ź±£¬c£ØNH £©>c£ØCl?£©>c£ØH+£©>c£ØOH?£©
£©>c£ØCl?£©>c£ØH+£©>c£ØOH?£©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com