
| A. | 往原溶液中加100mL水 | B. | 再加100mL原溶液 | ||
| C. | 将原溶液稀释为200mL | D. | 加入等浓度等体积的硫酸 |
分析 A、往原溶液中加100mL水,溶液的体积不是200ml;
B、再加100mL原溶液,溶液的浓度不变;
C、将原溶液稀释为200mL,溶液中溶质的物质的量不变,体积为原来体积的2倍;
D、加入等浓度等体积的硫酸,两者恰好完全反应.
解答 解:A、往原溶液中加100mL水,溶液的体积不是200ml,所以物质的量浓度不是原来的一半,故A错误;
B、再加100mL原溶液,溶液的浓度不变,不符合题意,故B错误;
C、将原溶液稀释为200mL,溶液中溶质的物质的量不变,体积为原来体积的2倍,所以物质的量浓度为原来的一半,故C正确;
D、加入等浓度等体积的硫酸,两者恰好完全反应,氢氧化钡的物质的量为0,所以反应后氢氧化钡的物质的量浓度为0,故D错误;
故选C.
点评 本题考查物质的量浓度的计算,题目难度不大,明确溶液稀释过程中溶质的物质的量不变为解答关键,注意掌握物质的量浓度的概念及表达式,试题培养了学生的灵活应用能力.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:解答题
| 金属 | 电子流动方向 | 电压/V |
| Fe | Fe→Cu | +0.78 |
| Zn | Zn→Cu | +1.10 |
| A | Cu→A | -0.15 |
| B | B→Cu | +0.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验操作 | 实验现象 | 解释与结论 |
| A | 将乙醇与浓硫酸共热至l70℃,所得气体通入酸性KMnO4溶液中 | 酸性KMnO4溶液褪色 | 乙醇发生消去反应,气体中只含有乙烯 |
| B | 淀粉溶液和稀H2SO4混合加热,加新制Cu(OH)2悬浊液加热至沸腾 | 有砖红色沉淀产生 | 淀粉发生水解,产物有还原性 |
| C | 向甲苯中滴入适量浓溴水,振荡,静置 | 溶液上层呈橙红色, 下层几乎无色 | 甲苯和溴发生取代反应,使溴水褪色 |
| D | 在洁净的试管中加入2%硝酸银溶液1mL,逐滴加入2%稀氨水至沉淀恰好溶解为止,再滴加几滴乙醛,振荡后,放入热水浴中加热 | 试管壁出现光亮的银镜 | 乙醛发生了氧化反应,乙醛有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
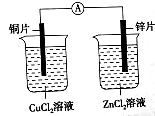 某实验小组拟用铜片、锌片、CuCl2溶液、ZnCl2溶液等设计原电池.并将装置图画到了如图所示程度.
某实验小组拟用铜片、锌片、CuCl2溶液、ZnCl2溶液等设计原电池.并将装置图画到了如图所示程度.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鼓励使用液化石油气做燃料 | B. | 鼓励使用太阳能、风能等能源 | ||
| C. | 鼓励煤火力发电,少用水力发电 | D. | 鼓励用私家车,少坐公交车出行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仅①③ | B. | 仅②③ | C. | 仅①② | D. | 仅③ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钙、铁、锌、硒都是人体必需的微量元素 | |
| B. | 发现煤气泄漏应立即关闭阀门,开窗通风 | |
| C. | 用肥皂水可鉴别硬水和软水 | |
| D. | 氢能源的大量应用需解决制取成本高、贮存困难等问题 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com