
����Ŀ�����������£��赥�ʺ�HCl��Ӧ����SiHCl3�Ǵֹ��ᴿ����Ҫ���裮ijС�������ͼ��ʾװ���������ת�����г�װ����ȥ���� 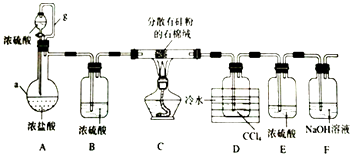
��֪��SiHCl3�ķе�Ϊ33.0��C���������л��ܼ�������ˮ���ҷ�Ӧ���ڿ������ױ�������CCl4�ķе�Ϊ76.8��C��
��ش�
��1������a������������g��������
��2��װ��A�У�Ũ�������ֵ�����Ϊ��ʵ��ʱ�����ȴ�Һ©��������һ��ʱ����ڵ�ȼC���ƾ��ƣ���������
��3��װ��C�з�����Ӧ�Ļ�ѧ����ʽΪ��
��4��װ��D�����õ�Һ̬�����ķ��뷽��Ϊ �� ����������ƣ�
��5����Ӧ�������ͨ��װ��F�е�NaOH��Һ���ݳ�����Ĵ�������Ϊ��
��6��SiHCl3�ڳ�ʪ�Ŀ����б�����������һ���������һ�������ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪ
���𰸡�
��1��������ƿ��ƽ��ѹǿ��ʹŨ�������μӣ������������𰸣�
��2����ˮ�ԣ��ž�װ���еĿ���������SiHCl3������е�ˮ������Ӧ�ͱ�O2����
��3��Si+3HCl ![]() SiHCl3+H2
SiHCl3+H2
��4������
��5����ȼ���������ռ���
��6��2SiHCl3+O2+2H2O�T2SiO2+6HCl
���������⣺��1������a�Ǿ���֧�ܵ���ƿ��Ϊ������ƿ��װ��A�е�b������Ϊ��ƽ��ѹǿ�����ã�ʹ��Һ©���е�Һ��Ũ����˳�����£�
�ʴ�Ϊ��������ƿ��ƽ��ѹǿ��ʹŨ�������μӣ������������𰸣�����2��װ��A��������ƿ��ʢ��Ũ���ᣬ��Һ©����ʢ��Ũ���ᣬ����Ũ�������ˮ���Լ��Ȼ���Ļӷ��ԣ���Һ©����������A���ų��Ȼ������壬SiHCl3�ķе�Ϊ33.0��C���������л��ܼ�������ˮ���ҷ�Ӧ���ڿ������ױ�������ʵ��ʱ�����ȴ�Һ©��������һ��ʱ����ڵ�ȼC���ƾ��ƣ��ž�װ���еĿ���������SiHCl3������е�ˮ������Ӧ�ͱ�O2������
�ʴ�Ϊ����ˮ�ԣ� �ž�װ���еĿ���������SiHCl3������е�ˮ������Ӧ�ͱ�O2��������3�����������Ϣ���赥�ʺ�HCl��Ӧ����SiHCl3��֪������Ȼ��ⷴӦ�ķ���ʽΪ��Si+3HCl ![]() SiHCl3+H2 ��
SiHCl3+H2 ��
�ʴ�Ϊ��Si+3HCl ![]() SiHCl3+H2����4��SiHCl3�ķе�Ϊ33.0��C���������л��ܼ����Ƴ���SiHCl3���ܲ������ᴿSiHCl3�ķ�����������е�ϵͣ�ͨ������ķ�������õ�������SiHCl3 ��
SiHCl3+H2����4��SiHCl3�ķе�Ϊ33.0��C���������л��ܼ����Ƴ���SiHCl3���ܲ������ᴿSiHCl3�ķ�����������е�ϵͣ�ͨ������ķ�������õ�������SiHCl3 ��
�ʴ�Ϊ������5���赥�ʺ�HCl��ӦSi+3HCl ![]() SiHCl3+H2 �� �ֹ������HCl���巴Ӧ�Ƶ�SiHCl3��Si+3HCl
SiHCl3+H2 �� �ֹ������HCl���巴Ӧ�Ƶ�SiHCl3��Si+3HCl ![]() SiHCl3+H2��װ��F�е�����������Ϊ�����չ������Ȼ��⣬ͨ��װ��F��ʣ������Ϊ����������ȼ������ˮ����ͨ����ȼ�������ռ�������
SiHCl3+H2��װ��F�е�����������Ϊ�����չ������Ȼ��⣬ͨ��װ��F��ʣ������Ϊ����������ȼ������ˮ����ͨ����ȼ�������ռ�������
�ʴ�Ϊ����ȼ���������ռ�������6������ȶ�������Ϊ�������裬SiHCl3�ڳ�ʪ�Ŀ����б�����������һ��������Ϊ�������裬����ԭ���غ��֪һ��������Ϊ�Ȼ��⣬���Ը÷�Ӧ�Ļ�ѧ����ʽΪ��2SiHCl3+O2+2H2O�T2SiO2+6HCl��
�ʴ�Ϊ��2SiHCl3+O2+2H2O�T2SiO2+6HCl��
�ֹ��ᴿ��װ��A��������ƿ��ʢ��Ũ���ᣬ��Һ©����ʢ��Ũ���ᣬ����Ũ�������ˮ���Լ��Ȼ���Ļӷ��ԣ���Һ©����������A���ų��Ȼ������壬�ž�װ���еĿ�����װ��B�����Ȼ���������и��װ��C���ֹ������HCl���巴Ӧ�Ƶ�SiHCl3��Si+3HCl ![]() SiHCl3+H2��װ��F�е�����������Ϊ�����չ������Ȼ��⣬װ��E��ֹF�е�ˮ��������װ��D��SiHCl3������Ӧ��װ��D�ռ�SiHCl3 �� ͨ��װ��F��ʣ������Ϊ��������ͨ����ȼ�������ռ������� ��1����������a�������Լ��������������ƽ��װ��A�е�b������Ϊ��ƽ��ѹǿ�����ã���2��Ũ���������ˮ�ԣ��Ȼ����ӷ���SiHCl3����ˮ���ҷ�Ӧ���ڿ������ױ���������3������Ȼ����ڼ��ȵ������·�Ӧ���ɺ����ȹ������������4���õ��IJ���е㲻ͬ�����Կ��Ʒе�ͨ������ķ����õ�SiHCl3����5����Ӧ�������Ϊ�������������пɿ�ȼ�ԣ���ͨ��ȼ�ջ������ռ��ķ�������β������6��SiHCl3�ڳ�ʪ�Ŀ����б�����������һ��������Ϊ�������裬һ�����������ԭ���غ��֪Ϊ�Ȼ��⣮
SiHCl3+H2��װ��F�е�����������Ϊ�����չ������Ȼ��⣬װ��E��ֹF�е�ˮ��������װ��D��SiHCl3������Ӧ��װ��D�ռ�SiHCl3 �� ͨ��װ��F��ʣ������Ϊ��������ͨ����ȼ�������ռ������� ��1����������a�������Լ��������������ƽ��װ��A�е�b������Ϊ��ƽ��ѹǿ�����ã���2��Ũ���������ˮ�ԣ��Ȼ����ӷ���SiHCl3����ˮ���ҷ�Ӧ���ڿ������ױ���������3������Ȼ����ڼ��ȵ������·�Ӧ���ɺ����ȹ������������4���õ��IJ���е㲻ͬ�����Կ��Ʒе�ͨ������ķ����õ�SiHCl3����5����Ӧ�������Ϊ�������������пɿ�ȼ�ԣ���ͨ��ȼ�ջ������ռ��ķ�������β������6��SiHCl3�ڳ�ʪ�Ŀ����б�����������һ��������Ϊ�������裬һ�����������ԭ���غ��֪Ϊ�Ȼ��⣮


 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д� ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����25 ��ʱ��������ʵĵ���ƽ�ⳣ����K(CH3COOH)��1.8��10��5��K(HSCN)��0.13�����ܵ���ʵ��ܶȻ�������Ksp(CaF2)��6��10��10����25 ��ʱ��2.0��10��3 mol/L�����ˮ��Һ�У�������ҺpH(��������仯)���õ�c(HF)��c(F��)����ҺpH�ı仯��ϵ������ͼ��ʾ��
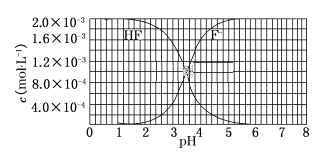
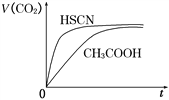
�����������Ϣ�ش��������⣺
��1��25 ��ʱ����20 mL 0.10 mol/L CH3COOH��Һ��20 mL 0.10 mol/L HSCN��Һ�ֱ���20 mL 0.10 mol/L NaHCO3��Һ��ϣ�ʵ���ò������������(V)��ʱ��(t)�ı仯��ͼ��ʾ����Ӧ��ʼ�Σ�������Һ����CO2��������ʴ������Բ����ԭ����__________����Ӧ��������������Һ�У�c(CH3COO��)________c(SCN��)(������������������������)��
��2��25 ��ʱ��HF����ƽ�ⳣ������ֵKa��______��
��3��4.0��10-3 mol/L HF��Һ��4.0��10-4mol/L CaCl2��Һ�������ϣ����ڻ��ҺpHΪ4.0�������Ե���ʱ���Һ����ı仯����_______��������������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ���н϶��Na2SO4��������Fe2��SO4��3�����ø���Һ��ȡâ�����ɹ�ѡ��IJ�����
�ټ�������H2SO4��Һ �ڼӽ���Na �۽ᾧ �ܼӹ���NaOH��Һ �ݼ�ǿ���ѽᾧˮ ���ˡ���ȷ�IJ���������
A.�ڢޢ�B.�ܢޢ٢�C.�ܢޢۢ�D.�ڢޢ٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25mL 0.1mol/L NaOH��Һ����μ���0.2mol/L CH3COOH��Һ��������ͼ��ʾ�������й�����Ũ�ȹ�ϵ�ıȽϣ���ȷ���� �� ��
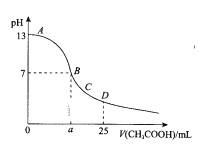
A. ��A��B����һ�㣬��Һ��һ������c(Na+)>c(CH3COO��)>c(OH��)>c(H+)
B. ��B�㣬a>12.5������c(Na+)��c(CH3COO��)=c(OH��)=c(H+)
C. ��C�㣺 c(Na+)> c(CH3COO��) > c(OH��)>c(H+)
D. ��D�㣺c(CH3COO��)+ c(CH3COOH)��2 c(Na+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽����ҵ���ϵ������ã�ij��ѧ��ȤС���������ͼʵ�鷽�����ú�����������ͭ�ĺϽ���ȡ�Ȼ������̷����壨FeSO47H2O���͵������壮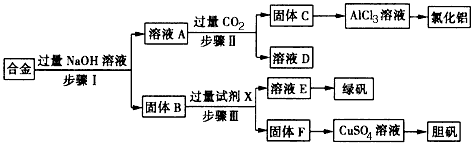
��ش�
��1��������о�����е�ʵ������� �� ʵ�����н��иò���ʱ���õ��IJ����������ձ��� ��
��2����ҺA�е���������Ҫ�����Լ�X�� ��
��3������ҺA��ͨ�����CO2�������ɹ���C�����ӷ���ʽΪ ��
��4���ӻ��������Ƕȿ��ǣ��ù���F�Ʊ�CuSO4��Һ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ۺ����ü������ڽ�Լ��Դ���������ڱ���������ʵ�������÷����ɵ�ص�ͭñ(Zn��Cu�ܺ���ԼΪ99%)����ͭ���Ʊ�ZnO�IJ���ʵ��������£�
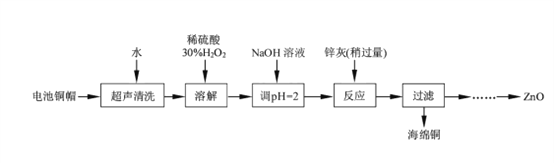
��1����ͭñ�ܽ�ʱ����H2O2��Ŀ����_______________���û�ѧ����ʽ��ʾ����
��ͭñ�ܽ���轫��Һ�й���H2O2��ȥ����ȥH2O2�ļ�㷽����_________________��
��2��Ϊȷ������п������Ҫ�ɷ�ΪZn��ZnO������Ϊ��������������������ʵ������ⶨ��ȥH2O2����Һ��Cu2���ĺ�����ʵ�����Ϊ��ȷ��ȡһ������ĺ���Cu2������Һ�ڴ�����ƿ�У�������ˮϡ�ͣ�����pH=3��4���������KI����Na2S2O3����Һ�ζ����յ㡣���������е����ӷ���ʽ���£�2Cu2����4I��=2CuI(��ɫ)����I2��I2��2S2O32��=2I����S4O62��
�ٵζ�ѡ�õ�ָʾ��Ϊ________________���ζ��յ�۲쵽������Ϊ________________��
�����ζ�ǰ��Һ��H2O2û�г��������ⶨ��Cu2���ĺ�������______________������ƫ������ƫ����������������
��3����֪pH��11ʱZn(OH)2������NaOH��Һ����[Zn(OH)4]2�����±��г��˼����������������������pH����ʼ������pH����������Ũ��Ϊ1.0 mol/L������
��ʼ������pH | ��ȫ������pH | |
Fe3�� | 1.1 | 3.2 |
Fe2�� | 5.8 | 8.8 |
Zn2�� | 5.9 | 8.9 |
ʵ���п�ѡ�õ��Լ���30% H2O2��1.0 mol��L��1HNO3��1.0 mol��L��1 NaOH��
�ɳ�ȥͭ����Һ�Ʊ�ZnO��ʵ�鲽������Ϊ��������Һ�м���30%��H2O2ʹ���ַ�Ӧ��
�ڵμ�1.0 moL/L���������ƣ�����pHԼΪ_________________��ʹFe3��������ȫ��
�۹��ˣ�
������Һ�еμ�1.0 moL/L���������ƣ�����pHԼΪ________��ʹZn2��������ȫ��
��____________________________��
��900�����ա�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��50 mL 0.6 mol��L��1����������Һ�����������Ƶ����ʵ���Ϊ (����)
A. 0.03 mol B. 0.04 mol C. 0.05 mol D. 0.06 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A.�����Ȼ���������Һ�����ˮ�У��ټ��ȼ����Ӻ�ɵõ�������������
B.�������������ɢ��������ֽ��Ҳ������Ĥ
C.��Һ�ͽ���ı��������ǿɷ��������ЧӦ
D.������������Һ�������Ȼ�����Һ�пɵõ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������װ�û�����ܴﵽʵ��Ŀ��(��Ҫ�ļг�װ�ü�ʯ������ʡ��)����

A. ʵ��������ϩ
B. ʵ��������Ȳ����֤��Ȳ�ܷ���������Ӧ
C. ʵ�����з���ʯ��
D. ����Ϊ���ᣬ��Ϊ����(��״)����Ϊ��������Һ����֤���ᡢ̼�ᡢ�������Ե�ǿ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com