
| ||
| 8 |
| 3 |
| ||
| 8mol×27g/mol |
| 13.5g |
| ||
| ||
| 8 |
| 3 |
| 9 |
| 8 |
| 3 |
| 2 |
| 9 |
| 8 |
| 3 |
| 2 |


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
| A、甲=丙>乙 |
| B、丙>乙>甲 |
| C、乙>丙>甲 |
| D、甲=乙=丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
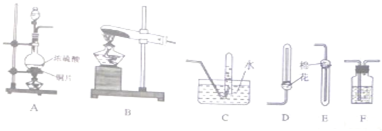
查看答案和解析>>
科目:高中化学 来源: 题型:
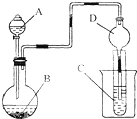
| A、若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色 |
| B、若A为醋酸,B为贝壳,C中盛澄清石灰水,则C中溶液无变化 |
| C、若A为浓氨水,B为生石灰,C中AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解 |
| D、实验仪器D主要起到防止溶液倒吸的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4、C2H4 |
| B、CH4、C3H6 |
| C、C2H2、C3H4 |
| D、C2H2、C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4.5 g |
| B、9.9 g |
| C、13.2 g |
| D、14.7 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液的pH值:②>①>③ |
| B、水电离出的c(OH-):③>①=② |
| C、①和③等体积混合后的溶液:c(CH3COOH)+c(CH3COO-)=0.1mol/L |
| D、②和③等体积混合后的溶液:c(Na+)=c(CH3COOH)+c(CH3COO-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com