
根据下面物质间转化的框图,回答有关问题;
`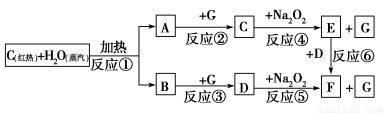
(1)由反应①产生的A、B混合物的工业名称是________。
(2)写出框图中D、E的化学式:D________;E________。
(3)如果2 mol Na2O2与足量水蒸气反应,可得标准状况下气体的体积是________L,同时反应中转移电子总数是____________。(NA表示阿伏加德罗常数)
(4)如果A、B混合气体7.8 g,在与G充分反应后,通过足量Na2O2层,可使Na2O2增重________g。
(1)水煤气
(2)CO2 NaOH
(3)22.4 2NA
(4)7.8
【解析】(1)由碳与水蒸气反应的产物成分可知,此混合物的工业名称为水煤气。
(2)由图中信息及E+D―→F可推知,A为氢气,B为CO,故E为NaOH,D为CO2。(3)由化学方程式:2Na2O2+2H2O=4NaOH+O2↑可知,若2 mol Na2O2参加反应,则生成1 mol氧气,在标准状况下体积为22.4 L;同时有2 mol电子发生转移。(4)由2H2+O2=2H2O及2Na2O2+2H2O=4NaOH+O2↑可推知:过氧化钠增加的质量为氢气的质量;由2CO+O2=2CO2及2Na2O2+2CO2=2Na2CO3+O2可推知:过氧化钠增加的质量为CO的质量,故二者不管比例如何,它们通过Na2O2充分反应后,过氧化钠增加的质量即是氢气和一氧化碳的质量,为7.8 g。


科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-1练习卷(解析版) 题型:实验题
一般测定样品中成分含量的实验应重复2~3次。为了测定某氢氧化钠固体中混有的碳
酸钠的质量分数,甲、乙、丙三位同学分别设计了如下实验方案:
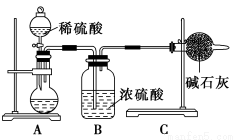
Ⅰ.甲同学的方案如图所示:
(1)如何检验A装置的气密性?___________________________________。
(2)甲同学重复进行了三次实验,得到碳酸钠的质量分数的数据存在较大的偏差,你认为可能引起测量结果偏低的原因是________(填序号)。
A.装置内原有空气中的二氧化碳气体也被碱石灰吸收
B.装置外空气中的水蒸气和二氧化碳被碱石灰吸收
C.反应完成后,装置中的二氧化碳没有全部被碱石灰吸收
D.加入稀硫酸的量不足、反应不充分
(3)为了让甲的实验测量结果更准确,在其他实验步骤都正确的条件下,你认为图中的实验装置应该如何改进:___________________________________________。
Ⅱ.乙同学的方案是:从图中所提供的装置中选择实验装置,代替甲同学实验装置中的B、C,通过测定放出的二氧化碳的体积(不考虑二氧化碳溶于水)来计算。
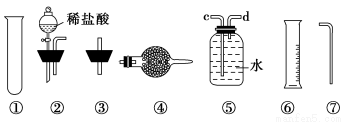
选择最简装置的连接顺序为________。
Ⅲ.丙同学的方案是:称取样品m g,并溶解,加入过量氯化钡溶液,过滤、洗涤、烘干、称量,得固体n g。
(1)配制100 mL 0.10 mol/L BaCl2溶液的实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外还有______(填仪器名称)。
(2)混合物中碳酸钠的质量分数为(用m、n表示)________。
(3)Ca2+、Ba2+都可以使CO32—沉淀完全,能否使用氯化钙溶液代替氯化钡溶液?________(填“能”或“否”),原因是:______________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-1练习卷(解析版) 题型:填空题
生活和生产中常用到胶体的性质,请看下述四例:
(1)做实验时,手指不慎被玻璃划破,可从急救箱中取氯化铁溶液应急止血,其原理是
_______________________________________________。
(2)在陶瓷工业上常遇到因陶土里混有氧化铁而影响产品质量。解决方法之一是把这些陶土和水一起搅拌,使微粒直径在10-9~10-7m之间,然后插入两根电极,再接通直流电源。这时阳极聚集陶土胶粒,阴极聚集氧化铁胶粒,理由是________。
(3)水泥和冶金工厂常用高压电对气溶胶作用以除去大量烟尘,减少对空气的污染,这种作用运用了________原理。
(4)四氧化三铁在强碱性溶液中与次氯酸盐反应,生成高铁酸盐(FeO42—),FeO42—有强氧化性,可以杀菌消毒。高铁酸盐还有净化水的作用,能净化水的原因是 ______________________________________________________
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-3练习卷(解析版) 题型:填空题
根据下列各题所给出的数据,可分别求出其“溶质的质量分数”或“溶质的物质的量
浓度”,试判断并求解。
(1)设NA表示阿伏加德罗常数的数值,若某氢氧化钠溶液V L中含有N个OH-,则可求出此溶液中______________________为__________________。
(2)已知某氢氧化钠溶液中Na+与H2O的个数之比为1∶a,则可求出此溶液中________为________。
(3)已知标准状况下1体积水能溶解500体积的氯化氢,则可求出标准状况下氯化氢饱和溶液中__________为________。
(4)已知将100 mL氯化铝的水溶液加热蒸干灼烧,可得到白色固体b g,则可求出原氯化铝溶液中________为________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-3练习卷(解析版) 题型:选择题
硫酸铜水溶液呈酸性,属保护性无机杀菌剂,对人畜比较安全,其同石
灰乳混合可得“波尔多”溶液。实验室里需用480 mL 0.10 mol/L的硫酸铜溶液,则应选用的容量瓶规格和称取溶质的质量分别为( )
A.480 mL容量瓶,称取7.68 g硫酸铜
B.480 mL容量瓶,称取12.0 g胆矾
C.500 mL容量瓶,称取8.00 g硫酸铜
D.500 mL容量瓶,称取12.5 g胆矾
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-2练习卷(解析版) 题型:选择题
标准状况下,1 L的密闭容器中恰好可盛放n个N2分子和m个H2分子组成的混合气体,则阿伏加德罗常数可近似表示为( )
A.22.4(m+n)
B.22.4×6.02×1023(m+n)
C.22.4(m+n)/(6.02×1023)
D.m+n
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-2练习卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下列叙述错误的是( )
A.18 g H2O中含有的质子数为10NA
B.12 g金刚石中含有的共价键数为4NA
C.46 g NO2和N2O4混合气体中含有原子总数为3NA
D.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习2-3-2氧化还原反应方程式配平及计算练习卷(解析版) 题型:填空题
雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为 。
(2)上述反应中的氧化剂是 ,反应产生的气体可用 吸收。
(3)As2S3和HNO3有如下反应:
As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O若生成2 mol H3 AsO4,则反应中转移电子的物质的量为 。若将该反应设计成一原电池,则NO2应该在 (填“正极”或“负极”)附近逸出。
(4)若反应产物NO2和11.2 L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量 (选填编号)。
a.小于0.5 mol b.等于0.5 mol
c.大于0.5 mol d.无法确定
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十五 有机判断型专题练习卷(解析版) 题型:选择题
近年来流行喝苹果醋。苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等作用的保健食品。苹果酸(α?羟基丁二酸)是这种饮料的主要酸性物质,其结构如下图所示:

下列相关说法正确的是( )
A.苹果酸在一定条件下能发生消去反应
B.苹果酸在一定条件下能催化氧化生成醛
C.苹果酸在一定条件下能发生加聚反应生成高分子化合物
D.1 mol苹果酸与NaHCO3溶液反应最多消耗3 mol NaHCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com