
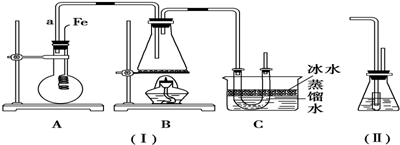
分析 由实验装置可知,A中苯与溴发生取代反应生成溴苯,生成的HBr进入B中,B中乙醇、HBr在浓硫酸作用下发生取代反应生成溴乙烷,C中冰水冷却,
(1)长导管起到冷凝回流作用;
(2)形管内用蒸馏水封住管底可防止HBr逸出;
(3)溴乙烷不溶于水,溶液分层;
(4)证明溴和苯的上述反应是取代反应而不是加成反应,即检验溴离子.
解答 解:由实验装置可知,A中苯与溴发生取代反应生成溴苯,生成的HBr进入B中,B中乙醇、HBr在浓硫酸作用下发生取代反应生成溴乙烷,C中冰水冷却,
(1)导管a的作用是导气、冷凝,故答案为:导气、冷凝;
(2)C装置中U形管内用蒸馏水封住管底的作用是溶解HBr,防止HBr及产物逸出,故答案为:溶解HBr,防止HBr及产物逸出;
(3)反应完毕后,U形管内的现象是液体分层,下层为无色油状液体;分离出溴乙烷时所用最主要仪器的名称是分液漏斗,
故答案为:液体分层,下层为无色油状液体;分液漏斗;
(4)证明溴和苯的上述反应是取代反应而不是加成反应,即检验溴离子.
①装置(Ⅱ)的锥形瓶中为苯,其作用为吸收挥发出的Br2蒸气,小试管内的液体是水,其作用为吸收HBr气体,
故答案为:苯吸收挥发出的Br2蒸气,水吸收HBr气体;
②反应后,向锥形瓶中滴加AgNO3溶液,生成AgBr沉淀,观察到现象为生成淡黄色沉淀,可说明苯与溴发生取代反应生成溴苯和HBr,故答案为:AgNO3;生成淡黄色沉淀.
点评 本题考查物质的制备实验,为高频考点,把握制备实验装置、有机物的性质、发生的反应为解答的关键,侧重分析与实验能力的综合考查,题目难度中等.


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 2:3 | B. | 1:2 | C. | 3:1 | D. | 1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(Ba2+)=C(SO42-)=Ksp½ | |
| B. | C(Ba2+)•C(SO42-)>Ksp C(Ba2+)=C(SO42-) | |
| C. | C(Ba2+)•C(SO42-)=Ksp C(Ba2+)>C(SO42-) | |
| D. | C(Ba2+)•C(SO42-)≠Ksp C(Ba2+)<C C(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在任何条件下,化学反应的焓变都等于化学反应的反应热 | |
| B. | △H>0时反应放热,△H<0时反应吸热 | |
| C. | △H越大,说明反应放出的热量越多 | |
| D. | 一个化学反应中,当反应物能量大于生成物能量时,反应放热,△H为“-” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:8 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2是还原剂,PbCl2是氧化剂 | B. | CuCl2是还原剂,O2是氧化剂 | ||
| C. | 乙烯是还原剂,O2是氧化剂 | D. | PbCl2和CuCl2都是氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com