
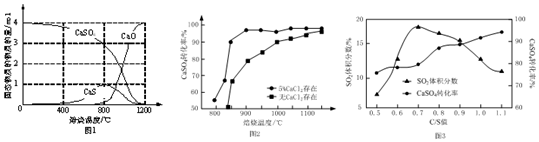
���� ��1��������֪�Ȼ�ѧ����ʽ����Ŀ�귽��ʽ�����ݸ�˹���ɼ���õ�Ŀ�귽��ʽ�ķ�Ӧ�ȣ�
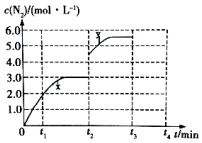
��2���ٴ�ͼʾ1��֪�ڵ���800��ʱ��Ҫ��ԭ����ΪCaS������800��ʱ��Ҫ�����ƺ�����Ʒ�Ӧ���������ƺͶ�������
�����Ȼ��ƺ����Ȼ��ƴ��ڵķ�Ӧ������ƽ����ͬ�����ı䷴Ӧ���̣�����CaCl2Ϊ���������¶ȸ���1200��ʱ���ﵽƽ�⣬��������ܸı�ƽ�⣬������������CaCl2��CaSO4��ת����������ͬ��
��̼�Ͷ�����̼�ڸ��������·�Ӧ��������һ����̼�����Ե�$\frac{C}{S}$ֵ����0.7ʱ����Ӧ����������SO2�������������������Ҳ������ת�����������ʣ�
��3����Ӧ�����ӷ���ʽΪCaSO4��s��+CO32-��aq��?SO42-��aq��+CaCO3��s��������Ksp��CaSO4��=c��Ca2+����c��SO42-����Ksp��CaCO3��=c��Ca2+����c��CO32-������c��CO32-����
��� �⣺��1����֪��CaSO4•2H2O��s���TCaSO4•$\frac{1}{2}$H2O��s��+$\frac{3}{2}$H2O��g����H1=83.2kJ•mol-1
��CaSO4•2H2O��s���TCaSO4��s��+2H2O��l����H2=26kJ•mol-1
��H2O��g��=H2O��l����H3=-44kJ•mol-1
����-�ۡ�2-�ٵ�CaSO4•$\frac{1}{2}$H2O��s���TCaSO4��s��+$\frac{1}{2}$H2O��g�������H4=[26kJ•mol-1-��-44kJ•mol-1����2-83.2kJ•mol-1]=30.8kJ•mol-1��
�ʴ�Ϊ��30.8��
��2���ٴ�ͼʾ1��֪���ڵ���800��ʱ��CaS�ɷֵ����ʵ���Ϊ1����CaO�����ʵ�������Ϊ0�������ڵ���800��ʱ��Ҫ��ԭ����ΪCaS������800��ʱ��Ҫ�����ƺ�����Ʒ�ӦCaS+3CaSO4$\frac{\underline{\;����\;}}{\;}$4CaO+4SO2���������Ƶ����ʵ������ӣ��Ƶ����ʵ�����С��
�ʴ�Ϊ��CaS��CaS+3CaSO4$\frac{\underline{\;����\;}}{\;}$4CaO+4SO2����
�ڴ������ܸı䷴Ӧ�����ʣ��ı䷴Ӧ���̣������ܸı仯ѧƽ�⣬��ͼʾ��֪�����¶ȸ���1200��ʱ����������CaCl2��CaSO4��ת����������ͬ������CaCl2�������������������¶ȸ���1200��ʱ����������CaCl2��CaSO4�ķ�Ӧ��������·�Ӧ���ﵽƽ�⣬����CaCl2���ı�ƽ����ƶ���
�ʴ�Ϊ������������������·�Ӧ���ﵽƽ�⣬����CaCl2���ı�ƽ����ƶ���
�۵�$\frac{C}{S}$ֵ����0.7ʱ�������£�������C��CO2��Ӧ����CO���壬��Ӧ����ΪCaO��SO2��CO2��CO��ʹ�������������Ҳ��������Ʋ���ת��Ϊ�����������ʣ�
�ʴ�Ϊ�������£�������C��CO2��Ӧ����CO��ʹ�������������ת��Ϊ�����������ʣ���
��3����Ӧ�����ӷ���ʽΪCaSO4��s��+CO32-��aq��?SO42-��aq��+CaCO3��s��������Ӧ�ﵽƽ�����Һ��c��SO42-��=2.0mol•L-1����֪Ksp��CaSO4��=c��Ca2+����c��SO42-��=7.10��10-5��c��Ca2+��=3.55��10-5mol•L-1��Ksp��CaCO3��=6.2125��10-7��Ksp��CaCO3��=c��Ca2+����c��CO32-����c��CO32-��=1.75��10-2 mol•L-1��
�ʴ�Ϊ��1.75��10-2 mol•L-1��
���� ���⿼�鷴Ӧ�ȵļ��㡢��ѧƽ���ƶ�Ӱ�����ء������ܽ�ƽ��ļ��㣬���ո�˹���ɵ�����Ӧ���Լ�������ƽ���Ӱ���ǽ��ؼ�����Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2H2S | B�� | NH3 HCl | C�� | P4 CCl4 | D�� | C2H4 CH4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ������˵��������ǣ�������
������˵��������ǣ�������| A�� | X����������̼ԭ��һ����ͬһƽ���� | |
| B�� | X����ϩ������ͬϵ�� | |
| C�� | Y�ɷ���ȡ����Ӧ��������Ӧ | |
| D�� | Y�ĺ�����ͬ�����ŵ�ͬ���칹����8�֣������������칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | �缫��Ӧʽ | ���ֵĻ��� |
| A | O2+2H2O+4e-�T4OH- | ���Ի���������ȼ�ϵ�صĸ�����Ӧ |
| B | 4OH--4e-�TO2��+2H2O | �����Ի����¸�����������ʴ |
| C | Cu-2e-�TCu2+ | ��ͭ���缫���NaOH��Һ��������Ӧ |
| D | H2-2e-�T2H+ | �ö��Ե缫���H2SO4��Һ��������Ӧ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��֪��298K��101kPa�����£������·�Ӧ��
��֪��298K��101kPa�����£������·�Ӧ��| ���ʣ�mol�� ʱ�� | NO | CO | N2 | CO2 |
| ��ʼ | 0.40 | 1.0 | ||
| 2min ĩ | 2.0 | 0.80 | 1.6 | |
| 4min ĩ | 1.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ϊ��ȥ����CuCl2��Һ�к��е�����Fe3+�����ڼ��ȡ�����������¼��백ˮ�����˺�������Һ�м����������� | |
| B�� | �ڹ�ҵ�ϳ�NH3�ķ�Ӧ�У���ȡ���´�ʩ | |
| C�� | �����£���ƽ����ϵH2��g��+Br2��g��?2HBr��g����ѹ����ʹ������ɫ���� | |
| D�� | ���Ȼ�����Һ�в��ϻ�����ͨ��HCl���壬���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ĵ���ʽ��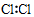 | B�� | �����Ľṹʽ��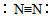 | ||
| C�� | Fһ�Ľṹʾ��ͼ�� | D�� | H2O2�ĵ���ʽ��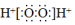 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com