
(17分)美日科学家因研发“有机合成中的钯催化的交叉偶联”而获得2010年度诺贝尔化学奖。有机合成常用的钯/活性炭催化剂长期使用,催化剂会被杂质(如:铁、有机物等)污染而失去活性,成为废催化剂,故需对其回收再利用。一种由废催化剂制取氯化钯(PdCl2)的工艺流程如下:
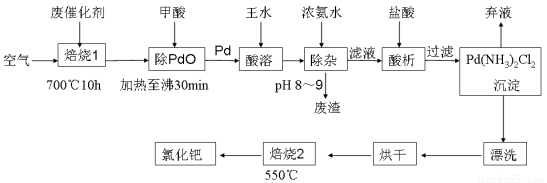
(1)甲酸还原氧化钯的化学方程式为 。
(2)加浓氨水时,钯元素转变为可溶性[Pd(NH3)4]2+,此时铁元素的存在形式是 (写化学式)。
(3)王水是浓硝酸与浓盐酸按体积比1∶3混合而成的,钯在王水中溶解的过程中有化合物A和一种无色、有毒气体B生成。
①气体B的化学式为
②经测定,化合物A由3种元素组成,有关元素的质量分数为Pd:42.4%,H:0.8%。则A的化学式为 ;
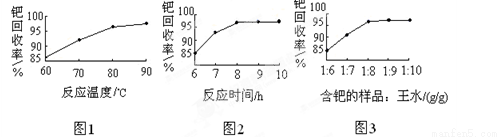
(4)钯的回收率高低主要取决于王水溶解的操作条件,已知反应温度、反应时间和王水用量对钯回收率的影响如图1~图3所示,则王水溶解钯的适宜条件是:反应温度为 ,反应时间约为 ,含钯的样品与王水的质量比为 。
(5)700℃“焙烧1”的目的是 , 550℃“焙烧2”的目的是 。
(1)PdO+HCOOH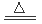 Pd+CO2↑+H2O;(2)Fe(OH)3;(3)①NO;②H2PdCl4;(4)80~90℃;8h;1:8;(5)除去活性炭及有机物,脱氨[或“将Pd(NH3)2Cl2转变为PdCl2”]
Pd+CO2↑+H2O;(2)Fe(OH)3;(3)①NO;②H2PdCl4;(4)80~90℃;8h;1:8;(5)除去活性炭及有机物,脱氨[或“将Pd(NH3)2Cl2转变为PdCl2”]
【解析】
试题分析:(1)甲酸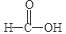 分子中含有醛基,有还原性,能把氧化钯还原为Pd,它本身被氧化为碳酸,反应的化学方程式为PdO+HCOOH
分子中含有醛基,有还原性,能把氧化钯还原为Pd,它本身被氧化为碳酸,反应的化学方程式为PdO+HCOOH Pd+CO2↑+H2O;(2)王水有强的氧化性,会把Fe氧化为Fe3+,加浓氨水时,钯元素转变为可溶性[Pd(NH3)4]2+,此时铁元素也会形成Fe(OH)3沉淀。(3)①王水把Pb氧化时,其中的硝酸被还原得到无色、有毒的气体B是NO;②Pd:42.4÷106.4=0.4;H:0.8÷1=0.8.所以Pd:H=1:2.由于Pd是+2价,H为+1价,根据化合物的正负化合价的代数和为O,所以还应该含有4个-1价的阴离子。它的物质的量为0.4mol×4=1.6mol.因此其相对原子质量为:(1-42.4%-0.8%)÷(0.4×4)=35.5。所以该离子是Cl-。A的化学式为H2PdCl4;(4)由题目提供的示意图可知则王水溶解钯的适宜的反应温度为80~90℃;反应时间约为8小时,含钯的样品与王水的质量比为1:8。(5)700℃“焙烧1”的目的是除去废Pd催化剂中的活性炭及有机物杂质;550℃“焙烧2”的目的是将Pd(NH3)2Cl2煅烧使之转变为PdCl2。
Pd+CO2↑+H2O;(2)王水有强的氧化性,会把Fe氧化为Fe3+,加浓氨水时,钯元素转变为可溶性[Pd(NH3)4]2+,此时铁元素也会形成Fe(OH)3沉淀。(3)①王水把Pb氧化时,其中的硝酸被还原得到无色、有毒的气体B是NO;②Pd:42.4÷106.4=0.4;H:0.8÷1=0.8.所以Pd:H=1:2.由于Pd是+2价,H为+1价,根据化合物的正负化合价的代数和为O,所以还应该含有4个-1价的阴离子。它的物质的量为0.4mol×4=1.6mol.因此其相对原子质量为:(1-42.4%-0.8%)÷(0.4×4)=35.5。所以该离子是Cl-。A的化学式为H2PdCl4;(4)由题目提供的示意图可知则王水溶解钯的适宜的反应温度为80~90℃;反应时间约为8小时,含钯的样品与王水的质量比为1:8。(5)700℃“焙烧1”的目的是除去废Pd催化剂中的活性炭及有机物杂质;550℃“焙烧2”的目的是将Pd(NH3)2Cl2煅烧使之转变为PdCl2。
考点:考查废催化剂制取氯化钯(PdCl2)的反应原理、反应条件的选择、化学式的确定、方程式的书写。


 能力评价系列答案
能力评价系列答案科目:高中化学 来源:2013-2014陕西省富平县高二下学期期末考试化学试卷(解析版) 题型:填空题
(5分)观察下列结构简式,回答下列问题:
Ⅰ、乙酸的结构简式为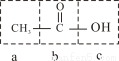
(1)a的名称是__________。
(2)c的名称是________________。
Ⅱ、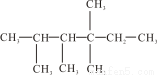
(1)有机物名称是__________________________。
(2)此有机物为烯烃加成的产物,则原来烯烃的结构可能有_______种。
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期期中考试高二化学试卷(解析版) 题型:选择题
能说明氯的非金属性比硫强的事实是( )
A.氯气与氢气反应生成氯化氢,而硫与氢气反应生成硫化氢
B.向硫化氢的水溶液中通入氯气可得到淡黄色的硫
C.氯气能与水反应而硫不能
D.氯原子最外电子层上有7个电子而硫最外电子层上有6个电子
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期期中考试高一化学试卷(解析版) 题型:选择题
下列有关说法正确的是( )
A.大多数金属在自然界以游离态形式存在
B.工业上,一般用热还原法获得Hg和Ag
C.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
D.人们常用钢作建造材料而不用纯铁主要原因是钢的机械性能更好
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期期中考试高一化学试卷(解析版) 题型:选择题
硒被誉为“生命的奇效元素”,富硒食品倍受追捧,重庆多地打造富硒农产品基地。已知硒元素与氧元素同族,与钙元素同周期,下列关于硒的描述错误的是( )
A.原子序数是24
B.元素周期表中硒位于第四周期第VIA族
C.最高价氧化物是SeO3,是酸性氧化物
D.气态氢化物化学式是H2Se,稳定性比HCl差
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市5月高三月考理综化学试卷(解析版) 题型:选择题
甲、乙、丙、丁为中学常见物质,其中甲、乙为单质,丙为氧化物,它们之间存在如图所示的转化关系。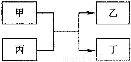 下列说法正确的是
下列说法正确的是
A.若甲、乙均为金属单质,则丁所属的物质类别一定是碱性氧化物
B. 若甲为金属单质,乙为非金属单质,则甲只能是Mg
C.若甲、乙元素是同主族元素,根据元素周期表推测,此时乙单质可能是Si
D.若甲、乙元素是同周期元素,则该反应的化学方程式一定为:2F2 + 2H2O=4HF + O2
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市名校联盟高三三诊理综化学试卷(解析版) 题型:填空题
(14分)湿法炼锌的冶炼过程可用下图简略表示:
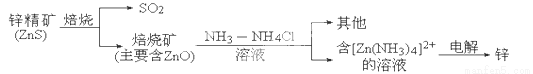
请回答下列问题:
(1)已知:N2(g)+2H2(g)===N2H4(l) ΔH=a kJ·mol-1,该反应不能自发进行,则a 0(填“>”、“<”或“=”).
(2)ZnS焙烧的反应2ZnS+3O2 2SO2+2ZnO所涉及的物质中,发生氧化反应的物质是 ,不含离子键的化合物是 .
2SO2+2ZnO所涉及的物质中,发生氧化反应的物质是 ,不含离子键的化合物是 .
(3)电解过程中析出锌的电极反应式为___________________________.
(4)产生的SO2可用Ba(NO3)2溶液吸收,部分产物可作为工业原料,其反应的离子方程式为 .
(5)锌-空气电池与锂电池相比,具有储存电量高、成本低、没有安全隐患等优点。该电池的总反应为2Zn+O2===2ZnO,电解质溶液为KOH溶液,则负极的电极反应式为 。25℃时,以该电池为电源,用两个等质量的铜棒作电极电解500 mL 0.1mol/L CuSO4溶液,一段时间后切断电源,对电极干燥并称量,测得两电极的质量差为9.6 g,则至少需要________L空气(折算成标准状况)进入该电池。
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市高三5月月考理综化学试卷(解析版) 题型:选择题
下列实验对应的结论正确的是:
| A | B | C | D |
装 置 |
|
|
|
|
结 论 | 实验室制取乙炔 | 能证明非金属性 Cl>C>Si | 分离出Cl2与KI溶 液反应生成的碘 | 白色沉淀是BaSO3 |
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市万州区高三考前模拟理综化学化学试卷(解析版) 题型:简答题
(15分)
铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)单质铁属于 晶体,将FeCl3溶液加热蒸干、灼烧所得的物质是 (填化学式).
(2)请写出铝与氢氧化钠溶液反应的化学方程式____
(3)金属Cu单独与氨水或单独与双氧水都不反应,但可与二者的混合溶液反应生成深蓝色溶液,该深蓝色的浓溶液中加入乙醇所产生的现象是 ,画出呈深蓝色的离子的结构式____ 写出Cu与氨水、双氧水反应的离子方程式:____
(4)在硫酸亚铁溶液中加入过量的碳酸氢铵,有FeCO3沉淀生成,写出其化学方程式____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com