
(分)以硫酸工艺的尾气、氨水、石灰石、焦炭及碳酸氢铵和KCl为原料可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸氢铵等物质且利用率较高。合成路线如下:
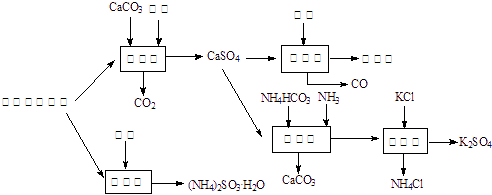
⑴生产中,反应Ⅱ中往往需要向溶液中加入适量的对苯二酚等物质,其目的是 。
⑵下列有关说法正确的是_______________。
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅲ中发生反应的化学方程式为:CaSO4+4C![]() CaS +4CO↑
CaS +4CO↑
C.反应Ⅳ需控制在60~70 ℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
⑶反应Ⅴ反应液用40%乙二醇溶液,温度控制在25 ℃,硫酸钾的产率超过90%,其原因是_________________________。
⑷(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为N2,若某尾气含标准状况试写出二氧化氮与亚硫酸铵反应的化学方程式___________________________。
⑴防止亚硫酸铵被氧化(2分)
⑵ABCD(4分)
⑶乙二醇是有机溶剂能减小K2SO4的溶解度,使硫酸钾充分析出(2分)
⑷4(NH4)2SO3+2NO2 = 4(NH4)2SO4+N2 ↑(2分)
本题涉及5个反应,反应I为2SO2+2CaCO3+O2![]() 2CaSO4+2CO2,很显然该反应过程中若通入足量的空气,可提高SO2的转化率。反应II为SO2+2NH3·H2O
2CaSO4+2CO2,很显然该反应过程中若通入足量的空气,可提高SO2的转化率。反应II为SO2+2NH3·H2O![]() (NH4)2SO3·H2O+H2O,由于亚硫酸盐易被氧化,因此加入抗氧化剂对苯二酚可防止产物被氧化。反应III提供的原料是CaSO4和焦炭,产物是CaS和CO,易得化学方程式为CaSO4+4C
(NH4)2SO3·H2O+H2O,由于亚硫酸盐易被氧化,因此加入抗氧化剂对苯二酚可防止产物被氧化。反应III提供的原料是CaSO4和焦炭,产物是CaS和CO,易得化学方程式为CaSO4+4C![]() CaS +4CO↑。反应IV中原料涉及易分解的NH4HCO3,因此反应应控制在一定温度下以防止铵盐分解。反应V的化学方程式为(NH4)2SO4+2KCl
CaS +4CO↑。反应IV中原料涉及易分解的NH4HCO3,因此反应应控制在一定温度下以防止铵盐分解。反应V的化学方程式为(NH4)2SO4+2KCl![]() 2NH4Cl+K2SO4。
2NH4Cl+K2SO4。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
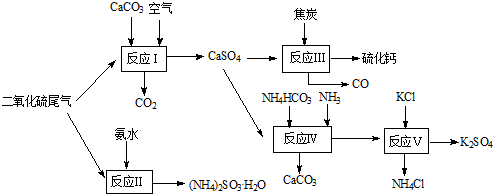
(8分)以硫酸工艺的尾气、氨水、石灰石、焦炭及碳酸氢铵和KCl为原料可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸氢铵等物质。合成路线如下:
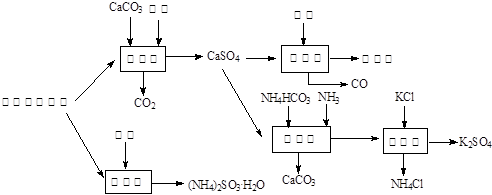
(1)生产中,反应Ⅱ中往往需要向溶液中加入适量的对苯二酚等物质,其目的是 ▲ 。
(2)下列有关说法正确的是 ▲ 。
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅲ中发生反应的化学方程式为:CaSO4+4C![]() CaS+4CO↑
CaS+4CO↑
C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
(3)反应Ⅴ反应液用40%乙二醇溶液,温度控制在25℃,硫酸钾的产率超过90%,其原因是
▲ 。
(4)(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为N2,试写出二氧化氮与亚硫
酸铵反应的化学方程式 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)以硫酸工艺的尾气、氨水、石灰石、焦炭及碳酸氢铵和KCl为原料可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸氢铵等物质。合成路线如下:
(1)生产中,反应Ⅱ中往往需要向溶液中加入适量的对苯二酚等物质,其目的是 。
(2)下列有关说法正确的是 。
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅲ中发生反应的化学方程式为:CaSO4+4CCaS +4CO↑
C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
(3)反应Ⅴ反应液用40%乙二醇溶液,温度控制在25℃,硫酸钾的产率超过90%,其原因是 。
(4)(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为N2,试写出二氧化氮与亚硫酸铵反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2010年江苏省高三第四次模拟考试化学试题 题型:填空题
(8分)以硫酸工艺的尾气、氨水、石灰石、焦炭及碳酸氢铵和KCl为原料可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸氢铵等物质。合成路线如下:
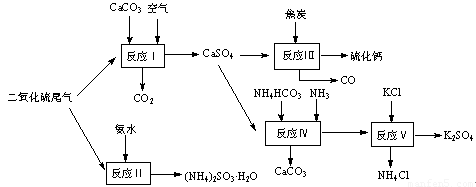
(1)生产中,反应Ⅱ中往往需要向溶液中加入适量的对苯二酚等物质,其目的是 。
(2)下列有关说法正确的是 。
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅲ中发生反应的化学方程式为:CaSO4+4C CaS +4CO↑
CaS +4CO↑
C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
(3)反应Ⅴ反应液用40%乙二醇溶液,温度控制在25℃,硫酸钾的产率超过90%,其原因是 。
(4)(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为N2,试写出二氧化氮与亚硫酸铵反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com