
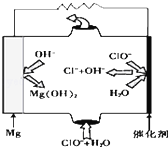
 ��������Ȼ�ѧ����ʽ����ѧ����ʽ���缫��Ӧʽ������ʽ�ȣ�����д��
��������Ȼ�ѧ����ʽ����ѧ����ʽ���缫��Ӧʽ������ʽ�ȣ�����д��| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ij�¶�ʱ��BaSO4��ˮ�еij����ܽ�ƽ�⣺BaSO4��s��?Ba2+��aq��+SO42-��aq��Ksp=c��Ba2+��?c��SO42-���������ܽ�ƽ��������ͼ��ʾ������˵����ȷ���ǣ�������
ij�¶�ʱ��BaSO4��ˮ�еij����ܽ�ƽ�⣺BaSO4��s��?Ba2+��aq��+SO42-��aq��Ksp=c��Ba2+��?c��SO42-���������ܽ�ƽ��������ͼ��ʾ������˵����ȷ���ǣ�������| A��b��ʱc��Ba2+��?c��SO42- ��С��Ksp |
| B��a���Ӧ��Ksp����c���Ӧ��Ksp |
| C����ˮϡ�Ϳ���ʹ��Һ��b��䵽c�� |
| D������������Na2SO4������ʹ��Һ��a��䵽c�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼװ�ã��Թ���ʢ��ˮ������a��ʢ�и����Na2O2������U�ι���ע��dz��ɫ��ˮ������������Ƥ��������Թܿڣ�ʵ��ʱ�������е�Na2O2���䵽�Թ�b��ˮ�У��������������ǣ�������
��ͼװ�ã��Թ���ʢ��ˮ������a��ʢ�и����Na2O2������U�ι���ע��dz��ɫ��ˮ������������Ƥ��������Թܿڣ�ʵ��ʱ�������е�Na2O2���䵽�Թ�b��ˮ�У��������������ǣ�������| A��U�ι��ں�ɫ��ȥ |
| B���Թ�����Һ��� |
| C������a��� |
| D��U�ι�ˮλd��c |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
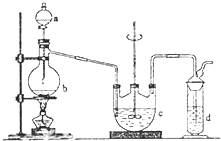 ��ʵ�����п�ͨ�����·�Ӧ��ȡ���������Na2S2O3��2Na2S+Na2CO3+4SO2�T3Na2S2O3+CO2
��ʵ�����п�ͨ�����·�Ӧ��ȡ���������Na2S2O3��2Na2S+Na2CO3+4SO2�T3Na2S2O3+CO2�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A����KMnO4��ĩ��ȡO2 |
| B����Ũ��ˮ��CaO��ȡNH3 |
| C����Zn��ϡ������ȡH2 |
| D����ʯ��ʯ��ϡ������ȡCO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ˮ�еμ�ŨH2SO4��KW���� |
| B��CaCO3������ϡ���ᣬҲ�����ڴ��� |
| C��25��ʱ���ô�����Һ�ζ���Ũ��NaOH��Һ��pH=7��V������VNaOH |
| D��NaCl��Һ��CH3COONH4��Һ�������ԣ�����Һ��ˮ�ĵ���̶���ͬ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com