
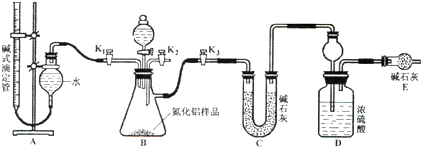
分析 从实验装置和实验步骤上看,本实验的原理是用足量硫酸与样品中Al4C3完全反应,测量生成的甲烷气体,从而可测得Al4C3的百分含量;用足量NaOH溶液与样品中AlN完全反应,用浓硫酸充分吸收生成的氨气,并称量其质量,从而求得AlN的质量分数.
(1)②AlN水解得到氢氧化铝与氨气,氢氧化铝与NaOH溶液反应生成偏铝酸钠;
(3)关闭活塞K2、K3,打开活塞 K1,通过分液漏斗加入过量的稀硫酸,与烧瓶内物质充分反应,测量生成甲烷气体的体积.待反应进行完全后,关闭活塞K1,打开活塞K3,通过分液漏斗加入过量的NaOH溶液,与烧瓶内物质充分反应,由于装置中残留部分氨气,打开K2,通入空气一段时间,排尽装置的氨气,被装置D完全吸收,测定生成氨气质量;
(4)①根据氮原子的守恒,氨气的物质的量等于AlN的物质的量,可求得AlN的质量分数;
②读取滴定管中气体的体积时,液面左高右低,气体的压强大于大气压,测定气体甲烷的体积偏小;
②根据碳原子的守恒,Al4C3的物质的量等于甲烷的物质的量的三分之一,可求得Al4C3的质量分数;
(5)B装置分液漏斗中的稀硫酸滴入锥形瓶中会排出一部分空气,按甲烷的体积进行了测定.
解答 解:从实验装置和实验步骤上看,本实验的原理是用足量硫酸与样品中Al4C3完全反应,测量生成的甲烷气体,从而可测得Al4C3的百分含量;用足量NaOH溶液与样品中AlN完全反应,用浓硫酸充分吸收生成的氨气,并称量其质量,从而求得AlN的质量分数.
(1)②AlN水解得到氢氧化铝与氨气,氢氧化铝与NaOH溶液反应生成偏铝酸钠,总反应方程式为:AlN+NaOH+H2O=NaAlO2+NH3↑,
故答案为:AlN+NaOH+H2O=NaAlO2+NH3↑;
(3)关闭活塞K2、K3,打开活塞 K1,通过分液漏斗加入过量的稀硫酸,与烧瓶内物质充分反应,测量生成甲烷气体的体积.待反应进行完全后,关闭活塞K1,打开活塞K3,通过分液漏斗加入过量的NaOH溶液,与烧瓶内物质充分反应,由于装置中残留部分氨气,打开K2,通入空气一段时间,排尽装置的氨气,被装置D完全吸收,防止测定的氨气的质量偏小,测定生成氨气质量,
故答案为:关闭活塞K2、K3,打开活塞K1;打开活塞K2,通入空气一段时间;
(4)①氨气的质量为(z-y)g,物质的量为$\frac{(z-y)g}{17g/mol}$=$\frac{z-y}{17}$mol,根据氮原子的守恒,氨气的物质的量等于AlN的物质的量,所以AlN的质量为$\frac{z-y}{17}$mol×41g/mol=$\frac{41(z-y)}{17}$g,故AlN的质量分数为$\frac{\frac{41(z-y)}{17}g}{xg}$×100%=$\frac{41(z-y)}{17x}$×100%,
故答案为:$\frac{41(z-y)}{17x}$×100%;
②读取滴定管中气体的体积时,液面左高右低,气体的压强大于大气压,测定气体甲烷的体积偏小,
故答案为:偏小.
③甲烷的体积为(a-b)mL,物质的量为$\frac{(a-b)×1{0}^{-3}L}{{V}_{m}L/mol}$=$\frac{(a-b)}{{V}_{m}}$×10-3mol,根据碳原子的守恒,Al4C3的物质的量等于甲烷的物质的量的三分之一,所以Al4C3的质量为$\frac{1}{3}$×$\frac{(a-b)}{{V}_{m}}$×10-3mol×144g/mol=$\frac{48(a-b)}{{V}_{m}}$×10-3g,Al4C3的质量分数为$\frac{\frac{48(a-b)}{{V}_{m}}×1{0}^{-3}g}{xg}$×100%=$\frac{0.048(a-b)}{{V}_{m}x}$×100%,
故答案为:$\frac{0.048(a-b)}{{V}_{m}x}$×100%;
(5)B装置分液漏斗中的稀硫酸滴入锥形瓶中会排出一部分空气,也按甲烷的体积进行了测定,测得Al4C3的质量分数会偏高,
故答案为:B装置分液漏斗中的稀硫酸滴入锥形瓶中会排出一部分空气.
点评 本题考查对实验原理与操作步骤的理解、化学计算、物质组成的测定等,难度较大,是对所需知识的综合运用,需要学生具有扎实的基础知识与分析问题、解决问题的能力,理解实验原理是解答的关键.


科目:高中化学 来源: 题型:选择题
| A. | 该溶液中离子浓度关系为:c (Na+)>c(HCO3-)>c (OH-)>c(H+) | |
| B. | 25℃时,加水稀释后,$\frac{c(O{H}^{-})}{c({H}^{+})}$变小 | |
| C. | 温度升高,c(OH-)×c(H+)不变(忽略体积变化) | |
| D. | 溶液中c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
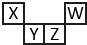 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Z所处的族序数是周期序数的2倍.下列判断不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Z所处的族序数是周期序数的2倍.下列判断不正确的是( )| A. | 最高正化合价:X<Y<Z | |
| B. | 原子半径:X<Y<Z | |
| C. | 气态氢化物的热稳定性:Z<W | |
| D. | 最高价氧化物对应水化物的酸性:X<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
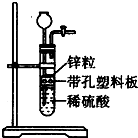 某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液体积不足液面无法浸没锌粒,而又无其他酸液可加入,为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④汽油⑤Na2C03溶液⑥KCl溶液( )
某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液体积不足液面无法浸没锌粒,而又无其他酸液可加入,为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④汽油⑤Na2C03溶液⑥KCl溶液( )| A. | ①②③ | B. | ②④⑤ | C. | ②③④⑥ | D. | ②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2:电解饱和食盐水 | B. | O2:过氧化氢与二氧化锰混合 | ||
| C. | H2:锌粒和稀硝酸混合 | D. | NH3:氮气和氢气混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝片与稀H2SO4反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | 灼热的碳与CO2反应 | D. | NaOH与HCl反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com