
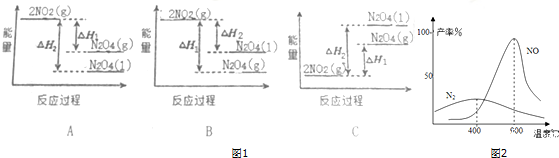
分析 (1)将NO2(g)转化为N2O4(g)的反应为放热反应,同种物质气态时能量比液态时能量高;
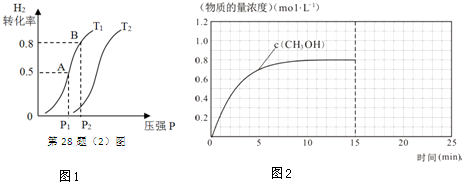
(2)根据图象可知温度低时生成氮气,温度高时生成NO,但该反应为放热反应,则温度高于900℃时,NO产率下降;
(3)①根据盖斯定律,由已知热化学方程式乘以合适的系数进行适当的加减,反应热也乘以相应的系数进行相应的加减;
②根据在反应中氨气做还原剂被氧化,次氯酸钠做氧化剂被还原来分析产物.
解答 解:(1)将NO2(g)转化为N2O4(g)的反应为放热反应,将N2O4(g)转化为N2O4(l)液为放热反应,所以在图象中该反应的反应物的总能量比生成物的总能量高,同种物质气态变液态会放出热量,即液态时能量比气态时能量低,则N2O4(l)具有的能量比N2O4(g)具有的能量低,图象A符合,故A正确;
故答案为:A;
(2)根据图象可知温度低时,氨气与氧气反应生成氮气;温度高时生成NO,但该反应为放热反应,当温度高于900℃时,温度越高,反应逆向进行的程度越大,则NO产率越小;
故答案为:N2;氨气转化为一氧化氮的反应为放热反应;
(3)①已知:N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ•mol-1①
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534.0kJ•mol-1②
NO2(g)?$\frac{1}{2}$N2O4(g)△H=-26.35kJ•mol-1③
根据盖斯定律,②×2-①-③×2得2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) 故△H=2×(-534.0kJ•mol-1)-67.7kJ•mol-1-2×(-26.35kJ•mol-1)=-1083.2kJ•mol-1;
故答案为:2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1083.0 kJ/mol;
②氨和次氯酸钠反应时,氨气中的氮元素被氧化为N2H4,NaClO中的氯元素被还原为NaCl,故化学方程式为:2NH3+NaClO=N2H4+NaCl+H2O,
故答案为:2NH3+NaClO=N2H4+NaCl+H2O.
点评 本题考查了能量变化图的分析、化学平衡移动的影响因素、盖斯定律的计算,题目难度中等,题目侧重于考查学生的综合运用能力,注意基础知识的积累掌握是关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
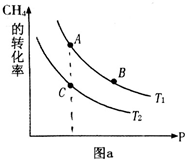 氢气、甲醇是优质的清洁燃料,可制作燃料电池.
氢气、甲醇是优质的清洁燃料,可制作燃料电池.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 | |
| B. | 活化分子间的碰撞一定能导致化学键断裂 | |
| C. | 在FeCl3+3KSCN═Fe(SCN)3+3KCl平衡体系中,加入KCl固体,平衡逆向移动 | |
| D. | NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g)△H=+185.57kJ/mol,能自发进行,原因是体系有自发地向熵增的方向转变的倾向 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | H2(g) | CO(g) | CH3OH(l) |
| 标准燃烧热(25℃) △H/kJ•mol-1 | -285.8 | -283.0 | -726.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 碳 | 氮 | Y | |
| X | 硫 | Z |
 ,其中氮的化合价为②-2,实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为③NaClO+2NH3=N2H4+NaCl+H2O .
,其中氮的化合价为②-2,实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为③NaClO+2NH3=N2H4+NaCl+H2O .查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3 是还原剂 | B. | CO是氧化剂 | ||
| C. | 氧化剂得到6mol电子 | D. | 还原剂失去8mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com