

| A. | e电极上可以析出使湿润的淀粉KI试纸变蓝的气体 | |
| B. | c电极周围溶液变红 | |
| C. | A烧杯内溶液的pH升高 | |
| D. | B烧杯中加一定量的KCl固体可恢复原状 |
分析 a电极上有红色物质析出,说明a为阴极,则b为阳极,c为阴极,d为阳极,e为阴极,电解池工作时阳极发生氧化反应,阴极发生还原反应,以此解答该题.
解答 解:a电极上有红色物质析出,说明a为阴极,则b为阳极,c为阴极,d为阳极,e为阴极,
A.e为阴极,电解氯化铜溶液时,阴极析出铜,故A错误;
B.c为阴极,生成氢气和氢氧化钠,可使酚酞变红,故B正确;
C.A中阳极铜被氧化,阴极析出铜,溶液浓度不变,故C错误;
D.B阳极析出氯气,阴极析出氢气,应通入氯化氢可恢复原状,故D错误.
故选B.
点评 本题综合考查原电池和电解池知识,为高考高频考点,侧重于学生的分析能力的考查,注意把握原电池和电解池的工作原理,把握电极方程式的书写方法,难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. |  从碘水中分离出碘 | B. |  检验试液中NH${\;}_{4}^{+}$的存在 | ||
| C. |  干燥SO2气体 | D. |  收集HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 的加成类似于
的加成类似于 的加成)
的加成) .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
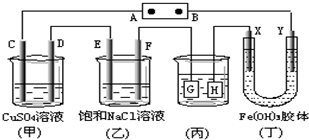
| A. | 电源B极是正极 | |
| B. | 欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 | |
| C. | 甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1:2:2:2 | |
| D. | 装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带负电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
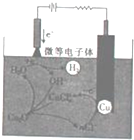 氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂灯领域有着广泛的用途.回答下列问题:
氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂灯领域有着广泛的用途.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是放热反应都是自发的,由于吸热反应都是非自发的 | |
| B. | 自发反应一定是熵增大,非自发反应一定是熵减少或不变 | |
| C. | 电解池的反应属于自发过程 | |
| D. | 自发反应在恰当条件下才能实现 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com