
【题目】硫酸铜溶液中滴入乙二胺(H2N—CH2—CH2—NH2)即可形成配离子A,其结构如图:

(1)基态的Cu2+核外电子排布式为________。
(2)元素C、N、O的第一电离能由大到小排列顺序为_______;![]() 的空间构型为________。
的空间构型为________。
(3)A中所形成的配离子中含有的化学键类型有__________(填标号)。
a.配位键 b.极性键 c.离子键 d.非极性键
(4)乙二胺分子中氮原子轨道的杂化类型为___________,乙二胺和三甲胺 [N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是________。
(5)硫酸铜灼烧可以生成一种红色晶体,其结构如图所示,则该化合物的化学式是____。已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a=______cm。(用含ρ、NA的计算式表示)

【答案】ls22s22p63s23p6 3d9或[Ar] 3d9 N>O> C 正四面体 abd sp3 乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键 Cu2O ![]()
【解析】
(1)铜是29号元素失去外层两个电子形成铜离子;
(2)根据同周期从左到右,元素的第一电离能呈增大趋势,但N元素原子的2p能级处于半满稳定状态,能量较低,第一电离能高于同周期相邻的元素;根据价层电子对互斥理论判断空间构型;
(3)根据成键原子的特点判断化学键类型;
(4)根据价层电子对数判断乙二胺分子中氮原子的杂化类型,根据是否含有氢键分析二者熔沸点高低不同的原因;
(5)均摊法计算晶胞中Cu、O原子数目,确定化学式;结合晶胞中原子数目计算晶胞质量,再根据晶胞体积求晶体密度=晶胞质量÷晶胞体积。
(1)Cu是29号元素,处于第四周期IB族,核外电子排布式为:1s22s22p63s23p63d104s1,失去最外层两个电子形成Cu2+,所以基态的Cu2+核外电子排布式为ls22s22p63s23p6 3d9或[Ar] 3d9;
(2)根据分析可知元素C、N、O的第一电离能由大到小排列顺序为N>O> C;SO42-中S原子孤电子对数=![]() ,价层电子对数为
,价层电子对数为![]() ,所以为sp3杂化,分子空间构型为正四面体,故答案为:N>O> C;正四面体;
,所以为sp3杂化,分子空间构型为正四面体,故答案为:N>O> C;正四面体;
(3)A中所形成的配离子中含有的化学键中N与Cu之间为配位键,C-C键为非极性键,C-N、N-H、C-H键为极性键,不含离子键,故答案为:abd;
(4)乙二胺分子中氮原子形成3个σ键,还有一孤电子对,所以价层电子对数为4,所以氮原子为sp3杂化,乙二胺分子间可以形成氢键,物质的熔沸点较高,而三甲胺分子间不能形成氢键,熔沸点较低,故答案为:sp3;乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键;
(5)Cu原子位于晶胞内部,O原子处于晶胞体心、顶点,晶胞中Cu原子数目=4、O原子数目=1+8×![]() =2,Cu、O原子数目之比为2:1,故化学式为Cu2O;晶胞质量m=
=2,Cu、O原子数目之比为2:1,故化学式为Cu2O;晶胞质量m=![]() ,若晶胞边长为acm,则晶胞体积为V =a3cm3,则晶胞密度
,若晶胞边长为acm,则晶胞体积为V =a3cm3,则晶胞密度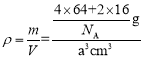 ,解得a=
,解得a=![]() cm,故答案为:Cu2O;
cm,故答案为:Cu2O;![]() 。
。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】(亚硝酸钠(NaNO2)是工业盐的主要成分,在漂白、电镀等方面应用广泛。实验室利用下图装置制备亚硝酸钠,并测定所制亚硝酸钠的纯度。(加热装置及部分夹持装置已略去)
Ⅱ.亚硝酸钠纯度的测定。
当Na2O2完全反应后,E中产生的固体除NaNO2外,还可能有NaNO3。测定亚硝酸钠纯度的步骤如下:
步骤一:取反应后的固体4.30 g溶于稀硫酸,向所得溶液中加入足量KI,将溶液中的NO2-和NO3-全部还原为NO,并通入足量N2,将NO全部赶出,最后将溶液稀释至1000 mL。
步骤二:取上述所得溶液10 mL,用淀粉作指示剂,用0.050 mol/L的Na2S2O3标准液滴定,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,最终消耗Na2S2O3溶液体积为16.00 mL。
(1)步骤二中达到滴定终点的标志为______________________。
(2)混合固体中NaNO2的质量分数为________。(保留三位有效数字)
(3)若在滴定终点读取滴定管刻度时,仰视标准液液面,则测得亚硝酸钠的纯度________。(填“偏高”“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.1000 mol·L-1盐酸滴入20.00 mL 0.100 0mol·L-1的某一元碱MOH溶液中,溶液的pH随加入盐酸体积变化曲线如下图所示。下列有关说法不正确的是( )

A.该一元碱的电离方程式为MOH = M++OH-
B.a、b、c三点中,b点水的电离程度最大
C.室温下,MOH的电离常数Kb=1×10-5 mol·L-1
D.b点:c (M+)=c (Clˉ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉水解的产物,设计如下实验方案:
![]()
请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是_________;
(2)试剂2为_________NaOH溶液,其作用是_________,使检验水解产物的实验得以顺利进行;发生反应的离子方程式为:_________;
(3)反应①的化学方程式为_________;
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是_________;
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的_________(填”能”或”否”)否,若不能,其原因是_________硫酸能溶解Cu(OH)2而使实验失败,最简单的改正措施是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3COOH、H2SO3是中学化学中常见的弱酸,请回答下列问题:
(1)常温下,下列叙述能证明CH3COOH为弱酸是_________。
a. CH3COONa 溶液的pH大于7;
b.相同体积相同浓度的盐酸和醋酸溶液,分别与足量锌粉反应,放出相同体积的氢气;
c.相同体积、相同pH的盐酸和醋酸,醋酸中和NaOH的物质的量多;
d.0.01mol/L的CH3COOH溶液,PH > 2
(2)常温下,向0.1 mol·L-1 CH3COOH溶液中加蒸馏水稀释,稀释后,下列各量增大的是_________:
a.![]() b.
b.![]() c.c(OH-)
c.c(OH-)
(3)将浓度均为0.1mol/LCH3COOH和CH3COONa溶液等体积混合,测得混合液中c(CH3COO-)>c(Na+),则下列关系式中正确的是(_____)
A.c(H+) > c(OH-) B.c(H+) < c(OH-)
C.c(CH3COOH) > c(CH3COO-) D.c(CH3COOH) + c(CH3COO-)=0.1mol/L
(4)若等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,溶液呈_______(填“酸性”,“中性”或“碱性”),原因是 _______________(用离子方程式表示)。若将pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈__________(填“酸性”,“中性”或“碱性”),溶液中c(Na+) ___________c(CH3COO-) (填“ >” 或“=”或“<” )。
(5)25℃时,H2SO3的电离常数Ka1=1×10-2mol/L,Ka2=6×10-3mol/L,则该温度下NaHSO3的水解平衡常数Kh=__________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下发生下列反应,其中属于盐类水解反应的是( )
A.CH3COO—+H2O![]() CH3COOH+OH—
CH3COOH+OH—
B.Cl2+H2O ![]() H++Cl-+HClO
H++Cl-+HClO
C.CH3COOH+NaOH![]() CH3COONa+H2O
CH3COONa+H2O
D.HCO3—+H2O![]() H3O++CO32-
H3O++CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
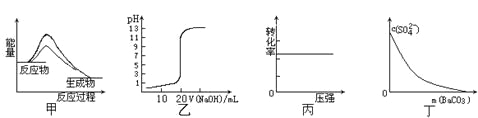
A.图甲表示使用催化剂后,该反应的ΔH变小
B.图乙表示0.10mol·L-1NaOH溶液滴定20.00mL0.10mol·L-1CH3COOH溶液所得到的滴定曲线
C.图丙表示反应H2(g) + I2(g)![]() 2HI(g)中H2的转化率随压强的变化
2HI(g)中H2的转化率随压强的变化
D.图丁表示在饱和Na2SO4溶液中逐步加BaCO3固体后,溶液中c(SO42-)的浓度变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是

A.图甲表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
B.图乙是金刚石与石墨分别氧化生成CO2的能量关系曲线,说明石墨转化为金刚石的反应的ΔH>0
C.图丙表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率大于b点
D.图丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关晶体的叙述中,错误的是
A.氯化钠晶体中,每个Na+周围距离相等且最近的Na+共有6个
B.金属晶体中,以“…ABCABCABC…”形式的堆积称为面心立方堆积
C.干冰晶体中,每个CO2分子周围距离相等且最近的CO2分子共有12个
D.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com