
| A、原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
| B、原子核外M层上有2个电子的X原子与原子核外N层上有2个电子的Y原子 |
| C、2p轨道上有一个未成对电子的X原子与3p轨道上有一个未成对电子的Y原子 |
| D、L 层上只有一个空p轨道的X原子与M层有一个空p轨道的Y原子 |


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
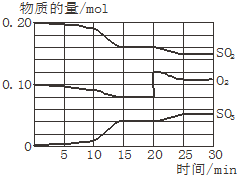 一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示:回答下列问题:
一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示:回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 将镁带投入盛放在敞口容器的盐酸里,产生H2的速率与时间的关系可由如图表示.
将镁带投入盛放在敞口容器的盐酸里,产生H2的速率与时间的关系可由如图表示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、带相反电荷的离子之间的相互吸引称为离子键 |
| B、金属元素与非金属元素化合时不一定形成离子键 |
| C、离子化合物中一定含有离子键,不可能含有共价键 |
| D、强酸、强碱和大多数盐都属于离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25 | B、30 | C、55 | D、80 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 卢瑟福的α粒子轰击金箔实验推翻了汤姆森在1903年提出的原子结构模型,为建立现代原子理论打下了基础.如图线条中,可能是α粒子(带正电)在该实验中的运动轨迹的是( )
卢瑟福的α粒子轰击金箔实验推翻了汤姆森在1903年提出的原子结构模型,为建立现代原子理论打下了基础.如图线条中,可能是α粒子(带正电)在该实验中的运动轨迹的是( )| A、abcd | B、abc |
| C、bcd | D、ad |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:5 | B、1:2 |
| C、4:5 | D、2:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com