
下列关于热化学反应的描述中正确的是( )
|
| A. | HCl和NaOH反应的中和热△H=﹣57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJ/mol |
|
| B. | CO(g)的燃烧热是283.0 kJ/mol,则2C02(g)=2CO(g)+02(g)反应的△H=+2×283.0 KJ/mol |
|
| C. | 反应A(s)+B(g)=C(s)+D(s)能自发进行,则一定有△H>0 |
|
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
考点:
热化学方程式;反应热和焓变.
专题:
化学反应中的能量变化.
分析:
A、依据中和热概念是强酸强碱的稀溶液完全反应生成1mol水放出的热量分析判断;
B、燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量,反应方向改变焓变符号改变;
C、反应自发进行的依据是△H﹣T△S<0;
D、燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量;
解答:
解:A、中和热概念是强酸强碱的稀溶液完全反应生成1mol水放出的热量,故A错误;
B、CO(g)的燃烧热是283.0 kJ/mol,则2C02(g)=2CO(g)+02(g)反应的△H=+2×283.0 KJ/mol,故B正确;
C、反应A(s)+B(g)=C(s)+D(s)能自发进行,△S<0,△H<0低温下可以存在△H﹣T△S<0,则不一定有△H>0,故C错误;
D、1mol甲烷燃烧生成液态水和二氧化碳所放出的热量是甲烷的燃烧热,故D错误;
故选B.
点评:
本题考查了燃烧热,中和热概念分析应用,反应自发进行的判断依据,掌握和理解概念实质是解题关键,题目难度中等.


科目:高中化学 来源: 题型:
迷迭香酸具有抗氧化、延缓衰老、减肥降脂等功效,它的结构简式为:
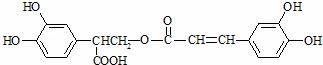
以邻苯二酚为原料合成迷迭香酸的路线为:
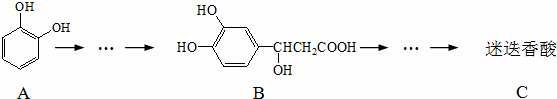
下列说法正确的是( )
|
| A. | 有机物A分子中所有原子一定在同一平面上 |
|
| B. | 有机物B可以发生取代、加成、消去、氧化反应 |
|
| C. | 有机物C在稀硫酸催化下水解的一种产物是B |
|
| D. | 1 mol B与足量的NaOH溶液反应,最多可消耗4 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金。
Ⅰ.氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示。
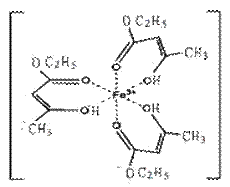
(1)此配合物中,铁离子的价电子排布式为 。
(2)此配合物的-C2H5中C-H间形成化学键的原子轨道分别是 ; 。
Ⅱ.(2)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n ,与Ni(CO)n中配体互为等电子体的离子的化学式为 (写出一个即可)。
(2)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途。已知CuH晶体结构单元如图所示。该化合物的的密度为ρg/cm3,阿伏加德罗常数的值为NA,则该晶胞中Cu原子与H原子之间的最短距离为 cm(用含ρ和NA的式子表示)。
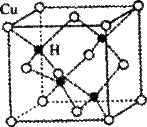
Ⅲ.硼元素在化学中有很重要的地位,硼及其化合物广泛应用于永磁材料、超导材料、富燃料材料、复合材料等高新材料领域应用。
(1)三氟化硼在常温常压下为具有刺鼻恶臭和强刺激性的无色有毒腐蚀性气体,其分子的立体构型为 ,B原子的杂化类型为 。
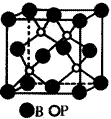
(2)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。下图示意的是磷化硼的晶体结构单元,则磷化硼的化学式为 ,微粒间存在的作用力为 。
(3)正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子间通过氢键相连(如下图)。
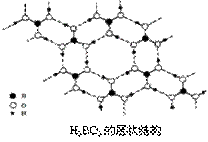
①1 mol H3BO3的晶体中有 mol氢键。
②硼酸溶于水应生成弱电解质一水合硼酸H2O·B(OH)3,它电离生成少量[B(OH)4]- 和的H+ 离子。则硼酸为 元酸,[B(OH)4]-含有的化学键类型为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
120℃时,1体积某烃和4体积O2混和,完全燃烧后恢复到原来的温度和压强,体积不变,该烃分子式中所含的碳原子数不可能是( )
|
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,0.1mol•L﹣1的HA溶液中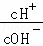 =1010,0.01mol•L﹣1的BOH溶液pH=12.请回答下列问题:
=1010,0.01mol•L﹣1的BOH溶液pH=12.请回答下列问题:
(1)HA是 (填“强电解质”或“弱电解质”,下同),BOH是 .
(2)HA的电离方程式是 .
(3)在加水稀释HA的过程中,随着水量的增加而减小的是 (填字母).
A.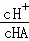 B.
B.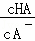 C.c(H+)与c(OH﹣)的乘积 D.c(OH﹣)
C.c(H+)与c(OH﹣)的乘积 D.c(OH﹣)
(4)在体积相等、pH相等的HA溶液与盐酸溶液中加入足量Zn,HA溶液中产生的气体比盐酸中产生的气体 (填“多”、“少”或“相等”).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表示方法正确的是( )
|
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
|
| B. | 由C(石墨)→C(金刚石);△H=+1.9 kJ/mol可知,金刚石比石墨稳定 |
|
| C. | 在稀溶液中:H+(aq)+OH﹣(aq)═H2O(l);△H=﹣57.3 kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的稀溶液混合,放出的热量大于57.3 kJ |
|
| D. | 在101kPa、25℃时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l);△H=﹣285.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质的颜色变化,可用勒夏特列原理解释的是( )
|
| A. | 光照氯水,颜色变浅 |
|
| B. | 向盛有NO2的集气瓶中投入活性炭,颜色变浅 |
|
| C. | 加热氯化铁溶液,溶液变浑 |
|
| D. | 压缩H2与I2(g)反应的平衡混合气体,颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,某化合物W受热分解:2W A↑+2B↑+4C↑,测得反应后生成的混合气体是相同条件下等体积H2质量的11.43倍,则W的摩尔质量是( )
A↑+2B↑+4C↑,测得反应后生成的混合气体是相同条件下等体积H2质量的11.43倍,则W的摩尔质量是( )
A. 11.43 B. 22.86g/mol C. 80.01 D. 80.01g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
用所学知识回答问题:
(1)浓硝酸久置常会显黄色,是因为 (用化学反应方程式表示),可采用 的方法消除黄色.
(2)酸性高锰酸钾溶液的氧化性比普通高锰酸钾的氧化性强,酸化时所用的酸为 ,向酸性KMnO4溶液中加入KI溶液,溶液紫红色褪去(所得溶液可使淀粉溶液变蓝),请写出KMnO4溶液褪色的离子方程式
(3)硫化氢的水溶液久置于空气中会变浑浊,请写出相关的化学反应方程式
(4)配平下面的化学方程式: Cu2O+ HNO3→ Cu(NO3)2+ NO↑+ H2O.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com