
���� ��1�����ݵ�ط�Ӧʽ�ж������������ݵ�ʧ�����жϷ�Ӧ���ͣ����ݵ��������жϵ������������ƶ�����
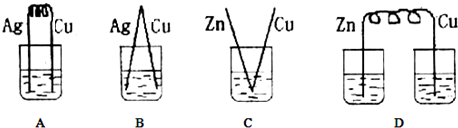
��2��ͭ��ϡ�����Ӧ�����װ����ͭ�缫�ϲ�����������˵����װ�ù�����ԭ��أ���ͭ��������
��3�����ݵ�ط�Ӧʽ=������Ӧʽ+������Ӧʽ��д��������Ӧʽ����Ӧʽ��
��4������ȼ�ϵ���У������ڸ�������������Ӧ������������������ԭ��Ӧ���鲻��ȫ����������̼�����Ӷ������缫������ͨ��������ȼ�ϵ�����ɵĶ�����̼�ܹ���KOH��Һ��Ӧ��������Һ���Լ�����
��� �⣺��1�����ݷ�Ӧ����ʽ֪�����õĽ��������������Ը�����Al������ʧ���ӷ���������Ӧ���缫��ӦʽΪAl-3e-=Al3+������Ϊ���������ӴӸ��������·�����������������෴�������������·�������������Ͼۼ��������ӣ�����������������������������������
�ʴ�Ϊ��������Al-3e-=Al3+��������������
��2���⣺ͭ��ϡ�����Ӧ�����װ����ͭ�缫�ϲ�����������˵����װ�ù�����ԭ��أ���ͭ��������
A��Cu��Ag������ϡ���ᷴӦ�����ܷ����Է���������ԭ��Ӧ�����ܹ���ԭ��أ���A����
B��Cu��Ag������ϡ���ᷴӦ�����ܷ����Է���������ԭ��Ӧ����װ�ò��ܹ���ԭ��أ���B����
C����װ�ù���ԭ��أ�Zn��ʧ������������ͭ�����������Է�����������C��ȷ��
D����װ�ò��ܹ��ɱպϻ�·�����Բ����γ�ԭ��أ���D����
�ʴ�Ϊ��C��
��3����ʽ��ȼ�ϵ�صĵ�������ᣬ����ܷ�Ӧʽ���ɱ�ʾΪ��2H2+O2=2H2O��
�为����ӦΪ��2H2-4e-=4H+ �ڣ�
��������ӦΪ ��-�ڣ���O2+4e-+4H+=2H2O���ʴ�Ϊ��O2+4e-+4H+=2H2O��
��4���ټ���ȼ�ϵ���У������ڸ�������������Ӧ������������������ԭ��Ӧ����صĵ�����Dz�����Y2O3��ZrO2���壬���������ŵ����������ӣ��缫��ӦʽΪO2+4e-=2O2-���ʴ�Ϊ��O2+4e-=2O2-��
���鲻��ȫ����������̼�����Ӷ������缫������ͨ�����ʴ�Ϊ��̼��
�ۼ���ȼ�ϵ�����ɵĶ�����̼�ܹ���KOH��Һ��Ӧ��������Һ���Լ������ʴ�Ϊ��������
���� ���⿼�黯ѧ��Դ���͵���Լ�ԭ��ص��жϡ��缫��Ӧʽ��д����Ŀ�Ѷ��еȣ�ע��缫��Ӧʽ����д��


 ����С����ͬ������ϵ�д�
����С����ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ֻ��������Ԫ����ͬ���Ҹ�Ԫ�ص���������Ҳ��ͬ��������һ����ͬ���칹�� | |
| B�� | ��������6��̼ԭ�ӵ���ֻ���γ�5��̼̼���� | |
| C�� | ��ϩ�����е�����ԭ�Ӷ���ͬһƽ���� | |
| D�� | ����ʽΪC3H6Cl2��C3H2Cl6���л��������е�ͬ���칹����Ŀ��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 254gI2�� g����ͨ�� 2gH2�� g������Ӧ���� 9.48 kJ | |
| B�� | 1mol��̬����1mol��̬���������������17.00kJ | |
| C�� | ��Ӧ��1���IJ���ȷ�Ӧ��2���IJ����ȶ� | |
| D�� | ��Ӧ��2���ķ�Ӧ���������ȷ�Ӧ��1���ķ�Ӧ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
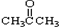 ��CH3CH2Br ��
��CH3CH2Br ��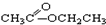 ��
��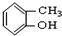 ��
��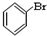 ��
�� ��
��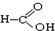 ��
��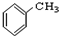 ��
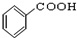
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �μӷ�Ӧ�����ʵ������Ǿ�����ѧ��Ӧ���ʵ���Ҫ���� | |
| B�� | ����Ӱ��ijЩ��ѧ��Ӧ���ʵ��������֮һ | |
| C�� | �ڸ��������£���һ�����淴Ӧ�ﵽƽ��״̬ʱ������������Ӧ���ܴﵽ���� | |
| D�� | ����ʲô��Ӧ������Ũ�ȣ�����Ȼ��ѹ����ʹ�ô����������Լӿ췴Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | NaOH��NaCl��HCl��Na2SO4 | B�� | NaCl��Na2SO4��NaOH��HCl | ||
| C�� | NaCl��NaOH��Na2SO4��HCl | D�� | Na2SO4��NaOH��NaCl��HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ�д��ڳ����ܽ�ƽ�⣺AgCl ��s��?Ag+��aq��+Cl-��aq�� | |
| B�� | ʵ�����֤��NH3���Ag+������Cl-ǿ | |
| C�� | ��������Ϣ����֪����Ũ��������ɵij���ΪAgCl | |
| D�� | ʵ�����ʵ���ҿ��ð�ˮϴ��������Ӧ����Թ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ù���������ữ�ĺ����ҽ���Һ����ȡ�⣺2I-+H2O2+2H+�TI2+2H2O | |
| B�� | ij��Һ�д��ڴ���Fe3+��S2-��Cl-��Na+������NaOH��Һ������Ӧ��Fe3++3OH-=Fe��OH��3�� | |
| C�� | ��AlCl3��Һ��Ͷ�������Na��Na+Al3++2H2O=Na++AlO2-+2H2�� | |
| D�� | ��Na2O2����Ͷ��H218O�У�2H218O+2Na2O2=4OH-+4Na++18O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10mL 0.5mol/L CH3COONa��Һ��6mL 1mol/L�����ϣ�c��Cl-����c��Na+����c��CH3COO-����c��H+����c��OH-�� | |
| B�� | ��Ũ�ȵ�����ϡ��Һ������������ �������� �۴��� ��̼������ �������� �ޱ����ƣ����ǵ�pH��С��������Ϊ���ۢݢ٢ܢڢ� | |
| C�� | ������0.1 mol/L��������Һ ��NH4Al��SO4��2 ��NH4Cl ��NH3•H2O ��CH3COONH4��c ��NH4+���ɴ�С��˳���ǣ��ڣ��٣��ܣ��� | |
| D�� | ��25��ʱ����a mol•L-1�İ�ˮ��0.01 mol•L-1������������Ϸ�Ӧʱ��Һ��c��NH4+��=c��Cl-�����ú�a�Ĵ���ʽ��ʾNH3•H2O�ĵ��볣��Kb=$\frac{1{0}^{-9}}{a-0.01}$ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com