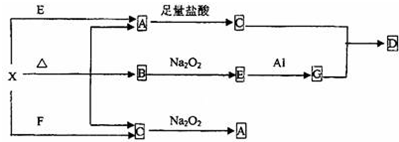
解答:
解:(1)C、D两种气体均能使澄清石灰水变浑浊,为SO
2、CO
2,A为短周期组成的黑色固体物质,与B的浓溶液共热时,产生SO
2、CO
2两种气体,同时生成水,A为C单质,B为浓硫酸,符合转化关系,反应方程式为:C+2H
2SO
4(浓)
CO
2↑+2SO
2↑+2H
2O,
a、二氧化硫和二氧化碳都不和氯化钡反应,所以现象相同,无法鉴别,故选;
b、二氧化硫能使酸性高锰酸钾褪色,二氧化碳不能使酸性高锰酸钾溶液褪色,所以能鉴别,故不选;
c、二氧化硫能使品红溶液褪色,二氧化碳不能使品红溶液褪色,所以能鉴别,故不选;
d、二氧化硫能和酸化的硝酸钡反应生成白色沉淀,二氧化碳不能和酸化的硝酸钡反应,所以能鉴别,故不选;
氢氧化钠的物质的量=2mol/L×0.5L=1mol,二氧化碳的物质的量是0.8mol,1<
=
<2,所以氢氧化钠和二氧化碳反应生成碳酸钠和碳酸氢钠,氢氧化钠和二氧化碳恰好反应生成碳酸钠和碳酸氢钠,反应方程式为:5NaOH+4CO
2═Na
2CO
3+3NaHCO
3+H
2O,
5NaOH+4CO
2═Na
2CO
3+3NaHCO
3+H
2O
5mol 4mol 1mol 3mol
1mol 0.8mol 0.2mol 0.6mol
通过方程式知,生成0.2mol碳酸钠、0.6mol碳酸氢钠,钠离子不水解,浓度最大,虽然碳酸钠和碳酸氢钠能水解,但盐在溶液中以电离为主,水解为次,所以碳酸氢根离子浓度大于碳酸根离子浓度,碳酸根离子和碳酸氢根离子水解导致氢氧根离子浓度大于氢离子浓度而使溶液呈碱性,所以溶液中离子浓度大小顺序为:c(Na
+)>c(HCO
3-)>c(CO
3 2- )>c(OH
-)>c(H
+),
故答案为:C+2H
2SO
4(浓)
CO
2↑+2SO
2↑+2H
2O;a;c(Na
+)>c(HCO
3-)>c(CO
3 2- )>c(OH
-)>c(H
+);
(2)若A为红色金属单质,与适量B的溶液在常温下恰好完全反应,生成的无色气体C遇空气迅速变成红棕色,则A为Cu,B为稀硝酸,C为NO,D为硝酸铜,反应方程式为:3Cu+8HNO
3(稀)=3Cu(NO
3)
2+2NO↑+4H
2O,1molHNO
3反应生成NO为1mol×
=0.25mol,标况下NO的体积为0.25mol×22.4L/mol=5.6L,故答案为:5.6;
(3)若生成的C、D为漂白粉的成分,其中D是漂白粉的有效成分,为氯气与氢氧化钙的反应,则D为Ca(ClO)
2,次氯酸钙与空气中二氧化碳、水反应生成次氯酸,次氯酸分解,而失去漂白性,反应方程式为:Ca(ClO)
2+H
2O+CO
2=CaCO
3+2HClO、2HClO
2HCl+O
2↑,
故答案为:Ca(ClO)
2+H
2O+CO
2=CaCO
3+2HClO、2HClO
2HCl+O
2↑;
(4)若反应A+B→C+D+H
2O 为实验室制取气体D的反应,且生成的D可以使紫色石蕊变蓝,则D为氨气,该反应为氯化铵与氢氧化钙的反应,反应方程式为:Ca(OH)
2+2NH
4Cl
CaCl
2+2NH
3↑+2H
2O,
故答案为:Ca(OH)
2+2NH
4Cl
CaCl
2+2NH
3↑+2H
2O.



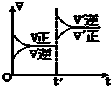 对达到平衡状态的可逆反应:X+Y?W+Z,在t℃时增大压强,则正逆反应速率变化如图所示(V代表速率,t代表时间)下列有关X、Y、Z、W的状态叙述正确的是( )
对达到平衡状态的可逆反应:X+Y?W+Z,在t℃时增大压强,则正逆反应速率变化如图所示(V代表速率,t代表时间)下列有关X、Y、Z、W的状态叙述正确的是( )