
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(s)+CO(g)MgO(s)+CO2(g)+SO2(g)△H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
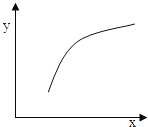
A. x表示温度,y表示容器内混合气体的密度
B. x表示CO的物质的量,y表示CO2与CO的物质的量之比
C. x表示SO2的浓度,y表示平衡常数K
D. x表示MgSO4的质量(忽略体积),y表示CO的转化率
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.硝酸银溶液与铜:Cu+Ag+=Cu2++Ag
B.氧化铜与盐酸反应:O2-+2H+=H2O
C.硫酸氢钠与氢氧化钠溶液混合:OH-+H+=H2O
D.向澄清石灰水中加入盐酸:2H++Ca(OH)2=Ca2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是( )
A. 反应达到平衡时,X的转化率为50%
B. 反应可表示为X+3Y ![]() 2Z,其平衡常数为1 600(mol/L) -2
2Z,其平衡常数为1 600(mol/L) -2
C. 增大压强使平衡向生成Z的方向移动,平衡常数增大
D. 改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃ 的恒温槽中,烧瓶内的气体逐渐变为红棕色:
N2O4(g)![]() 2NO2(g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2(g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①N2O4的消耗速率与NO2的生成速率之比为1:2
②NO2生成速率与NO2消耗速率相等
③烧瓶内气体的压强不再变化
④烧瓶内气体的质量不再变化
⑤NO2的物质的量浓度不再改变
⑥烧瓶内气体的颜色不再加深
⑦烧瓶内气体的平均相对分子质量不再变化
⑧烧瓶内气体的密度不再变化。
A. ②③⑥⑦ B. ①④⑧ C. 只有①④ D. 只有⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】成语是中华民族灿烂文化中的瑰宝,许多成语中蕴含着丰富的化学原理,下列成语中涉及氧化还原反应的是
A. 木已成舟 B. 铁杵成针 C. 蜡炬成灰 D. 滴水成冰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置和有关数据如下:

相对分子质量 | 密度/(g·cm3) | 沸点/℃ | 水中溶解性 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 112 | 难溶 |
实验步骤:
在A 中加入4.40g异戊醇、6.00g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯4.55g。
请回答下列问题:
(1)仪器B的名称是_____;B中冷却水是从_____(填“下口”或“上口”)流进的。
(2)加入碎瓷片的作用是_______;如果加热一段时间后发现忘记加瓷片,应该采取的操作是_____________________。
(3)在洗涤、分液操作中,第二次洗涤,用饱和碳酸氢钠溶液洗涤的主要目的是_______,不能用NaOH溶液洗涤的原因是___________。第二次洗涤后,充分振荡,然后静置,待分层后,产物应该从分液漏斗的_______(填“上口倒出”或“下口放出”)。
(4)在蒸馏操作中,仪器选择及安装都正确的是下图中的_____(填字母标号),若从130℃ 便开始收集馏分,会使实验的产率______(填“偏高”、“偏低”或“无影响”)。

(5)水的沸点为100℃,比乙酸异戊酯低42℃ ,但仍要先加入MgSO4后过滤再蒸馏,而不是直接蒸馏。结合题中信息分析,下列说法正确的是______(填字母)。
A.水可能会与乙酸异戊酯形成一种“恒沸溶液”(在溶液的某一组成时,在某温度下,混合液同时汽化或同时冷凝),不能进一步提纯,所以要先用MgSO4干燥
B.在加入MgSO4后如不先过滤就蒸馏,加热时硫酸镁的结晶水合物又会脱水
C.如不先用MgSO4吸收水分,蒸馏时水先被蒸出,浪费能源和延长蒸馏时间
D.本实验中要乙酸过量,而不是异戊醇过量,可能的原因是异戊醇比乙酸价格贵;另外异戊醇过量时,异戊醇与乙酸异戊酯沸点相近(小于30℃),蒸馏时完全分离困难
(6)将乙酸异戊酯中的异戊醇除去,是在哪个步骤中除去的______(填字母)。
A.在第一次水洗和后面的分液中除去的
B.在第二次用饱和碳酸氢钠溶液洗涤和后面的分液中除去的
C.在“过滤”中除去的
D.由于本实验中加入过量乙酸,异戊醇已经反应完全,所以不需除杂(异戊醇)了
E.在最后的“蒸馏”步骤中除去的
(7)产物乙酸异戊酯的产率是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com