
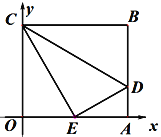
【题目】如图,矩形OABC中,OA、OC分别在平面直角坐标系x轴、y轴的正半轴上,点D在AB上,将△CDB沿着CD翻折,点B恰好落在OA的中点E处,若四边形OCDA的面积为![]() ,则直线ED的解析式为( )
,则直线ED的解析式为( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
【答案】C
【解析】
设OE=a,则EA=a,OA=2a.在Rt△COE中,求出CO.设BD=DE=x.在Rt△DAE中利用勾股定理求出BD、AD的长,利用四边形OCDA的面积求出a的值,进而得出点E、D的坐标,利用待定系数法即可解决问题.
设OE=a,则EA=a,OA=2a.
∵四边形OABC是矩形,∴CB=OA=2a,AB=OC,∠B=∠COA=∠BAO=90°.
∵△CDE≌△CDB,∴CE=CB=2a,BD=ED.
在Rt△COE中,∵OE=a,CE=2a,∴OC![]() ,∴AB=OC=
,∴AB=OC=![]() .设BD=DE=x.在Rt△DAE中,∵AD2+AE2=DE2,∴
.设BD=DE=x.在Rt△DAE中,∵AD2+AE2=DE2,∴![]() ,∴x=
,∴x=![]() ,∴AD=AB-BD=
,∴AD=AB-BD=![]() =
=![]() ,∴点E(a,0),点D(2a,
,∴点E(a,0),点D(2a,![]() ).
).
∵四边形OCDA的面积=![]() (AD+OC)OA=
(AD+OC)OA=![]() ,∴
,∴![]() ,解得:a=±3(负数舍去),∴a=3.∴点E(3,0),点D(6,
,解得:a=±3(负数舍去),∴a=3.∴点E(3,0),点D(6,![]() ).
).
设直线ED为y=kx+b,∴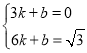 ,解得:
,解得: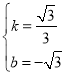 ,∴直线ED为:
,∴直线ED为:![]() .
.

故选C.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图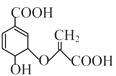 。下列关于分枝酸的叙述正确的是( )
。下列关于分枝酸的叙述正确的是( )
A.分子中含有3种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O–4e–=O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想合成具有以下结构的四种烃分子(键线式如图所示),下列有关说法错误的是( )
A.1mol甲分子内含有10mol共用电子对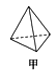
B.乙分子的一氯取代产物有1种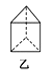
C.丙分子(立方烷)的三氯取代产物有2种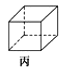
D.丁分子是不可能合成的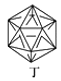
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气水蒸汽重整法是工业上生产氢气的重要方法,反应在 400℃以上进行。l 00kPa 时,在反应容器中通入甲烷与为水蒸汽体积比为1 : 5的混合气体,发生下表反应。
反应方程式 | 焓变△H(kJ/mol) | 600℃时的平衡常数 |
①CH4(g)+ H2O(g) | a | 0.6 |
②CH4(g)+ 2H2O(g) | +165.0 | b |
③CO(g)+ H2O(g) | -41.2 | 2.2 |
请回答下列下列问题:
(1)上表中数据 a=__________; b= ___________ 。
(2)对于反应②,既能加快反应又能提高CH4转化率的措施是_____________。
A.升温 B.加催化剂 C.加压 D.吸收CO2
(3)下列情况能说明容器中各反应均达到平衡的是___________。
A.体系中H2O与CH4物质的量之比不再变化
B.体系中H2的体积分数保持不变
C.生成n 个CO2的同时消耗2n个H2O
D. v正(CO)= v逆(H2)
(4)工业重整制氢中,因副反应产生碳会影响催化效率,需要避免温度过高以减少积碳。该体系中产生碳的反应方程式为 _______________。
(5)平衡时升温,CO含量将_________(选填“增大”或“减小”)。
(6)一定温度下 ,平衡时测得体系中 CO2和H2的物质的量浓度分别是0.75mo l/L、4.80mol/L , 则此时体系中CO 物质的量浓度是_______ mol/L。
(7)改变上述平衡体系的温度,平衡时H2O与CH4物质的量之比[![]() ]值也会随着改变,在图中画出其变化趋势。________________
]值也会随着改变,在图中画出其变化趋势。________________
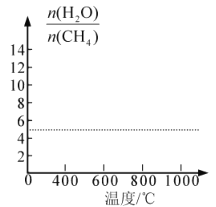
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氮及其化合物的化工生产中,对有关反应的反应原理进行研究有着重要意义。
(1)t℃时,关于N2、NH3的两个反应的信息如下表所示:
化学反应 | 正反应活化能 | 逆反应活化能 | t℃时平衡常数 |
N2(g)+O2(g)=2NO(g) △H>0 | a kJ/mol | b kJ/mol | K1 |
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H<0 | c kJ/mol | d kJ/mol | K2 |
请写出t℃时氨气被一氧化氮氧化生成无毒气体的热化学方程式:______________________,t℃时该反应的平衡常数为__________ (用K1和K2表示)。
(2)工业合成氨的原理为:N2(g)+3H2(g)![]() 2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。
2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。

①图甲中0~t1 min内,v(N2)=_____mol·L-1·min-1;b点的v(H2)正_____a点的v(H2)逆(填“大于”“小于”或“等于”)。
②己知某温度下该反应达平衡时各物质均为1 mol,容器体积为1L,保持温度和压强不变,又充入3 mol N2后,平衡________(填“向右移动”“向左移动”或“不移动”)。
(3)①科学家研究出以尿素为动力的燃料电池新技术。用这种电池可直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,写出负极电极反应式:________________________________________________。
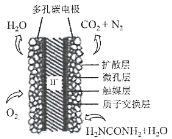
②理论上电池工作时,每消耗标准状况下2.24 L O2时,可产生的电量为________ (法拉第常数为96500C/ mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用甲苯制备一种芳香六元环酯(己)的方法如下:
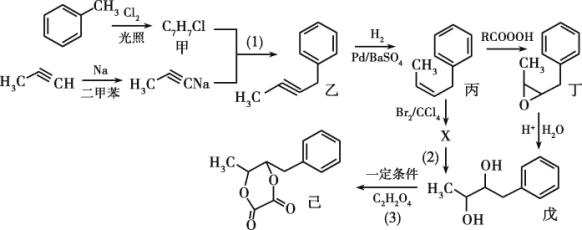
回答下列问题:
(1)写出物质丁的分子式_______,1mol丁完全燃烧需要氧气的物质的量为_______。
(2)物质甲的官能团名称为________。物质丙分子中共面的原子个数最多为_______。
(3)反应(3)的反应类型是_____,写出反应(1)的化学方程式_______。
(4)物质X的结构简式为______。
(5)物质丁的同分异构体较多,满足下列条件的物质丁的同分异构体数目是______,其中核磁共振氢谱有5组吸收峰,且峰面积之比为6:2:2:1:1的结构简式为______。
①能发生银镜反应 ②苯环上只有两个对位取代基
(6)写出以CH3CH=CH2为原料合成2-羟基丙酸(![]() )的合成路线(其他无机试剂任选)______。
)的合成路线(其他无机试剂任选)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某单烯烃A(C8H16)可以发生如下图示的转化,回答下列问题:

已知: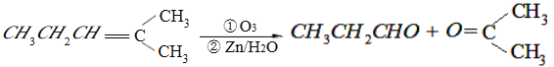
(1)B的分子式为___________________,D中含有官能团的名称___________________。
(2)B无银镜反应, D在浓硫酸存在下加热可得到能使溴水褪色且只有一种结构的物质E(不考虑立体异构),请写出E的结构简式____________________________________,D→E的反应类型___________________________。
(3)写出C→F的化学方程式_________________________________。
(4)H的同分异构体中,满足下列要求的结构一共有____________种(不考虑立体异构,包括H本身)
①属于酯类;②酸性条件下水解能得到相对分子质量为74的有机物
(5)已知: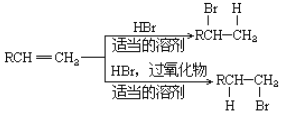 。
。
请写出由C制备2-丙醇的合成路线_____________________(无机原料任选)。合成路线流程图示例如下:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常用的食品抗氧化剂BHT的合成方法如下图所示(假设原料均能恰好完全反应):

下列说法中不正确的是( )
A.方法一的原子利用率为100%
B.方法二属于取代反应
C.X与Y均能与![]() 、
、![]() 溶液、溴水发生反应
溶液、溴水发生反应
D.![]() 在稀
在稀![]() 条件下发生消去反应可生成
条件下发生消去反应可生成![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com