
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��OH- |
| B��Ag+ |
| C��Na+ |
| D��Ca2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������ѻ����ǻ�ѧ�仯 |
| B������ϩ��������ϩ����ά�ض��Ǻϳɸ߷��� |
| C������ͭ�����ᡢ�����ǵ���� |
| D�����ᡢƯ�ۡ����ȼ����ǻ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ʮ��������ѧ�����߶�̼�����������˹㷺������о���ȡ����һЩ��Ҫ�ɹ���
��ʮ��������ѧ�����߶�̼�����������˹㷺������о���ȡ����һЩ��Ҫ�ɹ���
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��-332 | B��-118 |
| C��+350 | D��+130 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ |
| A����λʱ��������2 mol O3��ͬʱ����3 mol O2 |
| B��O2����������0.3 mol?L-1?s-1��O3����������0.2 mol?L-1?s-1 |
| C�������ڣ�2������O3��O2Ũ����� |
| D��������ܶȲ��ڸı䣮 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ҵ�ϳɰ��ķ�Ӧ��������Ҫʹ�ô��� |
| B����ҵ��������Ĺ�����ʹ�ù���������������߶��������ת���� |
| C��Fe��SCN��3��Һ�м�����������KSCN����ɫ���� |
| D��ʵ�������ű���ʳ��ˮ�ķ����ռ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
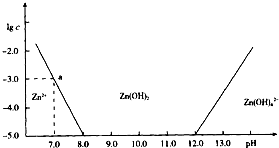 ��֪Zn2+��Ӧ�����ɰ�ɫ���������������ɫ�����ܽ�����Zn��OH��42-����ͼ����Zn2+����Һ����μ�������������Һ�ı仯����ʾ��ͼ��������Ϊ��Һ��pH��������ΪZn2+���ӻ�Zn��OH��42-�������ʵ���Ũ�ȵĶ���ֵ���ش��������⣮
��֪Zn2+��Ӧ�����ɰ�ɫ���������������ɫ�����ܽ�����Zn��OH��42-����ͼ����Zn2+����Һ����μ�������������Һ�ı仯����ʾ��ͼ��������Ϊ��Һ��pH��������ΪZn2+���ӻ�Zn��OH��42-�������ʵ���Ũ�ȵĶ���ֵ���ش��������⣮| c��HCl����mol?L-1�� | 0.50 | 1.00 | 2.04 | 2.90 | 4.02 | 5.16 | 5.78 |
| c��PbCl2����mol?L-1����10-3 | 5.10 | 4.91 | 5.21 | 5.90 | 7.48 | 10.81 | 14.01 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com