某研究小组用下列装置探究SO
2与酸性Fe(NO
3)
3溶液的反应.
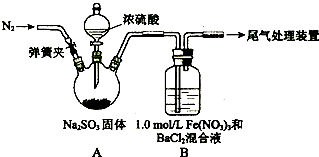
请回答:
(1)装置A中反应的化学方程式是
Na2SO3+H2S04(浓)=Na2S04+SO2↑+H2O
Na2SO3+H2S04(浓)=Na2S04+SO2↑+H2O
.
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是
打开弹簧夹,向装置中通入一段时间的N2,关闭弹簧夹
打开弹簧夹,向装置中通入一段时间的N2,关闭弹簧夹
.
(3)装置B中产生了白色沉淀,其成分是
BaS04
BaS04
,说明SO
2具有
还原性
还原性
性.
(4)甲乙两同学分析B中产生白色沉淀的原因:
甲同学:在酸性条件下SO
2与Fe
3+反应;
乙同学:在酸性条件下SO
2与NO
3-反应;
①按甲同学观点,装置B中反应的离子方程式是
SO2+2Fe3++Ba2++2H2O=BaSO4↓+2Fe2++4H+
SO2+2Fe3++Ba2++2H2O=BaSO4↓+2Fe2++4H+
,证明该观点应进一步确认生成的新物质,其实验操作及现象是
取少量B中溶液于试管中,加入适量氢氧化钠溶液,开始产生白色沉淀,白色沉淀迅速变成灰绿色,最终变为红褐色
取少量B中溶液于试管中,加入适量氢氧化钠溶液,开始产生白色沉淀,白色沉淀迅速变成灰绿色,最终变为红褐色
.
②按乙同学观点,只需将装置B中的Fe(NO
3)
3溶液替换为等体积的下列溶液,在相同条件下进行实验.应选择的试剂是(填序号)
c
c
.
a.0.1mol?L
-1稀硝酸
b.15mol?L
-1Fe(NO
3)
2溶液
C.6.0mol?L
-1NaNO
3和0.2mol?L
-1盐酸等体积混合的溶液.

 名师点拨卷系列答案
名师点拨卷系列答案