
(1)请把符合要求的化学方程式的字母填在下列空白处:
①既属于分解反应又是氧化还原反应的是____________________________
②属于分解反应,但不是氧化还原反应的是__________________________
③属于化合反应,但不是氧化还原反应的是__________________________
④不属于四种基本反应类型的氧化还原反应的是______________________
A.(NH4)2SO3  2NH3↑+H2O+SO2↑
2NH3↑+H2O+SO2↑
B.2KMnO4+16HCl(浓)= 2KCl+2MnCl2+ 5Cl2↑+ 8H2O
C.2C+SiO2 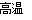 Si+2CO↑
Si+2CO↑
D.NH4NO3  N2O↑+2H2O
N2O↑+2H2O
E.Na2CO3+CO2+ H2O=2NaHCO3
F.MnO2+4HCl(浓)  MnCl2+Cl2↑+ 2H2O
MnCl2+Cl2↑+ 2H2O
(2)对于反应:K2Cr2O7+HCl → KCl+CrCl3+Cl2↑+H2O,回答下列问题:
①配平方程式,并用单线桥表示此反应转移的电子数目及方向
____K2Cr2O7+____HCl =____KCl +____ CrCl3+____Cl2↑+____H2O
②若反应中,发生氧化反应的HCl为1.2 mol,则被还原的K2Cr2O7 物质的量为___________mol。
(1) ① D ② A ③ E ④B、F
(2)1 14 2 2 3 7
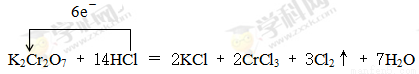 0.2
0.2
【解析】
试题分析:(1)A、反应(NH4)2SO3  2NH3↑+H2O+SO2↑属于分解反应,元素的化合价均不变,因此不是氧化还原反应;B、反应2KMnO4+16HCl(浓)= 2KCl+2MnCl2+ 5Cl2↑+ 8H2O中Mn和Cl元素的化合价分别由+7价降低到+2价、-1价升高到0价,因此是氧化还原反应,但不属于四种基本反应类型;C、反应2C+SiO2
2NH3↑+H2O+SO2↑属于分解反应,元素的化合价均不变,因此不是氧化还原反应;B、反应2KMnO4+16HCl(浓)= 2KCl+2MnCl2+ 5Cl2↑+ 8H2O中Mn和Cl元素的化合价分别由+7价降低到+2价、-1价升高到0价,因此是氧化还原反应,但不属于四种基本反应类型;C、反应2C+SiO2 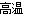 Si+2CO↑是置换反应,碳元素的化合价由0价升高到+2价,Si元素的化合价从+4价降低到0价,因此也是氧化还原反应;D、反应NH4NO3
Si+2CO↑是置换反应,碳元素的化合价由0价升高到+2价,Si元素的化合价从+4价降低到0价,因此也是氧化还原反应;D、反应NH4NO3  N2O↑+2H2O中NH4+中氮元素的化合价从-3价升高到+1价,NO3-中氮元素的化合价从+5价降低到+1价,因此是氧化还原反应,同时也是分解反应;E、反应Na2CO3+CO2+ H2O=2NaHCO3中元素的化合价均不变,不是氧化还原反应,属于化合反应;F、反应MnO2+4HCl(浓)
N2O↑+2H2O中NH4+中氮元素的化合价从-3价升高到+1价,NO3-中氮元素的化合价从+5价降低到+1价,因此是氧化还原反应,同时也是分解反应;E、反应Na2CO3+CO2+ H2O=2NaHCO3中元素的化合价均不变,不是氧化还原反应,属于化合反应;F、反应MnO2+4HCl(浓)  MnCl2+Cl2↑+ 2H2O中Mn元素的化合价从+4价降低到+2价,氯元素的化合价从-1价升高到0价,因此是氧化还原反应,但不属于四种基本反应类型。则
MnCl2+Cl2↑+ 2H2O中Mn元素的化合价从+4价降低到+2价,氯元素的化合价从-1价升高到0价,因此是氧化还原反应,但不属于四种基本反应类型。则
①既属于分解反应又是氧化还原反应的是D;
②属于分解反应,但不是氧化还原反应的是A;
③属于化合反应,但不是氧化还原反应的是E;
④不属于四种基本反应类型的氧化还原反应的是B、F。
(2)根据方程式K2Cr2O7+HCl → KCl+CrCl3+Cl2↑+H2O可知,反应中Cr元素的化合价从+6价降低到+3价,得到3个电子。氯元素的化合价从-1价升高到0价,因此根据电子得失守恒可知,氧化剂K2Cr2O7 与还原剂HCl的物质的量之比是1:6。根据原子守恒可知氯化钾和CrCl3前面的化学计量数分别是2和2,则氯化氢的计量数是14,所以氢气的计量数是7,则配平后的化学方程式为K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O,其中用单线桥可表示为
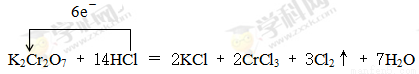 。
。
②若反应中,发生氧化反应的HCl为1.2 mol,则转移电子的物质的量是1.2mol。1molK2Cr2O7在反应中得到6mol电子,所以就电子得失守恒可知被还原的K2Cr2O7 物质的量为1.2mol÷6=0.2mol。
考点:考查氧化还原反应和四种基本反应类型的判断;氧化还原反应方程式配平和表示以及计算


科目:高中化学 来源:2016届黑龙江省高一上学期期末化学试卷(解析版) 题型:填空题
(1)某建筑材料,主要成分为铝硅酸盐,化学式是MgAl2H4Si4O14;化学式改写成氧化物形式为_________。该材料与酸或碱反应时可以看作各氧化物分别与酸、碱反应,则材料该与足量的氢氧化钠反应后过滤,滤渣主要是_______。
(2)除去FeCl2溶液中少量的FeCl3最好加入_________物质。
(3)鉴别Na2CO3和NaHCO3溶液可选用_________。(填序号)
①NaOH;②Ca(OH)2;③BaCl2;④K2SO4;⑤Ca(NO3)2
(4)某溶液中有①SO42―②Mg2+③Fe2+④Al3+四种离子,若向其中加入过量的氢氧化钠溶液,加热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
(5)将盛有18mLNO2和O2的混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积是( )
①1.2mL②2.4mL③3.6mL④5.2mL
A.①②B.①③C.②④D.①④
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
奥运五环代表着全世界五大洲的人民团结在一起。下列各项中的物质,能满足如图中阴影部分关系的是( )
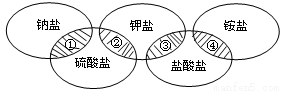
①②③④
ANaClK2SO4KCl(NH4)2SO4
BNa2SO4K2SO4KClNH4Cl
CNaClK2SO4KClNH4Cl
DNa2SO4K2SO4KCl(NH4)2SO4
查看答案和解析>>
科目:高中化学 来源:2016届陕西省安康市高一上学期期末质量检测化学试卷(解析版) 题型:选择题
下列离子方程式中,正确的是( )
A.氨水与硫酸铝溶液反应:Al3++3OH-=Al(OH)3↓
B.稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑
C.氢氧化铝与盐酸反应:Al(OH)3+3H+=Al3++3H2O
D.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag
查看答案和解析>>
科目:高中化学 来源:2016届陕西省安康市高一上学期期末质量检测化学试卷(解析版) 题型:选择题
某溶液中存在较多的H+、SO42-、NO3-,还可能大量存在的离子组是
A.Al3+、CO32-、Cl- B.Na+、NH4+、Cl-
C.Mg2+、Cl-、Fe2+ D.Mg2+、Ba2+、Br-
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高一上学期期中考试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.澄清的石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O
B.钠与水的反应Na+2H2O=Na++2OH -+ H2 ↑
C.硫酸氢钠溶液与少量氢氧化钡溶液混合:2H++SO42-+ Ba2++2OH-= BaSO4↓+2H2O
D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高一上学期期中考试化学试卷(解析版) 题型:选择题
(原创)下列叙述中正确的是
A.由HgCl2生成Hg2Cl2时,汞元素被还原
B.铁高温下与水蒸气反应,氧化产物为Fe2O3
C.阳离子只有氧化性,阴离子只有还原性
D.非标况下,1 mol H2的体积不可能为22.4 L
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省沈阳市高一上教学质量监测化学试卷(解析版) 题型:选择题
下列各组离子中,在碱性溶液中能共存,且加入硫酸过程中会产生气体和沉淀的是
A. K+ 、Na+、AlO2-、CO32- B.Na+、Cl-、SiO32-、K+
C. Na+、NO3-、AlO2-、K+ D.Na+、Cl-、HCO3-、Ba2+
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高一上学期12月月考化学试卷(解析版) 题型:选择题
NaOH、KOH等碱性溶液可以贮存在下列哪种试剂瓶中( )
A.具有玻璃塞的细口瓶 B.具有玻璃塞的广口瓶
C.带滴管的滴瓶 D.具有橡胶塞的细口瓶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com