
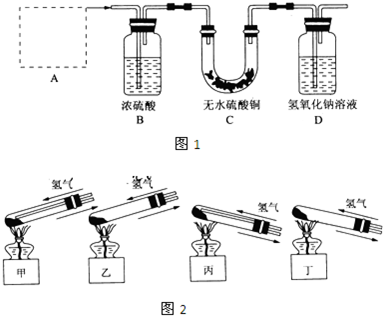
 实验室制氯气的实验装置图如下所示:
实验室制氯气的实验装置图如下所示:

 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案科目:高中化学 来源: 题型:
| A、0.5mol O3 和11.2L O2的体积一定相等 |
| B、5.6 gFe与足量的稀盐酸充分反应后,转移的电子数为0.2NA |
| C、标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| D、1L 0.1mol/L的醋酸溶液中H+数目为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.0mol/L盐酸 |
| B、自来水 |
| C、0.5mol/L硫酸 |
| D、1.0mol/L氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | 起始浓度/(mol?L-1) | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
| A、实验①反应后的溶液中:c(A-)>c(K+)>c(OH-)>c(H+) | ||
B、实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=
| ||
| C、实验②反应后的溶液中:c(A-)+c(HA)<0.1 mol/L | ||
| D、实验②反应后的溶液中:c(K+)+c(OH-)=c(H+)+c(A-) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2molC |
| B、2 molA、1 molB和1 molHe(不参加反应) |
| C、1 molB和1 molC |
| D、2 molA、2 molB和3 molC |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com