
| 选项 | 实验操作和现象 | 结论 |
| A | 向某无色溶液中滴加氯水和CCl4,振荡、静置,下层溶液显紫色 | 原溶液中有I- |
| B | 向稀HNO3中加入过量的Fe粉,充分反应后,滴入K3[Fe(CN)6]溶液,产生蓝色沉淀 | 稀HNO3将Fe氧化为Fe2+ |
| C | 常温下,测定盐酸和醋酸溶液的pH:盐酸pH小于醋酸pH | 证明相同条件下,在水中HCl电离程度大于CH3COOH |
| D | 室温下,用pH试纸测得:0.1mo/L Na2SO3溶液的pH约为10;0.1mol/LNaHSO3溶液的pH约为5. | HSO3-结合H+的能力比 SO32-的强 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.下层溶液显紫色,可知氯气氧化碘离子;
B.稀HNO3中加入过量的Fe粉,反应生成硝酸亚铁;
C.应测定等浓度的酸的pH;
D.由操作和现象可知,亚硫酸氢根离子电离大于其水解.
解答 解:A.下层溶液显紫色,可知氯气氧化碘离子,则原溶液中有I-,故A正确;
B.稀HNO3中加入过量的Fe粉,反应生成硝酸亚铁,因Fe与硝酸铁反应生成硝酸亚铁,结论不合理,故B错误;
C.应测定等浓度的酸的pH,操作与结论均不合理,故C错误;
D.由操作和现象可知,亚硫酸氢根离子电离大于其水解,则HSO3-结合H+的能力比SO32-的弱,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握离子的检验、物质的性质、pH与酸性比较、电离与水解、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液中CO32-水解:CO32-+2H2O?H2CO3+2OH- | |
| B. | Al溶于NaOH溶液:Al+2OH-═AlO2-+H2↑ | |
| C. | Fe3O4溶于稀HNO3:3Fe3O4+28H++NO3-═9Fe3++NO↑+14H2O | |
| D. | 向Ba(OH)2溶液中加少量稀H2SO4:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸 | 电离常数 | 弱酸 | 电离常数 |
| H2CO3 | Ka1=4.4×10-7 | H2C2O4 | Ka1=5.4×10-2 |
| Ka2=4.7×10-11 | Ka2=5.4×10-5 |
| A. | 2 | B. | 4 | C. | 6 | D. | 8 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时立即用沙子盖灭 | |
| B. | 制取有毒气体时需在通风橱中进行 | |
| C. | 将过期的化学药品直接倒入下水道 | |
| D. | 给试管中液体加热时试管口要避开人 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了使反应进行的更完全,可以使酸或碱适当过量 | |
| B. | 为了使反应均匀进行,可以向酸(碱)中分次加入碱(酸) | |
| C. | 因为中和热为一定值,所以实验结果与所用酸(碱)的用量 和种类均无关 | |
| D. | 测酸溶液的温度后,未冲洗温度计就直接测碱溶液的温度,会使中和热的数值偏大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+H++SO42-+NH4+=BaSO4↓+NH3•H2O+H2O | |
| B. | 将少量SO2气体通入NaClO溶液中:SO2+H2O+ClO-=SO42-+Cl-+2H+ | |
| C. | Na2CO3溶液中滴加几滴稀盐酸:CO32+H+=HCO3- | |
| D. | NaHCO3溶液中滴加少量澄清石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
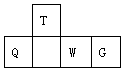 短周期元素T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角.下列判断正确的是( )
短周期元素T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角.下列判断正确的是( )| A. | 原子半径:W<T | |
| B. | 最简单气态氢化物的热稳定性:Q<T | |
| C. | 最高价氧化物对应水化物的酸性:W<Q | |
| D. | 简单离子的还原性:W<G |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com