
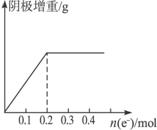
图4-15 通过电子的物质的量
A.Cu2+>X3+>H+ B.X3+>Cu2+>H+
C.Cu2+>H+>X3+ D.H+>Cu2+>X3+
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A.分解H2O2制O2,每生成1 mol O2转移4NA个电子
B.25 ℃时1 L pH=7的醋酸与醋酸钠的混合溶液中,一定有10-7NA个醋酸分子被电离
C.标准状况下,22 g C3H8与N2O混合气体所占体积约为11.2 L
D.用惰性电极电解1 L浓度均为2 mol·L-1的AgNO3与Cu(NO3)2混合溶液,当有0.2NA个电子发生转移时,阴极析出6.4 g金属
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)元素C在周期表中的位置是________________;
(2)化合物M中含有的化学键类型有__________;
(3)写出化合物Y与Z之间反应的离子方程式:_______________________________;
(4)以铂作电极,以Y溶液作为电解质溶液,A、C元素的单质分别在两电极上发生原电池反应,则正极上的电极反应式为________________;若以该电池作为电源,用惰性电极电解
查看答案和解析>>
科目:高中化学 来源:2013届浙江省金华一中高三12月月考化学试卷(带解析) 题型:单选题
NA为阿伏加德罗常数,下列叙述正确的是
A.0.5mol雄黄(As4S4,已知As和N同主族,结构如右图)含有NA个S—S键 |
| B.用惰性电极电解1 L浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 NA个电子转移时,阴极析出6.4g金属 |
| C.1mol过氧化氢分子中共用电子对数为3NA |
| D.0.1mol Na2CO3·10H2O在晶体中或溶液中,含有的CO32-离子均小于0.1 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com