
| A. | 78g Na2O2固体中,含有阴阳离子总数为4NA | |
| B. | 1mol Cl2与足量烧碱完全转移电子数为2NA | |
| C. | 1mol Be2+离子中含有的电子数为4NA | |
| D. | 16g臭氧(O3)含有NA个氧原子 |
分析 A.过氧化钠中含有的阴离子为 过氧根离子,78g过氧化钠的物质的量为1mol,含有2mol钠离子、1mol过氧根离子;
B. Cl2与足量烧碱完全转移电子数为NA;
C.1mol Be2+离子中含有的电子数为2NA
D.16g臭氧(O3)含有氧原子为$\frac{16g}{16g/mol}$×NA.
解答 解:A.78g过氧化钠的物质的量为1mol,1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总共含有3mol阴阳离子,含有的阴阳离子总数为3NA,故A错误;
B.1mol Cl2与足量烧碱完全转移电子数为NA,故B错误;
C.1mol Be2+离子中含有的电子数为2NA,故C错误;
D.16g臭氧(O3)含有氧原子为$\frac{16g}{16g/mol}$×NA=NA个,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,握好以物质的量为中心的各化学量与阿伏加德罗常数的关系.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
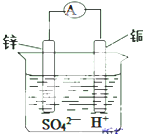 如图为某原电池示意图,请回答:
如图为某原电池示意图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 铊既能与强酸反应又能与强碱反应 | B. | 能生成+3价的化合物 | ||
| C. | Tl(OH)3与Al(OH)3一样是两性氢氧化物 | D. | Tl(OH)3的碱性比Al(OH)3强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18g D2O和18g H2O中含有的质子数均为10NA | |
| B. | 2L 0.5 mol•L-1亚硫酸溶液中含有的H+离子数为2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 标准状况下,2.24L Cl2与过量的稀FeI2溶液反应,转移电子总数为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com