
分析 (1)该核素的质量数为10+8=18;
(2)第三周期ⅥA族元素为S,最高正价为+6价;
(3)地壳中最多的元素是O(氧)其次依次是Si,Al,Fe;
(4)H2O分子具有10个电子,以此来解答.
解答 解:(1)含有8个质子,应为O元素,质子数为10+8=18,则可表示为188O,故答案为:188O;
(2)第三周期ⅥA族元素为S,最高正价为+6价,其最高价氧化物的水化物的化学式为H2SO4,故答案为:H2SO4;
(3)第三周期IIIA族是铝,是地壳中含量最多的金属元素,故答案为:三;IIIA;
(4)H2O分子具有10个电子,与H2O分子具有相同电子数的分子有Ne、HF、NH3、CH4,故答案为:Ne;HF.
点评 本题考查较综合,涉及化学用语及元素在周期表的位置、元素性质等,为高频考点,注意元素的位置、性质的应用即可解答,注重基础知识的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | OH-、H2O、F- | B. | Na+、NH4+、H3O+ | C. | H3O+、NH4+、NH2- | D. | Cl-、K+、H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有④ | B. | ①和③ | C. | ①②④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(NH4+):③>② | |
| B. | Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s)?Mg2+(aq)+2OH-(aq)右移 | |
| C. | pH:③>②>① | |
| D. | 将等体积的①和③混合,所得溶液中 c(Cl-)+c(CH3COO-)=c(NH4+)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将水加热,KW增大,pH不变 | |
| B. | 向水中加入少量的NaOH固体,平衡逆向移动,c(OH-)降低 | |
| C. | 向水中加入少量的NH4Cl固体,平衡逆向移动,溶液呈碱性 | |
| D. | 向0.1mol/L的醋酸溶液中加入一定量的醋酸钠晶体,溶液中的c(OH-)增大,KW不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数35、中子数45的溴原子:${\;}_{35}^{80}$Br | |
| B. | CH4的球棍模型示意图为 | |
| C. | 乙烯的结构简式:CH2CH2 | |
| D. | H216O、D216O、H218O、D218O互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
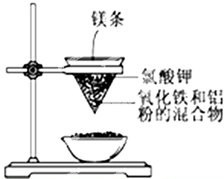
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
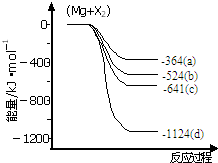 镁化合物具有广泛用途,请回答有关镁的下列问题:
镁化合物具有广泛用途,请回答有关镁的下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-389.9kJ•mol-1 | |
| B. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+2599.2kJ•mol-1 | |
| C. | C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(l)△H=-1299.6kJ•mol-1 | |
| D. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-1299.6kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com