
���� ��1���������̡�������ˮӦ������ѧʽ���Ȼ�����������ʽ���ݴ�д�����ӷ���ʽ��
��2�����ݷ���ʽMnO2+4HCl��Ũ��$\frac{\underline{\;����\;}}{\;}$MnCl2+Cl2��+2H2O����Ӧ��ÿ����1mol��������2mol�Ȼ����е��ȴ�-1������Ϊ�����е�0�۵��ȣ�ת��2mol���ӣ��ݴ˽��
��� �⣺��1������������Ũ���ᷴӦ���ӷ���ʽ��MnO2+2Cl-+4H+ $\frac{\underline{\;����\;}}{\;}$Mn2++Cl2��+2H2O��
�ʴ�Ϊ��MnO2+2Cl-+4H+ $\frac{\underline{\;����\;}}{\;}$Mn2++Cl2��+2H2O��
��2�����ݷ���ʽMnO2+4HCl��Ũ��$\frac{\underline{\;����\;}}{\;}$MnCl2+Cl2��+2H2O����Ӧ��ÿ����1mol��������2mol�Ȼ����е��ȴ�-1������Ϊ�����е�0�۵��ȣ�ת��2mol���ӣ������ɱ�״������11.2L���������ʵ���Ϊ$\frac{11.2L}{22.4L/mol}$=0.5mol��ת�Ƶ�����Ϊ1mol������Ϊ6.02��1023��NA��
�ʴ�Ϊ��6.02��1023��NA��
���� ���⿼�������ӷ���ʽ����д��������ԭ��Ӧ����ת����Ŀ���㣬��ȷ���ӷ���ʽ��д�����ǽ���ؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
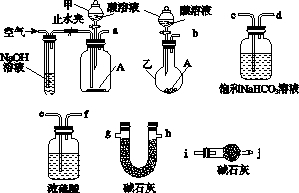 ��ʽ̼����A������θҩ������ɿɱ�ʾΪAl2Mg6��OH��x��CO3��y•zH2O��ijУ��ѧ��ȤС�����ⶨ�仯ѧʽ��ʵ��������£�
��ʽ̼����A������θҩ������ɿɱ�ʾΪAl2Mg6��OH��x��CO3��y•zH2O��ijУ��ѧ��ȤС�����ⶨ�仯ѧʽ��ʵ��������£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 9�� | B�� | 10�� | C�� | 11�� | D�� | 12�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
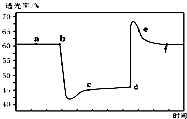 ��֪��Ӧ��2NO2��g��+4CO��g��?N2��g��+4CO2��g����H��0����һ������NO2��CO����װ�д�����ע�����к��ڣ���ͼ���������ѹ��ע�����Ĺ���������������ʱ��ı仯��������ɫԽ�����ԽС��������˵������ȷ���ǣ�������
��֪��Ӧ��2NO2��g��+4CO��g��?N2��g��+4CO2��g����H��0����һ������NO2��CO����װ�д�����ע�����к��ڣ���ͼ���������ѹ��ע�����Ĺ���������������ʱ��ı仯��������ɫԽ�����ԽС��������˵������ȷ���ǣ�������| A�� | b��IJ����ǿ���ѹ��ע���� | |
| B�� | c����a����ȣ�c��NO2����c��N2�������� | |
| C�� | e�㣺�ԣ��������ԣ��棩 | |
| D�� | ��������ϵ�¶ȱ仯����û��������ʧ����ƽ�ⳣ��K��c����K��f�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ȶ��ԣ�Na2CO3��NaHCO3 | B�� | �ǽ����ԣ�Cl��Br | ||
| C�� | ���ԣ�NaOH��Mg��OH��2 | D�� | ���ԣ�H2SO4��H3PO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
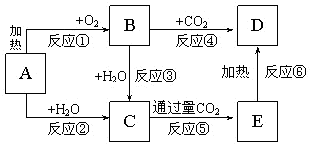 ��ͼ��ʾ�У�AΪһ�ֳ����ĵ��ʣ�B��C��D��E�Ǻ�AԪ�صij�����������ǵ���ɫ��Ӧ��Ϊ��ɫ��
��ͼ��ʾ�У�AΪһ�ֳ����ĵ��ʣ�B��C��D��E�Ǻ�AԪ�صij�����������ǵ���ɫ��Ӧ��Ϊ��ɫ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.8molCO2 | B�� | ��״����22.4LO2 | ||
| C�� | 3.6gˮ | D�� | ��NA��NH3���ӵİ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com