
œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «(ΓΓΓΓ)
A. Ι”ΟΩ…‘Ό…ζΉ ‘¥ΓΔ”Ο≥§ΝΌΫγΕΰ―θΜ·ΧΦΧφ¥ζ”–Μζ»ήΦΝΓΔΉΔ÷Ί‘≠Ή”ΒΡΨ≠ΦΟ–‘ΓΔ≤…”ΟΒΆΡήΚΡ…ζ≤ζΙΛ“’ΕΦΖϊΚœ¬Χ…ΪΜ·―ßΒΡΥΦœκ
B.Α±ΜυΥα «»ΥΧε±Ί–ηΒΡ”Σ―χΈο÷ ,ΤδΨßΧε÷ς“Σ“‘ΡΎ―Έ–Έ Ϋ¥φ‘Ύ,ΒςΫΎ»ή“ΚΒΡpHΩ…ΗΡ±δΥϋΒΡ»ήΫβΕ»
C. ·”ΆΝ―ΫβΓΔΟΚΒΡΤχΜ·ΓΔœπΫΚάœΜ·ΓΔΚΘΥ°÷ΤΟΨΓΔ¥ΩΦνΨßΧεΖγΜ·ΓΔœΥΈ§ΥΊ÷ΤΜπΟόΒ»Ιΐ≥Χ÷–ΕΦΑϋΚ§Μ·―ß±δΜ·
D.PM2.5 «÷Η¥σΤχ÷–÷±ΨΕ–Γ”ΎΜρΒ»”Ύ2.5ΈΔΟΉΒΡΩ≈ΝΘΈο,“≤≥ΤΈΣΓΑœΗΩ≈ΝΘΈοΓ±,PM2.5‘ΎΩ’Τχ÷–÷Μ–Έ≥…Τχ»ήΫΚ
 ‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗ
‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ2014ΗΏΩΦΜ·―ßΟϊ Π―Γ‘ώΧβΉ®ΝΖ Μ·―ß”κSTSEΝΖœΑΨμΘ®ΫβΈωΑφΘ© Χβ–ΆΘΚ―Γ‘ώΧβ
Μ·―ß”κΩΤ―ßΓΔΦΦ θΓΔ…γΜαΓΔΜΖΨ≥Οή«–œύΙΊΓΘœ¬Ν–”–ΙΊΥΒΖ®÷–¥μΈσΒΡ «(ΓΓΓΓ)
A.ΆΤΙψ Ι”ΟΖγΡήΓΔΧΪ―τΡήΒ»–¬Ρή‘¥ΡήΙΜΦθ…ΌΈ¬ “ΤχΧεΒΡ≈≈Ζ≈
B.≤ΆΉά…œΒΡ¥…≈Χ «ΙηΥα―Έ÷ΤΤΖ
C.÷ΤΉςΚΫΧλΖΰΒΡΨέθΞœΥΈ§ΚΆ”Ο”ΎΙβά¬Ά®–≈ΒΡΙβΒΦœΥΈ§ΕΦ «–¬–ΆΈόΜζΖ«Ϋπ τ≤ΡΝœ
D.”ΟΓΑ84Γ±œϊΕΨ“Κά¥…±ΥάH1N1ΝςΗ–≤ΓΕΨ «“ρΈΣ≤ΓΕΨΒΑΑΉ÷ ±δ–‘
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ2014ΗΏΩΦΜ·―ßΟϊ ΠΉέΚœΧβΉ®ΝΖ ”–ΜζΚœ≥…”κΆΤΕœΝΖœΑΨμΘ®ΫβΈωΑφΘ© Χβ–ΆΘΚΧνΩ’Χβ
“―÷Σ:ΔσΡή”κNaHCO3»ή“ΚΖ¥”Π,ΔσΚΆΔτΒΡœύΕ‘Ζ÷Ή”÷ ΝΩœύΒ»«“Δτ¥ΏΜ·―θΜ·ΒΡ≤ζΈο≤ΜΡήΖΔ…ζ“χΨΒΖ¥”ΠΓΘ
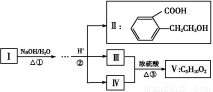
(1)Μ·ΚœΈοΔσ÷–ΙΌΡήΆ≈ΒΡΟϊ≥Τ «ΓΓΓΓΓΓΓΓ;Δρ≤ΜΡήΖΔ…ζΒΡΖ¥”Π «ΓΓΓΓΓΓΓΓΓΘ
A.Φ”≥…Ζ¥”ΠB.œϊ»ΞΖ¥”Π
C.θΞΜ·Ζ¥”ΠD.Υ°ΫβΖ¥”Π
(2)Ζ¥”ΠΔέΒΡάύ–ΆΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
(3)ΔθΒΡΫαΙΙΦρ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓ,ΔώΒΡΫαΙΙΦρ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΘ
(4)Μ·ΚœΈοΔω «ΔρΒΡΆ§Ζ÷“λΙΙΧε,Ά§ ±ΖϊΚœœ¬Ν–ΥΡ÷÷ΧθΦΰ,‘ρΔωΒΡΫαΙΙΦρ ΫΈΣΓΓΓΓΓΓΓΓΓΘ
A.±ΫΜΖ…œ”–ΝΫΗω»Γ¥ζΜυ«“±ΫΜΖ…œΒΡ“Μ¬»¥ζΈο”–2÷÷
B.Ρή”κFeCl3»ή“ΚΖΔ…ζœ‘…ΪΖ¥”Π
C.ΡήΖΔ…ζΥ°ΫβΖ¥”Π
D.ΚΥ¥≈Ι≤’ώ«βΤΉ”–6ΗωΖε,ΖεΒΡΟφΜΐ÷°±»ΈΣ1ΓΟ2ΓΟ2ΓΟ2ΓΟ2ΓΟ1
(5)Μ·ΚœΈοΔρΖΔ…ζΖ÷Ή”ΡΎ≥…ΜΖΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ ΓΓΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ2014ΗΏΩΦΜ·―ßΟϊ Π÷Σ ΕΒψΨΪ±ύ ―Γ–ό3Έο÷ ΫαΙΙ”κ–‘÷ ΝΖœΑΨμΘ®ΫβΈωΑφΘ© Χβ–ΆΘΚΧνΩ’Χβ
‘ΣΥΊHΓΔCΓΔNΓΔOΓΔFΕΦ «÷Ί“ΣΒΡΖ«Ϋπ τ‘ΣΥΊ,FeΓΔCu «”Π”ΟΖ«≥ΘΙψΖΚΒΡΫπ τΓΘ
(1)Fe‘ΣΥΊΜυΧ§‘≠Ή”ΒΡΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣΓΓ ΓΘ
(2)CΓΔH‘ΣΥΊ–Έ≥…ΒΡΜ·ΚœΈοΖ÷Ή”÷–Ι≤”–16ΗωΒγΉ”,ΗΟΖ÷Ή”÷–Π“Φϋ”κΠ–ΦϋΒΡΗω ΐ±»ΈΣΓΓΓΓ
(3)CΓΔNΓΔO»ΐ÷÷‘ΣΥΊΒΡΒΎ“ΜΒγάκΡή”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣ(”Ο‘ΣΥΊΖϊΚ≈±μ Ψ)ΓΓ
(4)‘Ύ≤βΕ®HFΒΡœύΕ‘Ζ÷Ή”÷ ΝΩ ±, Β―ι≤βΒΟ÷Β“ΜΑψΗΏ”Ύάμ¬έ÷Β,Τδ÷ς“Σ‘≠“ρ «
(5)CΓΔNΝΫ‘ΣΥΊ–Έ≥…ΒΡΜ·ΚœΈοC3N4–Έ≥…ΒΡ‘≠Ή”ΨßΧε,ΫαΙΙάύΥΤΫπΗ’ ·,…θ÷Ν”≤Ε»≥§ΙΐΫπΗ’ ·,Τδ‘≠“ρ « ΓΓ
(6)»γΆΦΈΣ ·ΡΪΨßΑϊΫαΙΙ Ψ“βΆΦ,ΗΟΨßΑϊ÷–Κ§”–ΧΦ‘≠Ή”ΒΡΗω ΐΈΣΓΓΓΓΓΓ ΓΓ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ2014ΗΏΩΦΜ·―ßΟϊ Π÷Σ ΕΒψΨΪ±ύ ―Γ–ό3Έο÷ ΫαΙΙ”κ–‘÷ ΝΖœΑΨμΘ®ΫβΈωΑφΘ© Χβ–ΆΘΚ―Γ‘ώΧβ
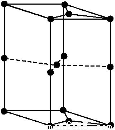
Π“ΦϋΩ…”…ΝΫΗω‘≠Ή”ΒΡsΙλΒάΓΔ“ΜΗω‘≠Ή”ΒΡsΙλΒάΚΆΝμ“ΜΗω‘≠Ή”ΒΡpΙλΒάΜρΝΫΗω‘≠Ή”ΒΡpΙλΒά“‘ΓΑΆΖ≈ωΆΖΓ±ΖΫ Ϋ÷ΊΒΰΙΙΫ®Εχ≥…ΓΘ‘ρœ¬Ν–Ζ÷Ή”÷–ΒΡΠ“Φϋ «”…ΝΫΗω‘≠Ή”ΒΡsΙλΒά“‘ΓΑΆΖ≈ωΆΖΓ±ΖΫ Ϋ÷ΊΒΰΙΙΫ®Εχ≥…ΒΡ «(ΓΓΓΓ)
A.H2 B.HClC.Cl2 D.F2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ2014ΗΏΩΦΜ·―ßΟϊ Π÷Σ ΕΒψΨΪ±ύ ―Γ–ό2Μ·―ß”κΦΦ θΝΖœΑΨμΘ®ΫβΈωΑφΘ© Χβ–ΆΘΚΧνΩ’Χβ
Έ“ΙζΜ·―ßΦ“ΚνΒ¬ΑώΗΡΗοΙζΆβΒΡ¥ΩΦν…ζ≤ζΙΛ“’,…ζ≤ζΝς≥ΧΩ…Φρ“Σ±μ Ψ»γΆΦ
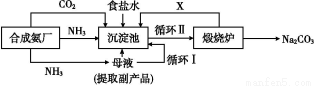
(1)…œ ω…ζ≤ζ¥ΩΦνΒΡΖΫΖ®≥ΤΓΓΓΓΓΓΓΓ,Η±≤ζΤΖΒΡ“Μ÷÷”ΟΆΨΈΣΓΓΓΓΓΓΓΓΓΘ
(2)≥ΝΒμ≥Ί÷–ΖΔ…ζΒΡΜ·―ßΖ¥”ΠΖΫ≥Χ Ϋ « ΓΓΓΘ
(3)–¥≥ω…œ ωΝς≥Χ÷–XΈο÷ ΒΡΖ÷Ή” ΫΓΓ ΓΘ
(4) Ι‘≠Νœ¬»Μ·ΡΤΒΡάϊ”Ο¬ ¥”70%ΧαΗΏΒΫ90%“‘…œ,÷ς“Σ «…ηΦΤΝΥΓΓΓΓΓΓΓΓ(Χν…œ ωΝς≥Χ÷–ΒΡ±ύΚ≈)ΒΡ―≠ΜΖΓΘ¥”≥ΝΒμ≥Ί÷–»Γ≥ω≥ΝΒμΒΡ≤ΌΉς «ΓΓΓΓΓΓΓΓ ΓΘ
(5)ΈΣΦλ―ι≤ζΤΖΧΦΥαΡΤ÷– «ΖώΚ§”–¬»Μ·ΡΤ,Ω…»Γ…ΌΝΩ ‘―υ»ή”ΎΥ°Κσ,‘ΌΒΈΦ”ΓΓΓΓΓΓΓΓΓΘ
(6)œρΡΗ“Κ÷–Ά®Α±Τχ,Φ”»κœΗ–Γ ≥―ΈΩ≈ΝΘ,ά以Έω≥ωΗ±≤ζΤΖ,Ά®Α±ΤχΒΡΉς”Ο”–ΓΓΓΓΓΓΓΓΓΘ
a.‘ω¥σNH4+ΒΡ≈®Ε», ΙNH4ClΗϋΕύΒΊΈω≥ω
b. ΙNaHCO3ΗϋΕύΒΊΈω≥ω
c. ΙNaHCO3ΉΣΜ·ΈΣNa2CO3,ΧαΗΏΈω≥ωΒΡNH4Cl¥ΩΕ»
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ2014ΗΏΩΦΜ·―ßΟϊ Π÷Σ ΕΒψΨΪ±ύ Ή®Χβ9»ή“Κ÷–ΒΡΒγάκΤΫΚβΝΖœΑΨμΘ®ΫβΈωΑφΘ© Χβ–ΆΘΚΧνΩ’Χβ
25 Γφ ±,ΒγάκΤΫΚβ≥Θ ΐ:
»θΥαΒΡΜ·―ß Ϋ | CH3COOH | HClO | H2CO3 |
ΒγάκΤΫΚβ≥Θ ΐ(25 Γφ) | 1.8ΓΝ10-5 | 3.0ΓΝ | K1=4.3ΓΝ10-7 K2=5.6ΓΝ10-11 |
ΜΊ¥πœ¬Ν–Έ Χβ:
(1)Έο÷ ΒΡΝΩ≈®Ε»ΈΣ0.1 mol/LΒΡœ¬Ν–ΥΡ÷÷Έο÷ :
a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3;
pH”…¥σΒΫ–ΓΒΡΥ≥–ρ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ(Χν±ύΚ≈)ΓΘ
(2)≥ΘΈ¬œ¬0.1 mol/LΒΡCH3COOH»ή“ΚΦ”Υ°œΓ ΆΙΐ≥Χ÷–,œ¬Ν–±μ¥ο ΫΒΡ ΐΨί“ΜΕ®±δ–ΓΒΡ «ΓΓΓΓΓΓΓΓ;
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)ΓΛc(OH-) D.c(OH-)/c(H+)
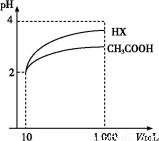
(3)ΧεΜΐΈΣ10 mL pH=2ΒΡ¥ΉΥα»ή“Κ”κ“Μ‘ΣΥαHXΖ÷±πΦ”Υ°œΓ Ά÷Ν1 000 mL,œΓ ΆΙΐ≥ΧpH±δΜ·»γΆΦ,‘ρHXΒΡΒγάκΤΫΚβ≥Θ ΐΓΓΓΓΓΓΓΓ(ΧνΓΑ¥σ”ΎΓ±ΓΔΓΑΒ»”ΎΓ±ΜρΓΑ–Γ”ΎΓ±)¥ΉΥαΒΡΤΫΚβ≥Θ ΐ;άμ”… «ΓΓ ΓΓ,
œΓ ΆΚσ,HX»ή“Κ÷–Υ°Βγάκ≥ωά¥ΒΡc(H+)ΓΓΓΓΓΓΓΓ(ΧνΓΑ¥σ”ΎΓ±ΓΔΓΑΒ»”ΎΓ±ΜρΓΑ–Γ”ΎΓ±)¥ΉΥα»ή“Κ÷–Υ°Βγάκ≥ωά¥ΒΡc(H+),άμ”… «ΓΓ ;
(4)25 Γφ ±,CH3COOH”κCH3COONaΒΡΜλΚœ»ή“Κ,»τ≤βΒΟΜλΚœ“ΚpH=6,‘ρ»ή“Κ÷–c(CH3COO-)-c(Na+)=ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ(ΧνΉΦ»Ζ ΐ÷Β)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ2014ΗΏΩΦΜ·―ßΟϊ Π÷Σ ΕΒψΨΪ±ύ Ή®Χβ8Μ·―ßΖ¥”ΠΥΌ¬ ”κΜ·―ßΤΫΚβΝΖœΑΨμΘ®ΫβΈωΑφΘ© Χβ–ΆΘΚΧνΩ’Χβ
Υ°ΟΚΤχ «“Μ÷÷ΗΏ–ßΤχΧε»ΦΝœ,Τδ÷ς“Σ≥…Ζ÷ «COΚΆH2,Ω…”ΟΥ°’τΤχΆ®Ιΐ≥ψ»»ΒΡΧΦ÷ΤΒΟ:C (s)+H2O(g) CO (g)+H2 (g)ΓΓΠΛH=+131 kJΓΛmol-1
CO (g)+H2 (g)ΓΓΠΛH=+131 kJΓΛmol-1
(1)TΈ¬Ε»œ¬,ΥΡΗω»ίΤς÷–ΨυΫχ––Ή≈…œ ωΖ¥”Π,Ης»ίΤς÷–ΧΦΉψΝΩ,ΤδΥϊΈο÷ ΒΡΈο÷ ΒΡΝΩ≈®Ε»ΦΑ’ΐΓΔΡφΖ¥”ΠΥΌ¬ ΙΊœΒ»γœ¬±μΥυ ΨΓΘ«κΧν–¥±μ÷–œύ”ΠΒΡΩ’ΗώΓΘ
»ίΤς ±ύΚ≈ | c(H2O) /molΓΛL-1 | c(CO) /molΓΛL-1 | c(H2) /molΓΛL-1 | v’ΐΓΔvΡφ±»Ϋœ |
Δώ | 0.06 | 0.60 | 0.10 | v’ΐ=vΡφ |
Δρ | 0.06 | 0.50 | 0.40 | ΔΌ |
Δσ | 0.12 | 0.40 | 0.80 | v’ΐ<vΡφ |
Δτ | 0.12 | 0.30 | ΔΎ | v’ΐ=vΡφ |
ΔΌΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ,ΔΎΓΓ ΓΘ
‘ΎTΈ¬Ε»œ¬ΗΟΖ¥”ΠΒΡΜ·―ßΤΫΚβ≥Θ ΐΈΣΓΓΓΓΓΓ ΓΓΓΘ
(2)Νμ”–“ΜΗω»ίΜΐΩ…±δΒΡΟή±’»ίΤςΓΘΚψΈ¬Κψ―Ιœ¬,œρΤδ÷–Φ”»κ1.0 molΧΦΚΆ1.0 molΥ°’τΤχ (H2O),ΖΔ…ζ…œ ωΖ¥”Π,¥οΒΫΤΫΚβ ±,»ίΤςΒΡΧεΜΐ±δΈΣ‘≠ά¥ΒΡ1.25 ±ΕΓΘΤΫΚβ ±Υ°’τΤχΒΡΉΣΜ·¬ ΈΣΓΓΓΓΓΓΓΓ;œρΗΟ»ίΤς÷–≤Ι≥δa mol ΧΦ,Υ°’τΤχΒΡΉΣΜ·¬ ΫΪΓΓΓΓΓΓΓΓ (Χν ΓΑ‘ω¥σΓ±ΓΔΓΑΦθ–ΓΓ±ΜρΓΑ≤Μ±δΓ±)ΓΘ
(3)‘Ύ“ΜΕ®ΧθΦΰœ¬”ΟΥ°ΟΚΤχΡήΚœ≥…ΦΉ¥Φ:CO(g)+2H2(g)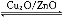 CH3OH(g)ΓΓΠΛH>0,ΗχΚœ≥…ΦΉ¥ΦΖ¥”ΠΧεœΒ÷–Ά®»κ…ΌΝΩCO‘ρΤΫΚβΓΓΓΓΓΓΓΓ “ΤΕ·,Φθ–Γ―Ι«Ω‘ρΤΫΚβΓΓΓΓΓΓΓΓ“ΤΕ·,ΫΒΒΆΈ¬Ε»‘ρΤΫΚβΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ“ΤΕ·(ΧνΓΑœρΉσΓ±ΓΔΓΑœρ”“Γ±ΜρΓΑ≤ΜΓ±)ΓΘ
CH3OH(g)ΓΓΠΛH>0,ΗχΚœ≥…ΦΉ¥ΦΖ¥”ΠΧεœΒ÷–Ά®»κ…ΌΝΩCO‘ρΤΫΚβΓΓΓΓΓΓΓΓ “ΤΕ·,Φθ–Γ―Ι«Ω‘ρΤΫΚβΓΓΓΓΓΓΓΓ“ΤΕ·,ΫΒΒΆΈ¬Ε»‘ρΤΫΚβΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ“ΤΕ·(ΧνΓΑœρΉσΓ±ΓΔΓΑœρ”“Γ±ΜρΓΑ≤ΜΓ±)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ2014ΗΏΩΦΜ·―ßΟϊ Π÷Σ ΕΒψΨΪ±ύ Ή®Χβ5Μ·―ßΡή”κ»»ΡήΝΖœΑΨμΘ®ΫβΈωΑφΘ© Χβ–ΆΘΚ―Γ‘ώΧβ
œ¬Ν–Έο÷ ΦδΒΡΖ¥”Π,ΤδΡήΝΩ±δΜ·ΖϊΚœ»γΆΦΒΡ «(ΓΓΓΓ)

A.Χζ”κΝρΖέ‘ΎΦ”»»ΧθΦΰœ¬ΒΡΖ¥”Π
B.ΉΤ»»ΒΡΧΦ”κΕΰ―θΜ·ΧΦΖ¥”Π
C.Ba(OH)2ΓΛ8H2OΨßΧεΚΆNH4ClΨßΧεΜλΚœ
D.ΧΦΥαΗΤΒΡΖ÷Ϋβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com