
| A. | 甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使酸性高锰酸钾溶液褪色 | |
| B. | 乙基对羟基的影响,使羟基的活性变弱,电离H+的能力不及H2O | |
| C. | 相等物质的量的甘油和乙醇分别与足量金属钠反应,甘油产生的H2多 | |
| D. | 苯酚中的羟基氢能与NaOH溶液反应,而醇羟基氢不能与NaOH溶液反应 |
分析 A、苯、甲烷都不能使酸性高锰酸钾溶液褪色,甲苯可以,说明苯环对甲基的影响;
B、烷基的斥电子性能,使得烷氧基中氧原子上的电子云密度增加,从而降低了醇的离解倾向;
C、羟基与钠反应生成氢气,甘油中羟基数目比乙醇中多;
D、苯环对酚羟基影响的结果是酚羟基具有酸性.
解答 解:A、甲苯能使酸性高锰酸钾溶液褪色而甲烷不能,说明H原子与苯基对甲基的影响不同,甲苯能使高锰酸钾酸性溶液褪色,说明苯环的影响使侧链甲基易被氧化,故A不选;
B、烷基的斥电子性能,使得烷氧基中氧原子上的电子云密度增加,从而降低了醇的离解倾向,所以乙基对羟基的影响,使羟基的活性变弱,提供H+的能力不及H2O,故B不选;
C、羟基与钠反应生成氢气,甘油中羟基数目比乙醇中多,由官能团数目不同导致,不能说明,故C选;
D、在苯酚中,由于苯环对-OH的影响,酚羟基具有酸性,对比乙醇,虽含有-OH,但不具有酸性,能说明上述观点,故D不选.
故选C.
点评 本题考查有机物的结构和性质,题目难度不大,注意有机物的原子团之间相互影响的特点.


科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①②③④ | C. | ③④⑤ | D. | 全部都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1-丁烯和环己烷 | B. | 1-庚烯和3-甲基-1-丁烯 | ||
| C. | 1-氯丙烷和2-氯丙烷 | D. | 甲苯和乙苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CHCl3是三角锥形 | |
| B. | 凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键 | |
| C. | AB2是V形,其A可能为sp2杂化 | |
| D. | NH4+是平面四边形结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
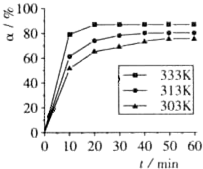
| A. | △H<0 | B. | △H>0 | C. | △H=0 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
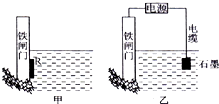 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的$\frac{1}{4}$
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的$\frac{1}{4}$查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 容器内压强 | B. | 平均相对分子质量 | ||
| C. | 各组分浓度 | D. | 混合气体的颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(R2-)+c(OH-)=c(Na+)+c(H+) | B. | c(R2-)>c(Na+)>c(H+)=c(OH-) | ||
| C. | 2c(R2-)+c(HR-)=c(Na+) | D. | 混合后溶液的体积为2aL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com