

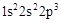 ,A为N元素;A与B形成的一种化合物常温下是红棕色气体,该气体为NO2,则B是O元素;根据E原子核外的M层中只有两对成对电子,其电子排布式为
,A为N元素;A与B形成的一种化合物常温下是红棕色气体,该气体为NO2,则B是O元素;根据E原子核外的M层中只有两对成对电子,其电子排布式为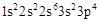 ,则E为S元素;由化合物C2E的晶体为离子晶体,原子序数依次增大,则可知C为Na元素;根据D单质的熔点在同周期单质中最高,可知D是Si元素;根据F原子核外最外层电子数与C相同,其余各层均充满,则F为29号元素,F是Cu元素;据此回答。
,则E为S元素;由化合物C2E的晶体为离子晶体,原子序数依次增大,则可知C为Na元素;根据D单质的熔点在同周期单质中最高,可知D是Si元素;根据F原子核外最外层电子数与C相同,其余各层均充满,则F为29号元素,F是Cu元素;据此回答。 =4,含有Cu:4,故该晶胞化学式为CuO。
=4,含有Cu:4,故该晶胞化学式为CuO。

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1 817 | 2 745 | 11 578 |
| Y | 738 | 1 451 | 7 733 | 10 540 |
| Z | 496 | 4 562 | 6 912 | 9 543 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
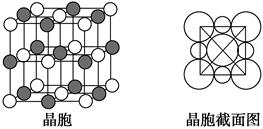
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
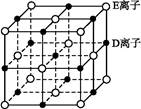
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由二氧化碳合成金刚石是化学变化 | B.金刚石是碳的一种同位素 |
| C.钠被氧化最终生成碳酸钠 | D.金刚石中只含有非极性共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com