
【题目】高炉炼铁中发生的基本反应之一:FeO(s)+CO(g)Fe(s)+CO2(g)不能自发进行,已知正反应吸热.
(l)关于化学反应方向的判据△H﹣T△S<0,反应___________(填能自发、不能自发)
答案:不能自发
(1)该反应中平衡常数的表达式 K═温度升高,化学平衡移动后达到新的平衡,平衡常数K值 . (均填增大、减小或不变)
(2)1100℃时测得高炉中 c(CO2)=0.025mol/L,c(CO)═0.lmol/L,已知1100℃时平衡常数K=0.263.在这种情况下该反应是否处于平衡状态(填是或否),此时化学反应速率是v(正)v(逆)(填=、>或<).
(3)反应达到平衡后,若保持容器体积不变时,再通入一定量的CO,则CO的转化率将(填“增大”、“减小”、“不变”).
【答案】
(1)![]() ;增大
;增大
(2) 否;>
(3)不变
【解析】(1)反应FeO(s)+CO(g)Fe(s)+CO2(g),△S=0,△H>0,△H﹣T△S>0,反应不能自发进行;(2)可逆反应FeO(s)+CO (g)Fe(s)+CO2(g)的平衡常数表达式k= ![]() ;该反应正反应是吸热反应,温度升高平衡向正反应方向移动,CO2的物质的量增大、CO的物质的量减小,故到达新平衡是CO2与CO的体积之比增大;(3)此时浓度商Qc= 0.25,小于平衡常数0.263,故反应不是平衡状态,反应向正反应进行,v(正)>v(逆);>;(4)若保持容器体积不变时,再通入一定量的CO,相当于增大压强,化学平衡不移动,CO的转化率不变;
;该反应正反应是吸热反应,温度升高平衡向正反应方向移动,CO2的物质的量增大、CO的物质的量减小,故到达新平衡是CO2与CO的体积之比增大;(3)此时浓度商Qc= 0.25,小于平衡常数0.263,故反应不是平衡状态,反应向正反应进行,v(正)>v(逆);>;(4)若保持容器体积不变时,再通入一定量的CO,相当于增大压强,化学平衡不移动,CO的转化率不变;
【考点精析】解答此题的关键在于理解化学平衡常数的含义的相关知识,掌握指在一定条件下的可逆反应里,正反应和逆反应的速率相等,反应混合物中各组分的浓度不变的状态,以及对化学平衡状态的判断的理解,了解状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等.


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】
(1)日本大地震和海啸造成核电站爆炸,发生核泄漏,使碘131、铯137等放射性核素扩散到空气和海洋中。碘131的原子核中,中子数与质子数之差为 , 铯元素位于元素周期表中第周期族。
(2)下列原子: ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 中共有种元素,种核素。
中共有种元素,种核素。
(3)在H3O+中,质子数、中子数、电子数之比为;在NH3D+中,质子数、中子数、电子数之比为。
(4)填写下列表格(Z——质子数,N——中子数,A——质量数):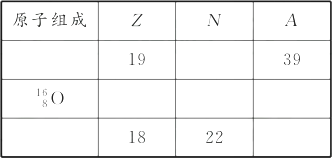
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应①:CO(g)+CuO(s) CO2(g)+Cu(s)和反应②:H2(g)+CuO(s) Cu(s)+H2O(g)在相同的温度下的平衡常数分别为K1和K2 , 该温度下反应③:CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是( )
A.反应①的平衡常数 ![]()
B.反应③的平衡常数K= ![]()
C.对于反应③,恒容时,温度升高,H2 的浓度减小,则该反应的焓变为正值
D.对于反应③,恒温恒容下,增大压强,H2 的浓度一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请回答有关问题: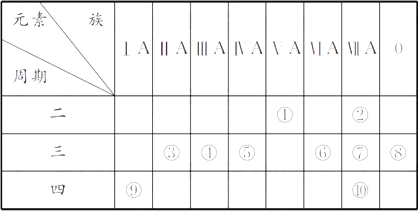
(1)⑤和⑧的元素符号分别是和。
(2)表中最活泼的金属是 , 非金属性最强的元素是(填元素符号,下同)。
(3)表中能形成两性氢氧化物的元素是 , 分别写出该元素的氢氧化物与⑥和⑨的最高价氧化物的水化物反应的化学方程式:。
(4)请设计一个实验方案,比较⑦和⑩的单质氧化性的强弱:。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普伐他汀是一种调节血脂的药物,其结构简式如图所示.下列说法不正确的是( ) 
A.普伐他汀分子中有4种含氧官能团
B.每个普伐他汀分子中含有13个手性碳原子
C.在一定条件下,普伐他汀能发生加成、取代、消去、缩聚反应
D.普伐他汀可以和NaOH溶液、Na2CO3溶液反应,还可以和酸性KMnO4溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表示正确的是( )
A.NaH与重水反应的方程式:NaH+D2O=NaOH+D2↑
B.三氟化氮的电子式: ![]()
C.熔融状态下硫酸氢钠的电离方程式:NaHSO4(熔融)=Na++HSO4﹣
D.羟基乙酸(HOCH2COOH)的缩聚物: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
(1)膦(PH3)是一种无色有剧毒的气体,其还原能力比氨(NH3)强,是一种强还原剂.某反应体系中存在下列物质:Cu、H2SO4、CuSO4、PH3、H3PO4、H2O.回答下列问题:
①上述反应体系中化学反应方程式为;
②膦(PH3)能和水发生微弱的化学反应,其水溶液呈弱碱性,该反应可用离子方程式表示为 .
(2)生活污水中含大量细小的悬浮物,可加某些物质使之聚集成较大的颗粒而沉淀.请你举一种常见的能使生活污水中悬浮物聚沉的物质,其化学式为 .
(3)用CH4催化还原NOX可以消除氮氧化物的污染.例如
CH4(g)+4NO2(g) 4NO(g)+CO2 (g)+2H2O(g)△H1=﹣574kJmol﹣1
CH4(g)+4NO(g)2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2 , 整个过程中放出的热量为867kJ,则△H2= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com