
| A. | 紫色石蕊溶液 | B. | 无色酚酞溶液 | C. | 碳酸钠溶液 | D. | 硝酸钾溶液 |
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:选择题
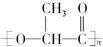 ,该酯可以作为新型的餐具原料.由它所产生的塑料在乳酸菌作用下,能迅速分解为无毒物质,可以降解.下列有关这种新型的可降解塑料的叙述正确的是( )
,该酯可以作为新型的餐具原料.由它所产生的塑料在乳酸菌作用下,能迅速分解为无毒物质,可以降解.下列有关这种新型的可降解塑料的叙述正确的是( )| A. | 降解塑料是一种纯净物 | |
| B. | 其生产过程中的聚合方式与聚苯乙烯相似 | |
| C. | 它属于一种线型高分子材料 | |
| D. | 其相对分子质量为72 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16 g O2所含的原子数目为NA | |
| B. | 0.5 mol H2O2含有的原子数目为1.5NA | |
| C. | 1 mol H2O含有的H2O分子数目为NA | |
| D. | 0.5NA个氯气分子的物质的量是0.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯分子中共平面的原子最多是12个 | |
| B. | 对二甲苯分子中有4个碳原子在一条直线上 | |
| C. | 1-丁烯分子中的4个碳原子一定不在同一平面内 | |
| D. | 2-丁烯分子中的4个碳原子一定不在同一平面内 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鸡蛋白溶胶中加入饱和硫酸铵溶液后有蛋白质析出 | |
| B. | 直径介于1nm~100nm之间的微粒称为胶体 | |
| C. | 因为液态氟化氢中存在氢键,所以其分子比氯化氢更稳定 | |
| D. | 电泳现象可证明胶体属于电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制氧气时,用Na2O2或H2O2做反应物可选择相同的气体发生装置 | |
| B. | 制氯气时,用饱和NaHCO3和浓硫酸净化气体 | |
| C. | 制氨气时,用排水法或向上排空气法收集气体 | |
| D. | 制二氧化氮时,用水或NaOH溶液吸收尾气 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com