
【题目】如图为某市售盐酸试剂瓶上的部分数据:

(1)该市售盐酸的物质的量浓度为_________mol/L。(计算结果精确到小数点后1位,下同)
(2)欲配制1mol/L盐酸溶液475mL,则需量取该市售盐酸_____mL,除烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是________;下列情况会使所配溶液浓度偏高的是______(填序号)
A.量筒使用前用未干燥
B.用量筒量取浓盐酸时,俯视刻度线
C.量取出的浓盐酸露置较长时间后才加水稀释
D.洗涤量取浓盐酸的量筒,并将洗涤液转移到容量瓶中
(3)浓度均为1mol/L的盐酸与氢氧化钡溶液等体积混合后OH-的物质的量浓度=___________mol/L(忽略溶液体积变化);质量分数分别为36.5%和13.5%的盐酸等体积混合,所得溶液的质量分数__________25%(填“>”“<”或“=”);在标准状况下,1体积水吸收__________体积的HCl气体可制得36.5%的盐酸(水的密度以1.00g/cm3计)。
【答案】11.8 42.4 玻璃棒和500mL容量瓶 D 0.5 > 352.8
【解析】
(1)根据c=1000ρw/M计算;
(2)依据稀释定律计算;根据配制一定物质的量浓度的步骤确定需用到的玻璃仪器;根据n=cV判断溶液中溶质的物质的量和溶液体积变化,进行误差分析;
(3)依据酸、碱的元次和化学方程式进行过量判断;盐酸浓度越大,溶液密度越大;依据c=n/V计算。
(1)根据c=1000ρw/M,密度为1.18g/mL、质量分数为36.5%的浓盐酸的物质的量为:(1000×1.18×36.5%)/36.5mol/L=11.8mol/L,故答案为:11.8 mol/L;
(2)①实验室应该用500ml容量瓶配制475mL1mol/L盐酸溶液,设需要浓盐酸的体积为VL,由稀释定律可得:VL×11.8mol/L=0.5L×1mol/L,解得V=0.0424L=42.4ml,故需要量取浓盐酸42.4ml,故答案为42.4ml;
②配制475mL1mol/L稀盐酸时使用的仪器除烧杯、量筒、胶头滴管外,还必须用到玻璃棒、500mL容量瓶,故答案为:玻璃棒、500mL容量瓶;
③A项、量筒使用前用未干燥,量取的浓盐酸体积偏小,溶质的物质的量偏小,导致所配溶液浓度偏低,故A错误;
B项、定容时仰视容量瓶刻度线,所配溶液体积偏大,导致所配溶液浓度偏低,故B错误;
C项、量取出的浓盐酸露置较长时间,浓盐酸挥发,溶质物质的量减小,配制的标准液浓度减小,故C错误;
D项、量筒使用错误,使用量同时不需要洗涤量筒,若洗涤量筒并将洗涤液倒入烧杯,相当多量取盐酸,n值偏高,c偏高,故D正确;
故答案为:D;
(3)①浓度均为1mol/L的盐酸与氢氧化钡溶液等体积混合,氢氧化钡过量,设溶液的体积为VL,则溶液中c(OH—)=(1mol/L×VL×2—1mol/L×VL)/2VL=0.5 mol/L,故答案为:0.5 mol/L;
②盐酸浓度越大,溶液密度越大,设溶液的体积为Vml,质量分数分别为36.5%和13.5%的盐酸等体积混合,所得溶液的质量分数(36.5%×V d1+13.5%×V d2)/(V d1+V d2)= 13.5%+23% d1/( d1+Vd2) >13.5%+23%×1/2=25%,故答案为:>;
③设水的体积为1L,HCl的体积为xL,则HCl的物质的量为x/22.4mol,HCl的质量为36.5x/22.4 g,1L水的质量为1000mL×1g/mL=1000g,则有(1000g+36.5x/22.4 g)×36.5%=36.5x/22.4 g,解得x=352.8g,故答案为:352.8。


科目:高中化学 来源: 题型:
【题目】(1)写出下图中序号①~③仪器的名称:
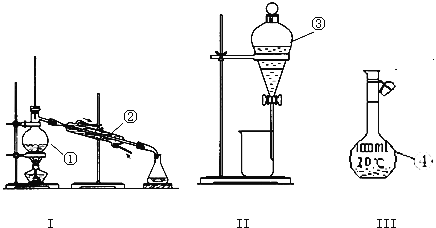
①_________;② _________;③__________ ;
仪器①~④中,使用时必须检查是否漏水的有 _______.(填仪器序号)
(2)如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.

现用该浓硫酸配制480mL1molL-1的稀硫酸.请回答下列问题:
a. 该硫酸的物质的量浓度为__________molL-1
b.经计算,配制480mL1molL-1的稀硫酸需要用量筒量取上述浓硫酸的体积为_______mL;
c.配制过程中下列各项操作会导致所配稀硫酸浓度偏小的是_____(双选)
A.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
B.所选用的烧杯、玻璃棒未洗涤
C.定容时,俯视容量瓶刻度线
D.摇匀后静置发现液面低于刻度线,继续滴加蒸馏水至刻度处.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钾和钠的化学性质相似,下列说法中能最好的解释这个事实的是( )
A.都是金属元素
B.原子半径相差不大
C.原子的最外层电子数相同
D.最高化合价相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以A为原料可制备C(丹皮酚)和D(树脂),其合成路线如下:

(1)A在空气中会缓慢变成粉红色,其原因是_____________________________________。
(2)A→B的反应类型为______________________;A生成D的反应中,试剂X(烃的含氧衍生物)为____________________(写结构简式)。
(3)只含有两个取代基的芳香化合物E是C的同分异构体,E既能与FeCl3溶液发生显色反应又能发生银镜反应和水解反应,则E共有________种(不考虑立体结构),其中核磁共振氢谱为六组峰且峰面积比为1:1:2:2:2:2 的结构简式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL0.1mol/L氨水中滴加一定浓度的稀盐酸,溶液中水电离的氢离子浓度随加入盐酸体积的变化如右图所示。下列说法错误的是
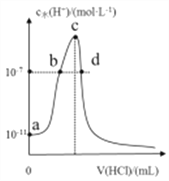
A. 常温下,0.1mol/L氨水的电离平衡常数Kb约为1.0×10-5
B. a、b之间的点一定满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C. c点溶液中c(NH4+)-)
D. c点溶质为NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸牛奶中的乳酸可增进食欲、促进胃液分泌、增强肠胃的消化功能,对人体具有保健作用,乳酸分子的结构简式为![]() 。工业上可由乙烯来合成乳酸,方法如下:
。工业上可由乙烯来合成乳酸,方法如下:

(1)乳酸所含的官能团的名称是_________________________。
(2)写出下列物质转化的化学方程式:
①A→B______________________________________。
②B→CH3CHO____________________________________。
③![]() __________________________________。
__________________________________。
(3)A在一定条件下可发生消去反应,写出其发生消去反应的化学方程式:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 金属铜与硝酸银溶液反应:Cu+Ag+ =Cu2++Ag
B. Ba(OH)2溶液和H2SO4溶液反应:Ba2+ + OH- + H+ + SO42- = BaSO4↓+ H2O
C. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
D. 石灰乳与盐酸反应:Ca(OH)2+2H+ = Ca2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国科学家威廉·诺尔斯、柏利·沙普利斯和日本化学家野依良治因通过使用快速和可控的重要化学反应来合成某些手性分子的方法而获得2001年的诺贝尔化学奖。所谓手性分子是指在分子中,当一个碳原子上连有彼此互不相同的四个原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子。凡是有一个手性碳原子的物质一定具有光学活性。例如,有机化合物: 有光学活性。则该有机化合物分别发生如下反应后,生成的有机物仍有光学活性的是( )
有光学活性。则该有机化合物分别发生如下反应后,生成的有机物仍有光学活性的是( )
A. 与乙酸发生酯化反应 B. 与NaOH水溶液共热
C. 在催化剂存在下与氢气作用 D. 与银氨溶液作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将牛奶和姜汁混合,待牛奶凝固便成为一种富有广东特色的甜品——姜撞奶。为了掌握牛奶凝固所需的条件,某同学在不同温度的等量牛奶中混人一些新鲜姜汁,观察混合物15min,看其是否会凝固,结果如下表。请回答下列问题:
温度(℃) | 20 | 40 | 60 | 80 | 100 |
结果 | 15min后仍未有凝固迹象 | 14min内完全凝固 | 1min内完全凝固 | 1min内完全凝固 | 15min后仍未有凝固迹象 |
(注:用曾煮沸的姜汁重复这项实验,牛奶在任何温度下均不能凝固)
(1)实验证明新鲜姜汁中含有一种酶,其作用是 。
(2)20℃和100℃时,15min后仍未有凝固迹象,说明酶的活性较低,其原因分别是 和 。
(3)若60℃时牛奶在有姜汁和没有姜汁的情况下都可以凝固,当反应进行到t时,向其中加人姜汁。下图中能正确表示加姜汁后牛奶凝固随时间变化趋势的曲线是 。
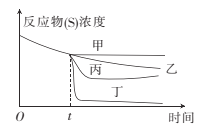
(4)为提高实验的准确度,实验中“不同温度的等量牛奶中混入一些新鲜姜汁”操作中应注意的是 。
(5)有同学说,该实验不能得出姜汁使牛奶凝固的最适温度,请提出解决方案: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com