
下列关于碱金属元素和卤素的说法中,错误的是( )
A.随核电荷数的增加,碱金属元素和卤素的熔沸点都逐渐降低
B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强
C.钾与水的反应比钠与水的反应更剧烈
D.溴单质与H2的反应比碘单质与H2的反应更剧烈
科目:高中化学 来源:2013-2014山西省汾阳市高一期末统考化学试卷(解析版) 题型:选择题
下列叙述正确的是 ( )
A.40K和 40Ca原子中质子数和中子数都不相等
B.金刚石和石墨的性质相同
C.H2和D2互为同位素
D.某物质只含一种元素,该物质一定是纯净物
查看答案和解析>>
科目:高中化学 来源:2013-2014山西省第二学期期末考试高一化学试卷(解析版) 题型:选择题
有机物乙苯 的一溴取代物的同分异构体有( )
的一溴取代物的同分异构体有( )
A.5种 B.6种 C.7种 D.8种
查看答案和解析>>
科目:高中化学 来源:2013-2014山西省高一下学期期中化学试卷(解析版) 题型:选择题
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4Al + 3O2 + 6H2O = 4Al(OH)3,下列说法不正确的是( )
A.正极反应式为:O2 + 2H2O + 4e- = 4OH-
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需更换铝板就可继续使用
查看答案和解析>>
科目:高中化学 来源:2013-2014山西省高一下学期期中化学试卷(解析版) 题型:选择题
下列各组物质中化学键的类型相同的是 ( )
A.CaCl2 MgCl2 Na2O B.H2O Na2O ? CO2
C.CaCl2 ? NaOH H2SO4 D.NH4Cl H2O CO2
查看答案和解析>>
科目:高中化学 来源:2013-2014山西省5月月考高二化学试卷(解析版) 题型:填空题
(9分)某有机化合物A含碳76.6%、含氢6.4%,A的相对分子质量约是甲烷的5.9倍。在常温下,该有机物的稀溶液可与浓溴水反应生成白色沉淀,1molA恰好跟3molBr2反应。
(1)求A的分子式 。
(2)写出A的稀溶液中滴加浓溴水的化学方程式。
(3)写出A与碳酸钠、碳酸氢钠溶液可能发生的反应的离子方程式。
查看答案和解析>>
科目:高中化学 来源:2013-2014山西省5月月考高二化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.乙酸与碳酸钠溶液反应:2H++CO32—== CO2↑+H2O
B.醋酸溶液与新制氢氧化铜反应:CH3COOH+OH- → CH3COO-+H2O
C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O → 2C6H5OH+CO32—
D.甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH-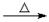 CO32—+2NH4++4Ag↓+6NH3+2H2O
CO32—+2NH4++4Ag↓+6NH3+2H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014山西省6月高二化学期末测试卷(解析版) 题型:实验题
(10分)1,2 -二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2 -二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。
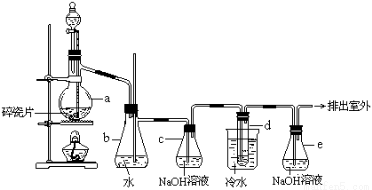
填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式。
______________________ ; 。
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象:____________________________________________。
(3)容器c中NaOH溶液的作用是:________________________________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因。__________
______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014山西大学附中高三第二学期5月理科综合化学试卷(解析版) 题型:选择题
硫酸亚铁是一种重要的化工原料,可以制备多种物质。有关下列制备方法错误的是
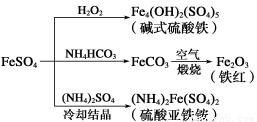
A.制备碱式硫酸铁利用了过氧化氢的氧化性
B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D.制备(NH4)2Fe(SO4)2利用了它的溶解度比FeSO4的溶解度大这一性质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com