

分析 (1)高碘酸H5IO6加入MnSO4溶液中可使溶液呈紫红色,这说明反应中有高锰酸钾生成,因此高碘酸是氧化剂,硫酸锰是还原剂.其中I元素的化合价从+7价降低到+5价,得到2个电子,Mn元素的化合价从+2价升高到+7价,失去5个电子,所以根据电子得失守恒可知,氧化剂与还原剂的物质的量之比是5:2,电子化合价降低的反应物是氧化剂、失电子化合价升高的反应物是还原剂;
(2)高碘酸H5IO6加入MnSO4溶液中可使溶液呈紫红色,这说明反应中有高锰酸钾生成,因此高碘酸是氧化剂,硫酸锰是还原剂.其中I元素的化合价从+7价降低到+5价,得到2个电子,Mn元素的化合价从+2价升高到+7价,失去5个电子,所以根据电子得失守恒可知,氧化剂与还原剂的物质的量之比是5:2;
(3)若向H5IO6溶液中加入足量的下列物质,能将碘元素还原成碘离子,说明该物质具有还原性,且选项中物质生成的单质或离子氧化性要小于碘;
(4)向含1mol H5IO6 的溶液中加入过量的过氧化氢溶液,再加入淀粉溶液,溶液变蓝,这说明有单质碘生成,同时有大量气体产生,该气体应该是氧气,根据反应物和生成物书写方程式;根据转移电子守恒计算.
解答 解:(1)高碘酸H5IO6加入MnSO4溶液中可使溶液呈紫红色,这说明反应中有高锰酸钾生成,因此高碘酸是氧化剂,硫酸锰是还原剂.其中I元素的化合价从+7价降低到+5价,得到2个电子,Mn元素的化合价从+2价升高到+7价,失去5个电子,所以根据电子得失守恒可知,氧化剂与还原剂的物质的量之比是5:2,电子化合价降低的反应物是氧化剂、失电子化合价升高的反应物是还原剂,
所以H5IO6是氧化剂、MnSO4是还原剂,且二者计量数之比为5:2,
故答案为:5H5IO6;2MnSO4;
(2)高碘酸H5IO6加入MnSO4溶液中可使溶液呈紫红色,这说明反应中有高锰酸钾生成,因此高碘酸是氧化剂,硫酸锰是还原剂.其中I元素的化合价从+7价降低到+5价,得到2个电子.Mn元素的化合价从+2价升高到+7价,失去5个电子,所以根据电子得失守恒可知,氧化剂与还原剂的物质的量之比是5:2,因此电子转移的方向和数目为 ,
,
故答案为: ;
;
(3)由于氯气、单质溴以及铁离子的氧化性均强于单质碘,所以选项acd不可能将高碘酸还原为碘离子,单质碘的氧化性强于S的,因此H2S可以把高碘酸还原为碘离子,故选b;
(4)向含1mol H5IO6 的溶液中加入过量的过氧化氢溶液,再加入淀粉溶液,溶液变蓝,这说明有单质碘生成,同时有大量气体产生,该气体应该是氧气,所以反应的化学方程式为2H5IO6+7H2O2=I2+12H2O+7O2↑,其中氧气的物质的量1mol÷2×7×22.4L/mol=3.5mol,在标准状况下的体积是3.5mol×22.4L/mol=78.4L,
故答案为:2H5IO6+7H2O2=I2+12H2O+7O2↑;78.4.
点评 本题考查氧化还原反应的判断、配平、应用以及有关计算等,为高频考点,侧重考查学生分析计算能力,正确书写方程式是解本题关键,注意反应中存在原子守恒和转移电子守恒,题目难度中等.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:解答题
 从原子、分子水平上帮助我们认识物质构成的规律:以微粒之间不同的作用力为线索,研究不同类型物质的有关性质:从物质结构决定性质的视角预测物质的有关性质.
从原子、分子水平上帮助我们认识物质构成的规律:以微粒之间不同的作用力为线索,研究不同类型物质的有关性质:从物质结构决定性质的视角预测物质的有关性质. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
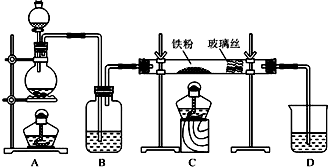
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.3克金属钠在干燥空气中被氧化成氧化物时失去的电子数目为0.1NA | |
| B. | 18克水所含的质子数目为NA | |
| C. | 在常温常压下,11.2升氯气所含的分子数目为0.5NA | |
| D. | 32克臭氧所含的原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )
美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )| A. | a极为电池的正极 | |
| B. | b极发生氧化反应 | |
| C. | 负极的反应为:4H++O2+4e-═2H2O | |
| D. | 电池工作时,1mol乙醇被氧化时有12mol转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合成氨的化学反应限度最大 | |
| B. | N2的转化率最高 | |
| C. | 催化剂的活性最大 | |
| D. | NH3在平衡混合气体中的体积分数最大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com