
下列关于苯的叙述正确的是
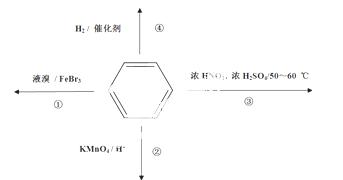
A.反应①常温下不能进行,需要加热
B.反应②不发生,但是仍有分层现象,紫色层在下层
C.反应③为加成反应,产物是一种烃的衍生物
D.反应④能发生,从而证明苯中是单双键交替结构
科目:高中化学 来源: 题型:
(1)请将下列五种物质:KBr、Br2、I2、KI、K2SO4分别填入下列横线上,组成一个未配平的化学方程式:
KBrO3+________+H2SO4—→________+________+________+________+H2O。
(2)如果该化学方程式中I2和KBr的化学计量数分别是8和1,则
①Br2的化学计量数是________;
②请将反应物的化学式及配平后的化学计量数填入下列相应的位置中:
KBrO3+ ________+ H2SO4—→;
③若转移10 mol e-,则反应后生成I2的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
LiPF6是锂离子电池中广泛应用的电解质。某工厂用LiF、PCl5为原料,低温反应制备LiPF6,其流程如下:
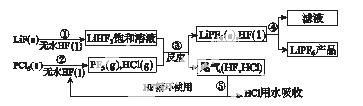
已知:HCl的沸点是-85.0 ℃,HF的沸点是19.5 ℃。
(1)第①步反应中无水HF的作用是________________、________________。反应设备不能用玻璃材质的原因是______________________________________________(用化学方程式表示)。无水HF有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的________溶液冲洗。
(2)该流程需在无水 条件下进行,第③步反应中PF5极易水解,其产物为两种酸,写出PF5水解的化学方程式:____________________________________。
条件下进行,第③步反应中PF5极易水解,其产物为两种酸,写出PF5水解的化学方程式:____________________________________。
(3)第④步分离采用的方法是________;第⑤步分离尾气中HF、HCl采用的方法是________。
(4)LiPF6产品中通常混有少量LiF。取样品w g,测得Li的物质的量为n mol,则该样品中LiPF6的物质的量为________mol(用含w、n的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是实验室蒸馏石油的实验装置,实验需要收集60~150 ℃和150~300 ℃的馏分。
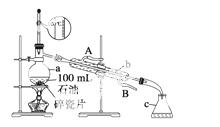
请回答下列问题:
(1)仪器a的规格和名称____________,仪器b、c的名称:b__ ______,c________。
______,c________。
(2)实验所选温度计是错误的,正确的选择应该是____________________________。
(3)实验时在仪器a中加入了少量碎瓷片,其目的是__________________________。
(4)实验时在仪器b中通入冷却水,请指明冷却水的流向
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对有机物结构或性质的描述,正确的是( )
A.甲苯中含有 少量苯酚,可加适量浓溴水,再过滤而除去
少量苯酚,可加适量浓溴水,再过滤而除去
B.苯的间二溴代物无同分异构体能说明苯不是单双键交替结构
C.使用酸性KMnO4溶液除去乙烷中混有的乙烯
D.一定条件下,Cl2在甲苯的苯环或侧链上均能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实。根据以下化学反应框图填空:
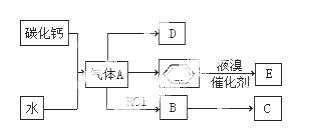
(1)写出A的电子式 ;D的最简式 ;
;D的最简式 ;
(2)写出碳化钙与水
 反应制取A的化学
反应制取A的化学 方程式 ;苯和液溴反应生成E的化学方程式 ,其反应类型为 。B→C的化学方程式 ,其反应类型为 。
方程式 ;苯和液溴反应生成E的化学方程式 ,其反应类型为 。B→C的化学方程式 ,其反应类型为 。
(3)D还可以用石蜡油制取,D在一定条件下存在如下转化关系(石蜡油含17个碳原子以上的液态烷烃,部分反应条件、产物被省略),G是一种酸性物质,H是具有果香气味的烃的衍生物。
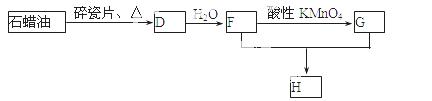
a.工业上,由石油获得汽油、煤油、石蜡油等成份的方法是 ;
b.D→F的化学方程式 
 ,其反应类型是 。
,其反应类型是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
LiPF6是锂离子电池中广泛应用的电解质。某工厂用LiF、PCl5为原料,低温反应制备LiPF6,其流程如下:
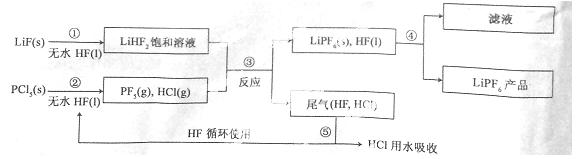
已知:HCl的沸点是-85.0 ℃,HF的沸点是19.5 ℃。
(1)第①步反应中无水HF的作用是 、 。反应设备不能用玻璃材质的原因是 (用化学方程式表示)。无水HF有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的 溶液冲洗。
(2)该流程需在无水条件下进行,第③步反应中PCl5极易水解,其产物为两种酸,写出PF5水解的化学方程式: 。
(3)第④步分离采用的方法是 ;第⑤步分离尾气中HF、HCl采用的方法是 。
(4)LiPF6产品中通常混有少量LiF。取样品wg,测得Li的物质的量为nmol,则该样品中LiPF6的物质的量为 mol(用含有w、n的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌。同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO4·7H2O)。某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾。制备皓矾的实验流程如下图所示。

已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为Fe(OH)3:2.7~3.7;Fe(OH)2:7.6~9.6;Zn(OH)2:5.7~8.0,试回答下列问题:
(1)加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,最好选用________,其理由是
______________________________________________________________________。
(2)加入的试剂②:供选择使用的有:a.Zn粉、b.ZnO、c.Zn(OH)2、d.ZnCO3、e.ZnSO4等,可选用__________。
(3)从晶体1→晶体2,该过程的名称是__________。
(4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是_____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
人体吸入的空气与呼出的气体中所含气体体积的比较,正确的是
①氧气:空气﹥呼出气体;②二氧化碳:空气﹤呼出气体;③水蒸气:空气﹥呼出气体。
A.②③ B.①② C.①③ D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com